紫杉醇(Paclitaxel, PTX)是一種重要的紫杉烷類化療藥物��。紫杉醇的抗腫瘤活性來自其與微管的高親和力�,穩(wěn)定和改善微管蛋白的聚合,有效抑制細胞有絲分裂�、細胞內(nèi)轉(zhuǎn)運,最終導(dǎo)致腫瘤細胞凋亡�。紫杉醇由于水溶性差和滲透性差,口服生物利用度低��,其天然形式臨床應(yīng)用受到限制��。此外����,由于其結(jié)構(gòu)中缺乏可修飾的功能基團,因此在試圖提高其溶解度時��,對天然紫杉醇進行化學改變非常復(fù)雜�����。因此����,選擇合適的給藥系統(tǒng)對提高紫杉醇的臨床應(yīng)用��、安全性和有效性至關(guān)重要��。
Taxol®是紫杉醇的第一個通用產(chǎn)品�����,采用了50:50乙醇和Cremophor ELTM(聚氧乙基化蓖麻油)混合物的共溶劑策略��。雖然該方法克服了溶解度問題��,但Cremophor ELTM存在非線性藥代動力學和嚴重的劑量限制性毒性��,如超敏反應(yīng)�����、神經(jīng)毒性和腎毒性���。由于這些不良反應(yīng),Taxol ®以135或175 mg/m2的劑量�����,每3周~4周給藥1次,每次需要輸注3小時以上�����。為了預(yù)防發(fā)生過敏反應(yīng),在紫杉醇治療前12小時口服地塞米松10mg��,治療前�����,6小時再囗服地塞米松10mg,治療前30~60分鐘給予苯海拉明肌注20mg���,靜注西咪替丁300mg或雷尼替丁50mg。此外����,Cremophor ELTM需要使用特殊的IVEX-2過濾器,以避免濾器中增塑劑浸出到產(chǎn)品中�。Taxol®規(guī)格為5ml:30mg的凍干粉,使用前需要用葡萄糖或生理鹽水稀釋���,單次使用量為7-9瓶��。
考慮到Cremophor ELTM毒性較大����,開發(fā)不含Cremophor ELTM,且溶解性好的紫杉醇制劑成為臨床急需�。2003年在中國獲得批準紫杉醇脂質(zhì)體(力樸素),它是一種由PTX����、卵磷脂﹑膽固醇﹑蘇氨酸﹑葡萄糖組成的脂質(zhì)體。與Taxol®相比�,力樸素對乳腺癌、非小細胞肺癌和胃癌具有相似的活性���,但副作用要小得多����。力樸素規(guī)格與給藥劑量與Taxol®一致����。與Taxol®相似,為預(yù)防紫杉醇可能發(fā)生的過敏反應(yīng)�����,在使用前30分鐘需要預(yù)處理:靜脈注射地塞米松5-10mg;肌肉注射苯海拉明50mg����;靜脈注射西米替丁300mg。
Abraxane TM是PTX的另一種上市藥物�����,由Abraxis BioScienc生產(chǎn)�����,并于2005年獲得FDA批準��。本品中PTX的配制采用人血清白蛋白(HSA)�。HSA是血液中含量最多的血漿蛋白����,其半衰期長達19小時,可與疏水物質(zhì)不可逆結(jié)合��,在體內(nèi)運輸�,并將其運送到細胞表面。此外����,HSA在細胞攝取和胞吞作用中起著重要作用����,因為它與gp60和其他在惡性細胞中高表達的蛋白質(zhì)(如酸性和富含半胱氨酸的分泌蛋白(SPARC))結(jié)合����。根據(jù)Abraxis BioSciences公司獲得的結(jié)果,Abraxane TM具有線性藥代動力學特征��,與Taxol®相比�����,其瘤內(nèi)濃度高出33%��。給藥劑量提高至260mg/m2�����,滴注時間縮短為30分鐘且無需進行過敏預(yù)處理�。Abraxane TM規(guī)格為100mg,單次使用量約為4瓶。目前�,石藥歐意藥業(yè)、江蘇恒瑞醫(yī)藥��、湖南科倫制藥、海正藥業(yè)等6家國內(nèi)藥企均已過評注射用紫杉醇(白蛋白結(jié)合型)����。
另一種上市藥物Genexol-PMTM由Samyang Corporation公司開發(fā),于2007年在韓國獲得批準�����。它由PTX和聚乙二醇-聚乳酸嵌段聚合組成的膠束��。粒徑為20~50nm����。臨床研究表明��,Genexol-PMTM具有劑量依賴的藥代動力學和良好的耐受性�,特別是對晚期胰腺癌或轉(zhuǎn)移性乳腺癌患者。2018年, 歐盟批準Oasmia公司 Apealea®上市��,聯(lián)合卡鉑用于首次復(fù)發(fā)的鉑敏感性上皮性卵巢癌��、原發(fā)性腹膜癌��、輸卵管癌成人患者的治療��。此次批準適用于28個歐盟成員國及歐洲經(jīng)濟區(qū)成員國冰島、列支敦士登和挪威�。該產(chǎn)品也是一種紫杉醇膠束,使用公司專有的賦形劑XR17����。XR17是一種基于維生素A的物質(zhì),可形成 20-60nm大小的膠束���。2021 年�,上海宜眾紫杉醇膠束獲得NMPA批準上市�,該產(chǎn)品以自主研發(fā)的全新藥用輔料單甲氧基聚乙二醇 2000-聚丙交酯兩親嵌段共聚物為載體,的由于mPEG長循環(huán)作用�,聚合物膠束包載的紫杉醇緩慢釋放,24小時內(nèi)釋放65%���,48小時釋放95%��。使用該產(chǎn)品前無需以抗組胺藥進行預(yù)處理����,最高耐受劑量為390 mg/m2��,高于紫杉醇注射液(Taxol)的200 mg/m2和紫杉醇白蛋白納米粒(Abraxane)的300 mg/m2����。
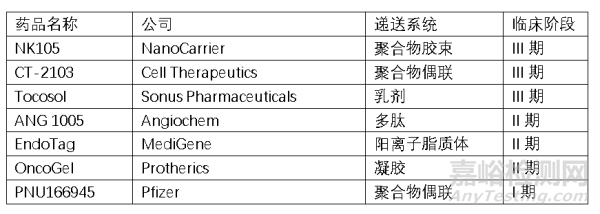
以上幾個產(chǎn)品均是針對紫杉醇注射液毒性及溶解性進行改良��,然而Genexol PM®在物理上不穩(wěn)定���,對多藥耐藥腫瘤治療無效。Abraxane®表現(xiàn)出有限的腫瘤攝取����、腫瘤消除和更高的半數(shù)抑瘤濃度。更多的遞送系統(tǒng)進一步開發(fā)�,根據(jù)文獻報道與Genexol PM®相比,聚乙二醇-共乳酸和d -a-生育酚聚乙二醇- 1000琥珀酸鹽組成的紫杉醇混合膠束對多藥耐藥腫瘤細胞有效;與Abraxane®相比�,重組嵌合多肽結(jié)合的紫杉醇納米顆粒具有2倍的全身腫瘤暴露,腫瘤攝取和幾乎完全的腫瘤消退�;紫杉醇載聚己內(nèi)酯-co- d -a-生育酚聚乙二醇1000琥珀酸納米顆粒的最大抑制濃度是Abraxane®的8倍;以下是一些進入臨床的新型紫杉醇制劑�。
2.口服劑型
為了提高臨床使用順應(yīng)性,同時降靜脈注射可能引發(fā)的注射液外滲�、靜脈炎等不良反應(yīng)口服紫杉醇制劑也一直是研發(fā)熱點。紫杉醇在口服時����,會被胃腸道細胞的P-糖蛋白泵排出。為此����,Athenex公司通過與新型P-糖蛋白抑制劑Encequidar進行聯(lián)合口服��,對腸道中P-糖蛋白的活性進行局部抑制�����,從而在提高藥物吸收����,減少副作用���。與傳統(tǒng)靜脈注射紫杉醇相比���,口服紫杉醇組的療效顯著提高,總緩解率為36%����,而靜脈注射紫杉醇組為24%;同時����,神經(jīng)病變發(fā)生率和嚴重程度較低,脫發(fā)�����,關(guān)節(jié)痛和肌痛的發(fā)生率也降低。然而����,F(xiàn)DA拒絕了該療法上市申請,理由是與靜脈注射紫杉醇相比��,口服紫杉醇可能有4級中性粒細胞減少���,3級嘔吐和未確定的胃腸道并發(fā)癥���,而這些副作用可能危及患者生命或者需要住院治療。并且該療法給藥機制所依賴的Encequidar成分并沒有得到FDA的審批����。FDA認為,如果想要獲得批準����,就需要采取額外的風險緩解策略來改善產(chǎn)品的毒性問題�����,包括劑量優(yōu)化和/或排除被認為具有高毒性風險的患者。另一種口服制劑RMX3001(韓國原產(chǎn)品代碼為DHP107����,注冊名為Liporaxel)是由DAEHWA Pharmaceuticals韓國大化公司與韓國科學技術(shù)研究所共同開發(fā),已于2016年9月9日成功獲得韓國食品與藥品監(jiān)督局的上市批準����,適應(yīng)癥為晚期和轉(zhuǎn)移性或局部復(fù)發(fā)性胃癌,是全球第一個開發(fā)成功并獲批上市的口服紫杉醇產(chǎn)品�。其優(yōu)勢在于Liporaxel是在脂質(zhì)自乳化DH-LASED技術(shù)的基礎(chǔ)上開發(fā)的,脂質(zhì)形成膠束�,黏附于小腸絨毛,脂乳吸收過程中形成藥物乳糜顆粒而被吸收�����。該產(chǎn)品無需給藥預(yù)防超敏反應(yīng)���,無注射型紫杉醇帶來不良反應(yīng)���;可在不使用P-糖蛋白抑制劑或吸收促進劑的情況下施用。一項多中心�、隨機、開放的III期臨床研究比較紫杉醇口服溶液(RMX3001/DHP107)與紫杉醇注射液(泰素®) 二線治療晚期胃癌患者療效和安全。結(jié)果顯示口服溶液療效不遜于紫杉醇注射液(泰素®)�����,神經(jīng)毒性��、白細胞減少���、脫發(fā)等不良反應(yīng)較注射液更輕�����。
3�、改劑型新藥設(shè)計考慮
紫杉醇制劑從普通的注射劑到采用各種遞藥系統(tǒng)改善毒性和溶解性注射劑再到增加順應(yīng)性降低毒性的口服制劑�。從不同紫杉醇制劑的開發(fā)歷程可以看出改劑型新藥設(shè)計上首先要立足于明確的臨床需求,比如提高有效性��、改善安全性�����、提高依從性�。其次,要有一定的技術(shù)儲備����,在對原料的藥學性質(zhì)充分了解的基礎(chǔ)上結(jié)合自身的技術(shù)平臺(新輔料、新技術(shù)等)進行新劑型的開發(fā)����;采用新輔料時,一定要對新輔料的安全性進行充分評估�����;改變給藥途徑后密切關(guān)注其藥動學變化及由此帶來的其他副作用����。此外,臨床實驗的設(shè)計也至關(guān)重要�����,選擇合適的適應(yīng)癥����,合適的試驗人群,合理的給藥劑量是項目成功的助推器�����。綜上所述:臨床需求,先進的技術(shù)平臺�����,創(chuàng)意的想法以及合理的臨床實驗設(shè)計是成功開發(fā)改良型新的關(guān)鍵要素���。
參考文獻
1. Haddad, R.; Alrabadi, N.; Altaani, B.; Li, T. Paclitaxel Drug Delivery Systems: Focus on Nanocrystals’ Surface Modifications. Polymers 2022, 14, 658.
2. A, P., Kar, S., Vignesh, K., Kolhe, U.D. (2020). An Overview of Paclitaxel Delivery Systems. In: Saneja, A., Panda, A., Lichtfouse, E. (eds) Sustainable Agriculture Reviews 43. Sustainable Agriculture Reviews, vol 43. Springer, Cham.
3. Ma P, Mumper RJ. Paclitaxel Nano-Delivery Systems: A Comprehensive Review. J Nanomed Nanotechnol. 2013 Feb 18;4(2):1000164.