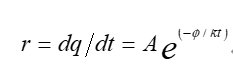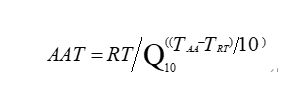1.貨架有效期影響因素
影響醫(yī)療器械貨架有效期的因素有很多,此處列舉了部分與無源植入性醫(yī)療器械密切相關(guān)的影響因素�,但不僅限于以下內(nèi)容:
外部影響因素主要包括:
- 儲存條件,例如溫度�����、濕度���、光照��、通風(fēng)情況�����、氣壓�、污染等���;
- 運輸條件�����,例如運輸過程中的震動���、沖撞���。
內(nèi)部影響因素主要包括:
- 醫(yī)療器械中各原材料/組件自身隨時間的推移而發(fā)生退化的特性,如某些高分子材料����、某些藥械組合產(chǎn)品中的藥物成分等;
- 醫(yī)療器械中各原材料/組件之間可能發(fā)生的相互作用���;
- 醫(yī)療器械中各原材料/組件與包裝材料(包括保存介質(zhì))之間可能發(fā)生的相互作用�;
- 醫(yī)療器械中各原材料/組件�����、包裝材料因生產(chǎn)工藝而造成的影響����,如生產(chǎn)過程中采用的輻照滅菌工藝等;
- 醫(yī)療器械中含有的放射性物質(zhì)和其放射衰變后的副產(chǎn)物對醫(yī)療器械中原材料/組件���、包裝材料的影響�����;
- 無菌包裝產(chǎn)品中微生物屏障的保持能力��。
內(nèi)部因素和外部因素均可不同程度地影響醫(yī)療器械產(chǎn)品的技術(shù)性能指標(biāo)�����,當(dāng)不能達(dá)到預(yù)期性能時可能造成器械失效�。注冊申請人宜盡可能將各因素進(jìn)行有效控制�����,使其對醫(yī)療器械技術(shù)性能指標(biāo)造成的影響降至最低�。
此外,產(chǎn)品設(shè)計開發(fā)時還需考慮以下因素對貨架有效期設(shè)定的影響:
- 原輔材料的影響�,如供應(yīng)商、質(zhì)量標(biāo)準(zhǔn)����、穩(wěn)定性等;
- 生產(chǎn)方式����,采用不同方式生產(chǎn)的同一醫(yī)療器械產(chǎn)品可能具有不同的貨架有效期�����;
- 生產(chǎn)環(huán)境���,如無菌醫(yī)療器械生產(chǎn)場所的潔凈度、溫度和濕度���、微生物及懸浮粒子負(fù)荷等����;
- 包裝����,例如在不同尺寸包裝容器中的液體產(chǎn)品可能因為與容器接觸的比表面積不同而具有不同的貨架有效期;
- 其他影響因素��,如生產(chǎn)設(shè)備改變的影響及設(shè)備所用清洗劑�、脫模劑的影響。
當(dāng)以上因素發(fā)生改變時���,可能導(dǎo)致貨架有效期的改變���,必要時重新驗證�����。
2.貨架有效期驗證過程
注冊申請人需對貨架有效期進(jìn)行研究�,證明在其規(guī)定的貯存運輸條件下�����,產(chǎn)品在貨架有效期內(nèi)滿足使用要求�。
醫(yī)療器械貨架有效期的驗證貫穿該器械研發(fā)的整個過程�,并在產(chǎn)品的驗證、改進(jìn)過程中不斷進(jìn)行確認(rèn)�����。
注冊申請人需合理設(shè)計醫(yī)療器械貨架有效期驗證方案�,并依據(jù)方案開展驗證,當(dāng)驗證結(jié)果不支持設(shè)定的貨架有效期時�,可對產(chǎn)品進(jìn)行改進(jìn)或根據(jù)已有的驗證結(jié)果重新設(shè)定貨架有效期。
3.貨架有效期驗證內(nèi)容
驗證試驗類型: 醫(yī)療器械貨架有效期的驗證試驗通?����?煞譃榧铀俜€(wěn)定性試驗、實時穩(wěn)定性試驗兩類�。
加速穩(wěn)定性試驗
加速穩(wěn)定性試驗是將樣品貯存在某一較高的溫度,以縮短時間來模擬實時老化的試驗�����。
加速穩(wěn)定性試驗設(shè)計是建立在假設(shè)材料變質(zhì)所涉及的化學(xué)反應(yīng)遵循阿列紐斯(Arrhenius)反應(yīng)速率函數(shù)基礎(chǔ)上的�����。該函數(shù)以碰撞理論為基礎(chǔ)�,確認(rèn)化學(xué)反應(yīng)產(chǎn)生變化的反應(yīng)速率的增加或降低按照以下公式進(jìn)行:
r:反應(yīng)進(jìn)行的速率;A:材料的常數(shù)(頻率因子)�;φ:表觀活化能(eV);k:波爾茲曼常數(shù)(0.8617×10-4eV/K)����;t:絕對溫度。
需要注意的是�,并不是所有材料/組件的老化均符合該函數(shù)的熱力學(xué)老化特性。注冊申請人在使用該函數(shù)進(jìn)行加速穩(wěn)定性試驗設(shè)計之前需考慮其適用性���。
大量化學(xué)反應(yīng)的研究結(jié)果表明溫度升高或降低10℃會導(dǎo)致化學(xué)反應(yīng)速率增加一倍或減半�����。則可根據(jù)阿列紐斯反應(yīng)速率函數(shù)建立加速老化簡化公式:
AAT:加速老化時間��;RT:實時老化時間����;Q10:溫度升高或降低10℃的老化系數(shù);TAA:加速老化溫度�����;TRT:預(yù)設(shè)的實際貯存溫度����。
上述公式反映了加速穩(wěn)定性試驗中加速老化時間與對應(yīng)的實時老化時間的關(guān)系。
其中�����,Q10一般設(shè)定為2�,也可保守設(shè)定為1.8��。如注冊申請人在加速穩(wěn)定性試驗中設(shè)定的Q10大于2���,則需同時提供詳細(xì)的相關(guān)研究資料���。
設(shè)定較高的加速老化溫度TAA可減少加速穩(wěn)定性試驗的時間�。但是����,由于較高的溫度(如高于聚合物玻璃化轉(zhuǎn)變溫度)可能導(dǎo)致醫(yī)療器械原材料、組件和/或包裝材料的性質(zhì)發(fā)生改變或引發(fā)多級或多種化學(xué)反應(yīng)�����,造成試驗結(jié)果的偏差�����。因此��,加速老化溫度一般不宜超過60℃�����。如注冊申請人在加速穩(wěn)定性試驗中設(shè)定了更高的加速老化溫度���,亦需提供詳細(xì)的相關(guān)研究資料�。
TRT宜能夠代表產(chǎn)品實際貯存條件下的溫度����,可結(jié)合預(yù)期儲存溫度范圍���、已有同類產(chǎn)品歷史數(shù)據(jù)、器械和/或包裝材料穩(wěn)定性數(shù)據(jù)等設(shè)定TRT���,并提供制定依據(jù)��。如產(chǎn)品具有專用的標(biāo)準(zhǔn)或指導(dǎo)文件規(guī)定TRT的���,宜優(yōu)先采用。
有些產(chǎn)品不適用于上述加速穩(wěn)定性試驗設(shè)計的����,需要進(jìn)行實時穩(wěn)定性試驗,如某些藥械組合醫(yī)療器械產(chǎn)品中的藥物成分�����。
實時穩(wěn)定性試驗
實時穩(wěn)定性試驗是將樣品貯存在規(guī)定的實際貯存條件下進(jìn)行的試驗���。實時穩(wěn)定性試驗中,注冊申請人宜根據(jù)產(chǎn)品的實際生產(chǎn)�����、運輸和貯存情況確定適當(dāng)?shù)臏囟取穸?、光照等條件,在設(shè)定的觀察時間點對產(chǎn)品進(jìn)行測試��。
申請人可結(jié)合預(yù)期儲存溫度范圍�、已有同類產(chǎn)品歷史數(shù)據(jù)、器械和/或包裝材料穩(wěn)定性數(shù)據(jù)等設(shè)定實時老化溫度�。如產(chǎn)品具有專用的標(biāo)準(zhǔn)或指導(dǎo)文件規(guī)定實時老化溫度的,宜優(yōu)先采用��。
實時穩(wěn)定性試驗結(jié)果是驗證產(chǎn)品貨架有效期的直接證據(jù)����。當(dāng)加速穩(wěn)定性試驗結(jié)果與其不一致時,應(yīng)以實時穩(wěn)定性試驗結(jié)果為準(zhǔn)�����。
其他試驗條件的考慮
在加速及實時穩(wěn)定性研究中�,申請人宜根據(jù)產(chǎn)品特性和預(yù)期貯存條件進(jìn)行評估選擇合適的相對濕度,并提供選擇的理由和依據(jù)����。一般建議相對濕度60%±10%��。若濕度在有效期內(nèi)對產(chǎn)品性能影響顯著�����,建議申請人設(shè)置高濕度和/或低濕度等條件�����,對產(chǎn)品進(jìn)行最不利條件性能驗證���。若相對濕度在有效期內(nèi)對產(chǎn)品影響不大,可不對相對濕度進(jìn)行特殊要求����。
如有其他因素顯著影響產(chǎn)品的穩(wěn)定性,建議設(shè)定適宜的試驗條件進(jìn)行驗證���,如光照等�����。
驗證試驗測試/評價項目
無論加速穩(wěn)定性試驗還是實時穩(wěn)定性試驗,注冊申請人均需在試驗方案中設(shè)定測試項目���、測試方法及判定標(biāo)準(zhǔn)�����。當(dāng)沒有判定標(biāo)準(zhǔn)時���,可采用零點時間性能數(shù)據(jù)作為測試項目的參照指標(biāo)���。
測試項目僅需評估產(chǎn)品隨時間老化的相關(guān)性能,包括器械自身性能測試和包裝系統(tǒng)性能測試兩方面���。其中包裝系統(tǒng)性能測試主要目的是為了驗證包裝系統(tǒng)對微生物的屏障性能���,即無菌狀態(tài)/微生物限度要求的保持。如涉及產(chǎn)品的生物相容性隨時間可能發(fā)生改變的���,還需進(jìn)行生物學(xué)評價�����。
驗證試驗的產(chǎn)品
醫(yī)療器械貨架有效期驗證試驗宜采用與常規(guī)生產(chǎn)相同的終產(chǎn)品進(jìn)行�����,適宜項目(如包裝系統(tǒng)性能)可采用無產(chǎn)品或模擬產(chǎn)品的包裝進(jìn)行驗證�。
注冊申請人可對試驗產(chǎn)品進(jìn)行設(shè)計最差條件下的驗證試驗以保證試驗產(chǎn)品可代表最惡劣的生產(chǎn)情況,如進(jìn)行一個標(biāo)準(zhǔn)的滅菌周期后�����,附加一個或多個滅菌周期���,或采用幾種不同的滅菌方法����。
2����、使用穩(wěn)定性
宜將使用穩(wěn)定性與貨架有效期研究進(jìn)行區(qū)分。產(chǎn)品應(yīng)在正常使用�、維護(hù)(如適用)情況下的生命周期內(nèi)維持其安全性和有效性。植入部位和預(yù)期用途不同����,影響其使用穩(wěn)定性的因素也不同,適用時需考慮植入操作的影響�。對于無源植入性醫(yī)療器械,使用穩(wěn)定性一般可在性能研究中開展驗證。
3�����、運輸穩(wěn)定性
運輸穩(wěn)定性通常通過模擬運輸試驗進(jìn)行�,通過模擬運輸過程中環(huán)境(溫度�����、濕度�、氣壓等)變化、跌落��、碰撞�、振動、加速度等����,產(chǎn)品不會發(fā)生性能、功能改變��,包裝系統(tǒng)具有保護(hù)產(chǎn)品的能力����。經(jīng)過模擬試驗后,觀察包裝外觀是否有不可接受的異常現(xiàn)象����,測試產(chǎn)品性能功能是否符合要求,證明運輸過程中的環(huán)境條件不會對醫(yī)療器械的特性和性能(包括完整性和清潔度)造成不利影響����。對于含液體的醫(yī)療器械,還需考慮低溫或凍融情況�。
運輸過程可能影響貨架有效期。如影響����,模擬運輸可與貨架有效期合并進(jìn)行。模擬運輸可在老化前或老化后進(jìn)行��。在老化前還是在老化后進(jìn)行�,取決于是模擬先運輸至醫(yī)院儲存、還是模擬在生產(chǎn)商處儲存然后運輸兩種不同的情況�����。
信息來源:無源植入性醫(yī)療器械穩(wěn)定性研究指導(dǎo)原則(2022年修訂版)