摘要
目的:了解我國兒童專用藥品(化學(xué)藥品與生物制品)中藥品說明書的標(biāo)注情況及存在問題�,為促進(jìn)兒童用藥信息的完善提供參考�。
方法:對兒童專用藥品進(jìn)行匯總�,并依據(jù)藥品說明書進(jìn)行信息表的填寫與統(tǒng)計,分析兒童專用藥品說明書存在的問題�。
結(jié)果:共收集到兒童專用藥品說明書1214份,其中國產(chǎn)藥品1180個(占97.20%)�,進(jìn)口藥品34個(占2.80%);兒童專用藥品數(shù)量最多的為呼吸系統(tǒng)用藥(占42.01%)�;兒童專用藥品口服劑型1094個(占90.11%),注射劑型57個(占4.70%)�,外用劑型59個(占4.86%),吸入劑型4個(占0.33%)�;說明書中標(biāo)注的劑量調(diào)整依據(jù)主要為年齡和體重(占45.80%),只依據(jù)年齡進(jìn)行劑量調(diào)整的占41.02%�,而7.91%的藥品未標(biāo)注劑量調(diào)整依據(jù);說明書中標(biāo)有兒童用藥最大劑量的占17.46%�,標(biāo)有兒童用藥療程的占28.01%,而標(biāo)有兒童藥代動力學(xué)的僅有16.72%�。
結(jié)論:我國兒童專用藥品說明書存在標(biāo)簽撰寫不規(guī)范、內(nèi)容不完善�、同一品規(guī)藥品說明書差異大等問題,建議相關(guān)部門加強(qiáng)藥品說明書的規(guī)范和管理�,加大上市后的監(jiān)管和數(shù)據(jù)監(jiān)查,督促藥品生產(chǎn)企業(yè)對兒童專用藥品說明書中的內(nèi)容進(jìn)行完善與改進(jìn)�,提高兒童合理用藥水平。
兒童健康是衡量一個國家衛(wèi)生保健水平的重要指標(biāo)之一�,保障兒童基本用藥需求�,促進(jìn)兒童用藥安全合理使用�,對于防治兒童疾病、提升兒童健康水平具有重要意義�。兒童在生理特點和病理特點上與成人有很大的不同,是高用藥風(fēng)險和重點監(jiān)控人群之一�。由于我國相對缺少適宜兒童的藥物,兒童專用劑型少�、規(guī)格少�、品種匱乏[1]�,人們常通過減量使用成人藥物的辦法治療兒童疾病,導(dǎo)致兒童用藥的風(fēng)險明顯增加�;而由于臨床試驗難度大、兒童用藥量少�、獲利低、劑型使用困難等諸多原因造成了企業(yè)研發(fā)動力不足�,使得兒童用藥經(jīng)常面臨無藥可用或者超說明書用藥的情況[2-4]。本研究以我國兒童專用化學(xué)藥品與生物制品作為研究對象�,通過梳理現(xiàn)有已批準(zhǔn)上市的兒童專用藥品目錄,收集整理說明書并對其中的兒童用藥信息進(jìn)行調(diào)查分析�,了解兒童專用藥品中藥品說明書的標(biāo)注情況,分析我國兒童專用藥品及說明書存在的問題并提出建議�,為進(jìn)一步規(guī)范兒童專用藥品說明書的內(nèi)容和促進(jìn)兒童用藥信息的完善提供參考�,促進(jìn)兒童合理用藥�,保障兒童用藥安全�。
一�、資料與方法
1.1 資料來源
中國兒童用藥數(shù)據(jù)庫是由中國醫(yī)藥工業(yè)信息中心推出�,我國首個針對兒童用藥的數(shù)據(jù)庫�,覆蓋政策�、研發(fā)�、上市�、臨床用藥�,可查詢國內(nèi)所有兒童用藥的上市信息�,為解決兒童藥臨床需求、提高用藥可及性助力�。通過中國兒童用藥數(shù)據(jù)庫對分類為兒童專用藥的品種進(jìn)行篩選�,導(dǎo)出兒童專用藥品(化學(xué)藥品與生物制品)�,與國家藥品監(jiān)督管理局相關(guān)藥品進(jìn)行信息核對�,參考美康合理用藥支持系統(tǒng)�、丁香園用藥助手及藥智數(shù)據(jù)等最新說明書信息�,生成兒童專用藥品目錄�。
1.2 收集方法
1.2.1
參考《中國國家處方集(第2版)》《英國國家處方集(兒童版)》(2016-2017版)對兒童專用藥品進(jìn)行分類�,并依據(jù)最新藥品說明書進(jìn)行信息表的填寫與統(tǒng)計�,分析兒童專用藥品說明書存在的問題�。
1.2.2
依據(jù)所收集藥品說明書中對于劑型的表述�,將所有藥品分為口服劑型�、注射劑型、吸入劑型和外用劑型4大類,分別進(jìn)行統(tǒng)計�。其中口服劑型表述包括片劑�、丸劑�、膠囊劑、口服散劑�、咀嚼片、顆粒劑�、混懸滴劑、口服混懸劑�、分散片、口服乳劑�、滴劑、干混懸劑�、口服凝膠劑、口服溶液劑�、泡騰顆粒劑�、糖漿劑�、口服錠劑、口腔崩解片�、口腔膜劑;注射劑型表述包含注射劑�、注射液、凍干粉針劑�、粉針劑、注射用混懸液�、注射用無菌粉末、注射用乳劑�;吸入劑型表述包含吸入用混懸液、噴鼻劑�;外用劑型表述包含栓劑、灌腸劑�、滴眼劑�、滴鼻劑�、外用散劑。
1.3 相關(guān)術(shù)語介紹
1.3.1
兒童:系指18歲以下的任何人�,除非對其適用之法律規(guī)定成年年齡低于18歲。
1.3.2
兒童專用藥:藥品說明書里僅有兒童使用說明�,無成人用藥說明,有明確的兒童適應(yīng)證和兒童用法用量�,以及兒童用藥相關(guān)的安全性信息。
二�、結(jié)果
共收集到兒童專用藥品說明書1214份,其中國產(chǎn)藥品1180個�,占97.20%,進(jìn)口藥品34個�,占2.80%。對藥品屬性及說明書內(nèi)容進(jìn)行匯總分析�。
2.1 兒童專用藥品藥理屬性分布
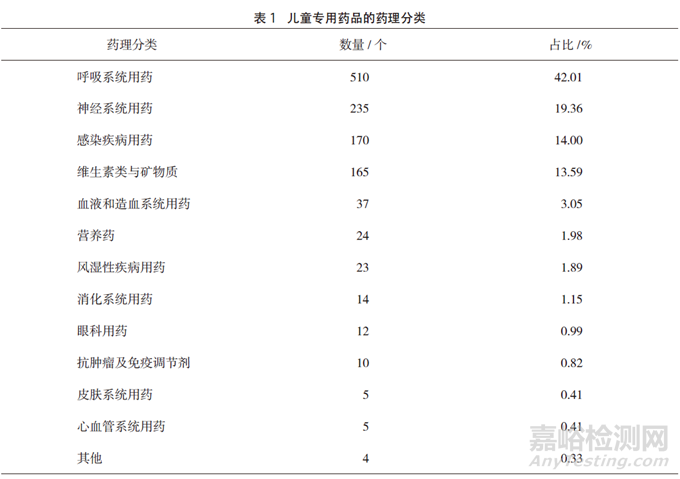
依據(jù)藥理作用分為13類常見疾病用藥,其中數(shù)量最多的為呼吸系統(tǒng)用藥�,占42.01%,主要包括咳嗽及感冒類藥品�;其次為神經(jīng)系統(tǒng)用藥、感染疾病用藥�、維生素類與礦物質(zhì),具體分類見表1�。
2.2 兒童專用藥品劑型分布
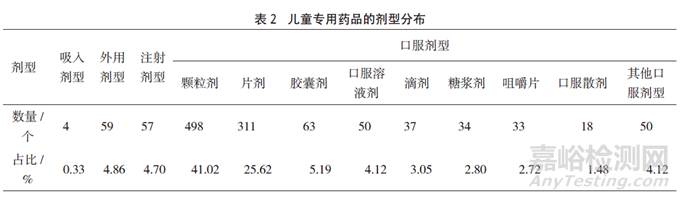
對兒童專用藥品劑型進(jìn)行分類匯總,吸入劑型4個(占0.33%)�,外用劑型59個(占4.86%),包括栓劑�、滴眼劑、灌腸劑等�;注射劑型57個(占4.70%)�;口服劑型1094個(占90.11%)�,主要為顆粒劑、片劑�、膠囊劑、口服溶液劑等�,具體分類見表2。
2.3 兒童專用藥品劑量調(diào)整依據(jù)
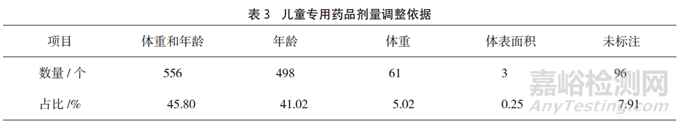
兒童專用藥品說明書劑量調(diào)整依據(jù)主要為年齡及體重�,其中以年齡和體重作為劑量調(diào)整依據(jù)的占45.80%,只依據(jù)年齡進(jìn)行劑量調(diào)整的占41.02%�,而7.91%的藥品未標(biāo)注劑量調(diào)整依據(jù)(見表3)。
2.4 兒童專用藥品說明書信息標(biāo)注情況
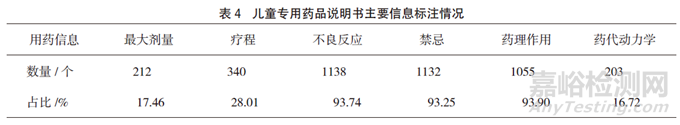
對兒童專用藥品說明書中是否標(biāo)明有兒童用藥最大劑量�、兒童用藥療程、不良反應(yīng)�、禁忌、藥理作用�、藥代動力學(xué)等6項說明書用藥相關(guān)信息進(jìn)行統(tǒng)計分析,標(biāo)有兒童用藥最大劑量的占17.46%�,標(biāo)有兒童用藥療程的占28.01%,標(biāo)有兒童藥代動力學(xué)信息的說明書僅占16.72%(見表4)�。
三、討論
通過調(diào)查發(fā)現(xiàn)�,我國兒童專用藥品以呼吸系統(tǒng)用藥為主,顆粒劑�、片劑等口服制劑為藥品主要的劑型。依據(jù)體表面積調(diào)整兒童用藥劑量是世界衛(wèi)生組織提倡的較為科學(xué)的方法�,但由于其計算方法復(fù)雜�,可操作性差�,目前在藥品說明書中標(biāo)注率較低,部分藥品未標(biāo)注兒童用藥劑量調(diào)整依據(jù)�,劑量調(diào)整缺乏指導(dǎo)標(biāo)準(zhǔn)�,給臨床用藥帶來不便。部分兒童專用藥品說明書存在問題需要修訂完善�,藥品說明書和標(biāo)簽撰寫不規(guī)范、不合理可能給醫(yī)護(hù)人員和患者使用帶來困擾�,甚至為臨床使用引入風(fēng)險[5-7]。通過匯總分析兒童專用藥品說明書及標(biāo)簽中藥學(xué)信息方面存在的問題�,為相關(guān)政策的制定提供支持,從而指導(dǎo)企業(yè)規(guī)范撰寫說明書及標(biāo)簽中藥學(xué)相關(guān)信息�,為患兒科學(xué)用藥提供依據(jù)。
3.1 說明書用語不規(guī)范
藥品說明書中兒科人群指代用詞不規(guī)范�。部分說明書存在標(biāo)注“小兒”等年齡段含糊不清的字句,但國內(nèi)外均沒有對“小兒”的年齡進(jìn)行定義�,另外,部分非處方藥(Over-The-Counter Drug�,OTC)使用“嬰兒”“幼兒”“小兒”等字樣進(jìn)行標(biāo)注,家長無法明確區(qū)分具體的適用年齡�,增加了兒童用藥風(fēng)險,如維B1乳酸鈣片�,“適應(yīng)證”表述為“適用于小兒佝僂病、軟骨病及發(fā)育不良”�。因此�,規(guī)范藥品說明書用語�,需要對兒童適用年齡進(jìn)行準(zhǔn)確描述,避免歧義�,有助于提高醫(yī)生及患者對藥品的認(rèn)知。
3.2 說明書項目不完整
藥品說明書中關(guān)于兒童用藥的不良反應(yīng)�、注意事項等內(nèi)容說明較少,且多是“請將藥品放于兒童不能接觸的地方”“尚不明確”“詳情請咨詢醫(yī)師或藥師”等語言表述�,如復(fù)方胃蛋白酶散,“注意事項”表述為“尚不明確”�,缺乏臨床意義,實用性較差�。
部分非處方藥說明書缺乏對輔料項的說明。如某廠家“甘草鋅膠囊”為甲類OTC藥品�,無輔料標(biāo)注,依據(jù)《藥品說明書和標(biāo)簽管理規(guī)定》�,非處方藥應(yīng)當(dāng)列出所用的全部輔料名稱。同時�,藥品處方中含有可能引起嚴(yán)重不良反應(yīng)的成分或者輔料的,應(yīng)當(dāng)予以說明�。
部分說明書缺乏核準(zhǔn)日期或修改日期。如某廠家“對乙酰氨基酚顆粒”�,無說明書核準(zhǔn)日期與修改日期標(biāo)注,依據(jù)《關(guān)于印發(fā)化學(xué)藥品和生物制品說明書規(guī)范細(xì)則的通知》�,核準(zhǔn)日期為國家藥品監(jiān)督管理局批準(zhǔn)該藥品注冊的時間。修改日期為此后歷次修改的時間。核準(zhǔn)和修改日期應(yīng)當(dāng)印制在說明書首頁左上角�。修改日期位于核準(zhǔn)日期下方,按時間順序逐行書寫�。
3.3 說明書標(biāo)注不統(tǒng)一
說明書內(nèi)容前后敘述不統(tǒng)一,例如適應(yīng)證表述的適用人群或適用年齡與用法用量項不一致�,如鹽酸托莫西汀膠囊“適應(yīng)證”適用人群表述為兒童和青少年,而“用法用量”適用人群為兒童�、青少年和成人;或存在藥品名稱包含“小兒”“兒童”等兒童專用藥品字眼�,但藥品說明書內(nèi)容為成人兒童共用藥�,如小兒硫酸慶大霉素顆粒,“用法用量”為兒童與成人共用�。
復(fù)方制劑規(guī)格表述形式不統(tǒng)一。如小兒硫酸亞鐵糖漿�,“規(guī)格”表述有“復(fù)方”“1mL:40mg”“每支裝10mL”“10mL/支”“每mL含硫酸亞鐵40mg,枸櫞酸2.1mg”等多種形式�,不便于臨床應(yīng)用,建議對該項內(nèi)容進(jìn)行規(guī)范統(tǒng)一�。
3.4 同一品規(guī)藥品的差異性
同一品規(guī)不同廠家說明書藥品性狀、適應(yīng)證�、用法用量、不良反應(yīng)�、禁忌、相互作用�、貯藏甚至OTC分類都存在差異,如美敏偽麻口服溶液,部分廠家的藥品說明書標(biāo)為兒童專用�,而另有部分廠家藥品說明書標(biāo)為成人兒童共用;15mL規(guī)格的布洛芬混懸滴劑�,有些產(chǎn)品說明書標(biāo)注為甲類OTC,而有些為非OTC用藥�。
同一成分規(guī)格的藥品說明書,藥品通用名不同�;或相同通用名的藥品,說明書成分不同�。如成分規(guī)格同為“磺胺嘧啶0.4g,甲氧芐啶50mg”的藥品名稱有“小兒雙嘧啶片”與“復(fù)方磺胺嘧啶片”2個�,而“小兒復(fù)方磺胺嘧啶散”組成成分有“磺胺甲惡唑0.1g,甲氧芐啶20mg”與“磺胺嘧啶0.15g�,磺胺脒0.1g,碳酸氫鈉0.1g”2種�。根據(jù)《中國藥品通用名稱命名原則》,藥品命名必須遵循一藥一名原則�。藥品名稱應(yīng)科學(xué)、明確�、簡短,詞干已確定的譯名應(yīng)盡量采用�,使同類藥品能體現(xiàn)系統(tǒng)性。
3.5 說明書內(nèi)容不精準(zhǔn)
我國兒童藥品說明書中主要是參照兒童年齡�、體重來確定用藥劑量,隨著生活水平的提高�,兒童的發(fā)育超過預(yù)期的情況越來越普遍,導(dǎo)致用藥劑量不夠準(zhǔn)確。按體表面積計算雖然計算方法較為復(fù)雜�,但科學(xué)性強(qiáng),而我國兒童用藥依據(jù)體表面積計算種類較少�,建議優(yōu)化兒童用藥劑量的計算方法。
藥品的用藥指導(dǎo)不詳細(xì)準(zhǔn)確�,不利于提高兒童用藥依從性。說明書中針對1歲以下兒童只說明“口服”過于籠統(tǒng)�,應(yīng)進(jìn)行更詳細(xì)的用藥指導(dǎo),如送服液體可使用乳汁�、牛奶或開水等,用藥時間建議注明“飯前15~30分鐘”“飯后半小時”等較為詳細(xì)的信息�。
四、結(jié)論
兒童是特殊用藥人群�,具有明顯區(qū)別于成人的生理病理特點�,對藥物的敏感性較強(qiáng)[8],藥品說明書中的不合理標(biāo)注在一定程度上增加了兒童臨床合理用藥的風(fēng)險[9-12]�。針對說明書中存在的問題,建議相關(guān)部門加強(qiáng)藥品說明書的規(guī)范制定和管理�,發(fā)布國內(nèi)說明書可讀性指導(dǎo)原則,以期達(dá)到內(nèi)容全面�、表達(dá)清晰、用語準(zhǔn)確�、通俗易懂;加強(qiáng)藥物臨床研究和監(jiān)測�,加大上市后的監(jiān)管和數(shù)據(jù)監(jiān)查,督促藥品生產(chǎn)企業(yè)對兒童專用藥品說明書中的內(nèi)容進(jìn)行完善與改進(jìn),保證說明書項目的完整性�、內(nèi)容的準(zhǔn)確性與規(guī)范性,以促進(jìn)兒童藥物的合理使用[13-16]�。同時通過不斷完善中國兒童專用藥品數(shù)據(jù)庫,統(tǒng)一動態(tài)管理系統(tǒng)平臺�,進(jìn)一步優(yōu)化藥品說明書的管理;以中國兒童專用藥品數(shù)據(jù)庫為基礎(chǔ)�,發(fā)揮政府及醫(yī)療機(jī)構(gòu)各自優(yōu)勢,引導(dǎo)企業(yè)修訂�,補(bǔ)充完善兒童專用藥品信息,全面掌握兒童專用藥品情況[17]�。為保障兒童基本用藥需求,促進(jìn)兒童用藥安全�、科學(xué)、合理使用�,近年來國家出臺了多項政策,對提升兒童健康水平具有重要意義�。《國家藥品安全“十二五”規(guī)劃》《關(guān)于保障兒童用藥的若干意見》《國家衛(wèi)生計生委辦公廳關(guān)于進(jìn)一步加強(qiáng)醫(yī)療機(jī)構(gòu)兒童用藥配備使用工作的通知》《首批鼓勵研發(fā)申報兒童藥品清單》《國家基本藥物目錄管理辦法(修訂草案)》等相關(guān)政策文件的出臺�,提出了鼓勵兒童適宜劑型研發(fā)、補(bǔ)充完善藥品說明書兒童用藥數(shù)據(jù)�、加快申報審批適宜兒童使用的品種、依據(jù)兒童專用適用藥分類制定兒童基本藥品目錄等�,為企業(yè)在兒童藥品的生產(chǎn)研發(fā)、醫(yī)療機(jī)構(gòu)在兒童藥品的配備使用及政府部門在兒童藥品的審批監(jiān)管等方面提供了方向�,促進(jìn)兒童用藥信息的完善[18-20]�。
參考文獻(xiàn)
[1] 陳敬�,魏國旭,柏林�,等. 我國兒童用藥立法的必要性和可行性研究[J]. 中國藥事,2020�,34(7):737-743.
[2] 吳娟,張順國�,黃詩穎,等. 兒童藥物臨床試驗的發(fā)展及現(xiàn)狀[J]. 醫(yī)藥導(dǎo)報�,2018,37(1):74-77.
[3] 吳文文�,王珊珊,李曼�,等. 兒科超說明書用藥現(xiàn)狀與對策分析[J]. 藥物流行病學(xué)雜志,2019�,28(6):418-422.
[4] 王雪韻,蘇巍巍�,丁宏�,等. 我國兒童藥品在臨床使用中存在的問題及對策分析[J]. 中國藥房,2019�,30(2):149-153.
[5] 闞淑月,于慶坤�,王慧麗,等. 藥品說明書中兒童用藥信息標(biāo)注情況與兒童用藥風(fēng)險[J]. 中國醫(yī)院藥學(xué)雜志�,2016�,36(20):1801-1804.
[6] 馬駿威�,任連杰. 藥品說明書中兒童用法用量藥學(xué)信息的撰寫與思考[J]. 中國醫(yī)藥工業(yè)雜志,2022�,53(11):1583-1587.
[7] 郭志燁,李玲玲�,褚智君,等. 某院門診兒童常用藥品說明書中兒童用藥信息標(biāo)注情況調(diào)查分析[J]. 兒科藥學(xué)雜志�,2022,28(6):33-37.
[8] 李宵�,丁琮洋,趙越�,等. 基于評價數(shù)據(jù)庫探索易致重度不良反應(yīng)藥品的兒童用藥安全性[J]. 中國現(xiàn)代應(yīng)用藥學(xué),2022�,39(12):1604-1613.
[9] 閆聰聰,王曉玲�,張勝男,等. 國內(nèi)8家兒童醫(yī)院常用藥品說明書中兒童用藥信息的調(diào)查分析[J]. 中國藥事�,2021,35(1):10-15.
[10] 劉婷�,余靜潔. 某院兒科門診超說明書用藥調(diào)查與分析[J]. 兒科藥學(xué)雜志,2022�,28(5):25-28.
[11] 方思曉,王一博. 藥品說明書在兒科臨床用藥中的應(yīng)用分析[J]. 中國藥物濫用防治雜志�,2021,27(6):944-947.
[12] 許淑紅�,張綺�,張林琦�,等. 探討我國兒科用藥的發(fā)展現(xiàn)狀及政策層面的思考[J]. 中國臨床藥理學(xué)雜志,2020�,36(12):1760-1767.
[13] 趙婷婷,趙建中�,王海學(xué). 關(guān)于規(guī)范國內(nèi)已上市藥品說明書的幾點思考[J]. 中國臨床藥理學(xué)雜志,2020�,36(14):2153-2155.
[14] 王雅君,韓容�,岳志華,等. 美國兒童藥品上市審批情況分析及其對我國兒童用藥保障工作的啟示[J]. 中國藥房�,2021,32(2):133-138.
[15] 劉涓�,任連杰.《兒童用藥(化學(xué)藥品)藥學(xué)開發(fā)指導(dǎo)原則(試行)》解讀[J]. 中國新藥雜志,2021�,30(23):2147-2152.
[16] 李豐杉,余勤. 兒童用藥研發(fā)及兒科臨床試驗的國際發(fā)展和國內(nèi)現(xiàn)狀[J]. 中國新藥雜志�,2020,29(17):1933-1938.
[17] 耿瑩�,張豪,王麗卿�,等.《化學(xué)藥品和治療用生物制品說明書中兒童用藥相關(guān)信息撰寫的技術(shù)指導(dǎo)原則(試行)》起草背景及要點內(nèi)容[J]. 中國新藥雜志�,2022,31(4):323-328.
[18] 趙巖松�,洪蘭�,葉樺. 加快我國兒童用藥研發(fā)的政策與法規(guī)分析[J]. 中國藥事�,2017,31(1):1-6.
[19] 陳慧�,蘇廣全,劉曉�,等. 中國醫(yī)療機(jī)構(gòu)藥品目錄管理評價指南[J]. 中國藥房,2022�,33(6):641-652.
[20] 袁利佳,王麗卿�,汪小燕,等. 藥品加快上市程序在兒童用藥注冊體系中的作用與思考[J]. 中國醫(yī)藥工業(yè)雜志�,2022,53(11):1529-1538