摘要:良藥苦口,但往往因為藥物苦澀而難以下咽�,使得患者用藥順應(yīng)性差,而掩味技術(shù)的運用可以較好改善這一情況����。合適有效的掩味技術(shù)能夠改善患者尤其是兒童的用藥順應(yīng)性,提高療效��,提高藥物的臨床價值����。本文對掩味技術(shù)研究最新進展進行概括��,從作用機制和應(yīng)用范圍等方面對傳統(tǒng)掩味技術(shù)進行分類匯總�,同時介紹了新型高效掩味技術(shù)����。
口服給藥是大多數(shù)藥物的首選給藥途徑,由于它用藥簡便�、成本低廉、劑量準(zhǔn)確[1]等優(yōu)點成為臨床用量較大的藥物制劑��。但是很多藥物在口服過程中或服藥后立即表現(xiàn)出苦味����,大多數(shù)患者尤其是兒童和老年人用藥順應(yīng)性差[2,3]。據(jù)調(diào)查結(jié)果顯示�,超過50%的患者沒有按照處方服藥,制藥業(yè)每年因此損失約300 億美元[4]��,而適口性差和藥物苦味是其主要原因����。因為苦味會導(dǎo)致患者產(chǎn)生服藥抵抗,導(dǎo)致治療的中斷����,從而失去藥物的最佳療效[5]����。
因此�,掩味技術(shù)已成為處方開發(fā)的重要組成部分����,在產(chǎn)品開發(fā)階段采用掩味技術(shù),可以促進公司在短時間內(nèi)推銷藥物��,并確?;颊叻幏e極性。本文通過對掩味原理進行剖析��,基于苦味產(chǎn)生機制總結(jié)藥物掩味技術(shù)����,并對不同掩味技術(shù)的應(yīng)用情況進行了簡要介紹。
1����、掩味技術(shù)
1.1 苦味產(chǎn)生機制
味覺的形成主要基于味蕾,味蕾是一種上皮分化的特殊器官����,在舌頭表面和邊緣大量分布�,在口腔和咽部黏膜表面部分分散����。它由味覺細(xì)胞組成,能夠表達(dá)苦味受體(type 2 bitter taste receptor, TAS2Rs)��,從而對各種味道進行識別[6]�。當(dāng)苦味物質(zhì)進入口腔經(jīng)過舌表面時,可溶性物質(zhì)與味蕾直接接觸��,激活TAS2Rs�,引起味覺細(xì)胞周圍環(huán)繞的感覺神經(jīng)末梢興奮,形成神經(jīng)沖動��,最終將神經(jīng)沖動傳入味覺中樞并經(jīng)神經(jīng)中樞整合�,產(chǎn)生苦味感知[7]。
1.2 藥物掩味技術(shù)
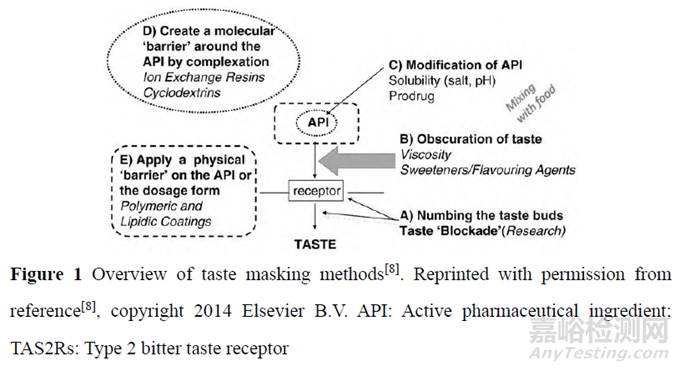
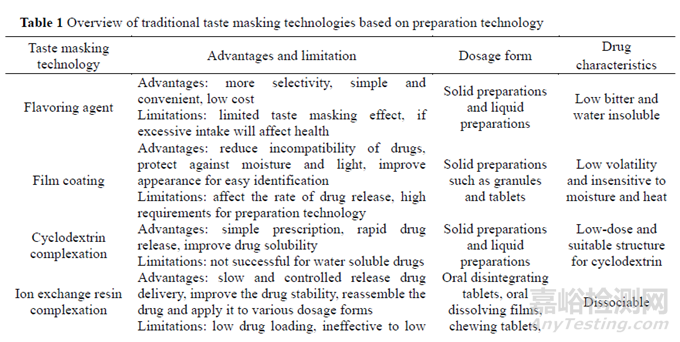
掩味技術(shù)的重點在于利用各種方法干預(yù)味覺形成的各個環(huán)節(jié)����。針對味覺產(chǎn)生的過程,藥物掩味技術(shù)如圖1[8]所示��。從活性藥物成分(active pharmaceutical ingredient, API)角度來說�,首先可以對API 進行修飾��,例如成鹽��、改變晶型或制成前藥�,從而減少藥物的溶解��。其次是在API 周圍建立分子屏障����,例如將離子交換樹脂或環(huán)糊精類物質(zhì)與 API 絡(luò)合��,阻止API 釋放后與味蕾接觸����,達(dá)到掩味目的。從味覺產(chǎn)生過程來說�,可以通過加入甜味劑、芳香劑等矯味劑降低感知到的API 苦味進行掩味�。從神經(jīng)沖動傳導(dǎo)的過程來說,可以通過麻痹味蕾和味覺阻斷進行掩味�。苦味阻滯劑主要包括苦味受體拮抗劑和苦味信號傳導(dǎo)抑制劑�。最后,從制劑的角度出發(fā)�,可以通過聚合物包衣��、微囊和脂質(zhì)包衣形成制劑或API 的物理屏障��,阻止API 釋放從而掩味[9,10]�。表1 從適用藥物及劑型以及各項掩味技術(shù)的優(yōu)缺點等方面總結(jié)了上述基于制劑工藝的掩技術(shù)概況����。
2、基于API 修飾的掩味技術(shù)
2.1 改變藥物溶解度
藥物苦味的產(chǎn)生主要源于藥物在口腔的唾液中溶解并且與味蕾上的 TAS2Rs相互作用��。因此��,藥物的掩味可以從降低API 的溶解度出發(fā)����,減少API 和TAS2Rs的結(jié)合概率,達(dá)到掩味效果��。例如����,將藥物制成口腔中不溶解的制劑如懸浮劑;改變成鹽��、改變晶型的方法使得API 保持不溶解的狀態(tài)����;使用在唾液中溶解度較低的前藥��,減少API 溶解�。
布洛芬[11]�、利福平[12]和丁螺環(huán)酮[13]存在著多種晶型,對應(yīng)有著不同的溶解度�。在紅霉素、麥迪霉素和麥白霉素等大環(huán)內(nèi)酯類藥物中加入鞣酸作為掩蔽劑����,可以與藥物迅速形成難溶性鞣酸鹽,對大環(huán)內(nèi)酯類抗生素的苦味有著較好的掩味效果[14]�。長春胺和曲馬多可以與糖精鈉�、糖精鉀形成糖精鹽,降低藥物的苦味�。當(dāng)需要使用該方法降低兒童制劑中藥物的溶解度時,需要考慮所加入成鹽劑對于兒童群體的安全性以及不同晶型藥物的生物利用度��。
如果藥物擁有 pH 依賴性的溶解度��,可以通過加入pH 調(diào)節(jié)劑使得藥物保持不電離的狀態(tài)����,從而限制藥物在制劑載體中的溶解度����,減少溶解度��,掩蔽藥物苦味�。在鹽酸丙哌維林混懸劑中加入碳酸氫鉀可以使其脫鹽成為游離丙哌維林,減少溶解從而使機體感受到藥物的苦味變少�。在阿奇霉素干混懸劑中加入pH 調(diào)節(jié)劑無水磷酸三鈉也能夠降低阿奇霉素的溶解度和苦味?�?紤]到兒童對于藥用輔料的耐受性與成人存在差異��,在調(diào)節(jié)pH 時應(yīng)當(dāng)使用合適的輔料�,并調(diào)節(jié)適當(dāng)濃度。
2.2 前藥
前藥設(shè)計是掩蓋不良味道藥物特性目的的方法之一����,如水或脂質(zhì)膜中的低溶解性、低靶向性����、化學(xué)不穩(wěn)定性、不良味道��、局部給藥后的刺激或疼痛、毒性��。對乙酰氨基酚是一種止痛藥�,其苦味產(chǎn)生是由于其結(jié)構(gòu)上的羥基與苦味受體相互作用。Hejaz 等[15]通過計算機輔助設(shè)計了三種對乙酰氨基酚前藥����,經(jīng)預(yù)測新添加的連接劑可以阻斷羥基與苦味受體的作用會起到掩味的作用。Chatale 等[16]通過合成前藥美洛昔康特戊酸酯來實現(xiàn)苦味官能團的化學(xué)修飾����。依據(jù)大鼠的單瓶實驗評估了口感改善情況。結(jié)果表明�,與美洛昔康相比,美洛昔康特戊酸酯的適口性顯著提高�。
3、添加矯味劑
矯味劑系指藥物中用以改善或屏蔽藥物不良?xì)馕逗臀兜赖妮o料����,在難以入口的活性藥物成分中加入矯味劑是最簡易常用����、最優(yōu)先考慮的掩味技術(shù),一般包括甜味劑��、芳香劑、增稠劑和味蕾麻痹劑四類�。矯味劑實現(xiàn)掩味的策略是進行神經(jīng)中樞味覺信號整合的干擾,不同甜味劑在感官上的甜度強度分布時間不同����。以生物堿、苷類����、抗生素、抗組胺類藥物苦味較大�,較多使用甜味劑和芳香劑來掩蓋。Zhao 等[17]以安賽蜜和糖精兩種矯味劑成鹽����,能有效掩蓋川芎嗪的苦味,解決了活性藥物成分味苦和生物利用度低所帶來的挑戰(zhàn)�。Ogbonna 等[18]為了開發(fā)適口的兒童口服液,利用糖精鈉和阿斯巴甜兩種甜味劑進行矯味��,相較于原始的糖漿劑��,對苦味掩蓋效果更好����,穩(wěn)定性更高��。與原始處方中利用45%蔗糖掩味不同�,Zhu等[19]采用三氯蔗糖和桔子香精兩種矯味劑�,顯著提高了板藍(lán)根口服液的用藥順應(yīng)性。
簡單的加入矯味劑/甜味劑掩味作用有限�,不足以掩蓋部分藥物的其他不良味道,過度使用甜味劑對健康的不利影響也日益增加�。為此,聯(lián)合國糧食及農(nóng)業(yè)組織與世界衛(wèi)生組織食物添加劑聯(lián)合專家委員會(JECFA)共同建立了添加劑成分每日最大攝入量的規(guī)定����,此外美國FDA“批準(zhǔn)藥品的非活性成分列表”可供生產(chǎn)者查詢某一輔料在不同給藥途徑下的最大添加比例,這些規(guī)定可以為矯味劑的用量選擇提供一定的理論支撐����。同時,矯味劑的選取也依賴于適應(yīng)癥����,對于治療某些特殊疾病的制劑,如治療糖尿病的制劑矯味時不能使用蔗糖����,可由木糖醇����、山梨醇�、麥芽糖醇��、甜菊糖苷等甜味劑�,如健胃藥中不得添加矯味劑等。
4����、基于劑型加工的掩味技術(shù)
4.1 包衣
包衣是最簡單直接且常用的掩味技術(shù),依賴物理掩味原理����,減少口腔對苦味的感知。聚合物包衣材料在唾液pH(6.97~7.40)下可形成不溶性屏障��,穩(wěn)定性高����,具有較低的劑量傾瀉風(fēng)險。對于兒童藥物����,安全性為首要考量[20]。美國FDA“非活性物質(zhì)數(shù)據(jù)庫(inactive ingredient database)”指出��,纖維素類聚合物如乙基纖維素、羥丙甲纖維素以及不同類型��、等級的甲基丙烯酸共聚物的口服毒性低[21]�,常被用于包衣掩味。
鹽酸普萘洛爾具有苦咸味�,兒童用藥順應(yīng)性較差,Sun 等[22]用Eudragit E100對復(fù)方穿心蓮顆粒進行包衣��,制備的掩味混懸顆粒在水中分散均勻��,口感良好�,適合兒童患者服用。兒童用藥中��,抗生素是一類重要的使用頻率極高的藥物����,其中羅紅霉素應(yīng)用較為普遍。Cao[23]研制的羅紅霉素口腔崩解片��,通過包衣技術(shù)����,不僅掩蓋了羅紅霉素的苦味,藥物的溶出率也并未發(fā)生影響�。Nishiyama 等[24]利用乙基纖維素和羥丙甲纖維素制備拉呋替丁的掩味層包衣顆粒����,隨著羥丙甲纖維素含量的增加����,掩味顆粒溶出延遲時間縮短����,在模擬口腔pH 環(huán)境中,藥物并無釋放�,證明其具有良好的掩味性能。
通過包衣材料進行掩味��,是目前直接且有效的掩味方式�,如何選擇合適的材料進行包衣,實現(xiàn)口腔中的掩味�,并能在胃里進行速釋,是當(dāng)前研究的重點�。很多研究結(jié)果如膜控包衣已證明聚合物材料包衣掩味的可行性[25]。
4.2 熱熔擠出技術(shù)
近年來��,熱熔融出(hot-melt extrusion , HME)技術(shù)已被用來制備多種藥物劑型和藥物釋放系統(tǒng)�。HME 技術(shù)通過在熔體擠出機中混合和熔化藥物、聚合物以及其他輔料��,然后用一個或多個旋轉(zhuǎn)螺桿迫使其通過模具以獲得所需產(chǎn)品。HME 技術(shù)應(yīng)用于藥物的掩味用途是很有利的��,與其他可用常規(guī)技術(shù)相比����,HME技術(shù)是一個連續(xù)的操作流程,不耗時��,易于放大�,而且API 在主流擠壓工藝中的暴露時間相當(dāng)短,適用于對濕度敏感的API����,可以提高API 穩(wěn)定性[26]。Kanikanti等[27]研制了用于恩諾沙星��、普多沙星�、馬博沙星等苦味藥物的膨化制品,其直徑≤0.5 mm�,其目的是減少苦味API 在口腔中釋放。擠壓過程是使用雙螺桿擠出機在室溫下進行的�,這不會導(dǎo)致熱成型材料完全熔化。溫和造粒后的擠出物被加工成合適的藥物形式��,如片劑、糊劑����、混懸劑或膠囊。
4.3 蒸汽制粒技術(shù)
濕法制粒技術(shù)是將藥物粉末與黏合劑混合�,靠黏合劑的橋架或黏結(jié)作用使粉末聚結(jié)在一起而制備顆粒的方法。其中黏合劑為濕法制粒技術(shù)的關(guān)鍵影響因素之一��,不同黏合劑制備的顆粒表面粗糙度�、孔隙率以及體外溶出效果均有所不同�。而蒸汽制粒技術(shù)是一種新型濕法制粒技術(shù),以水蒸氣作為黏合劑�。蒸汽冷凝后,在藥物粉末顆粒上形成熱薄膜�,將苦味 API 包封其中,減少苦味API 與味蕾的接觸��,達(dá)到掩味的目的[28]����。Albertini 等[29]評估了三種不同的黏合劑(水、聚維酮�、水蒸氣)的制備對乙酰氨基酚顆粒的掩味效果。體外溶出研究表明�,與水和聚維酮相比,采用水蒸氣制備的顆粒體外釋藥速度更緩慢�。此外�,6 名志愿者的味覺測試也證實了蒸汽制粒具有顯著的掩味效果�。
4.4 微囊與微球
微囊是一種具有聚合物材料外殼的微型包裹體:聚合物材料作為囊材將液體或固體藥物包裹形成微小膠囊。因為只有藥物溶解才能產(chǎn)生味覺����,故利用聚合物材料對苦味API 進行包裹,可以降低其在唾液中的溶解度��,從而掩蓋味道[30]�,原理與藥物包衣相似。微球則是藥物溶解或分散在聚合物材料中����,形成微小球狀實體,通過減緩藥物的釋放達(dá)到掩味效果�。常用制備方法包括噴霧干燥法、噴霧凝結(jié)法��、流化床法�、液中干燥法等。常用的聚合物材料包括聚丙烯酸樹脂類合成高分子材料��;纖維素衍生物等半合成高分子材料�;明膠、海藻酸鹽、殼聚糖等天然高分子材料[31]�。Bao 等[32]以聚丙烯酸樹脂IV 為囊材,采用液中干燥法制備氧氟沙星掩味微囊��。體外試驗顯示����,該微囊在模擬口腔環(huán)境(pH 值為7.0)介質(zhì)中釋放極其緩慢既可掩味又能實現(xiàn)持續(xù)釋藥。
阿奇霉素(azithromycin, AZM)為第二代大環(huán)內(nèi)酯類抗生素�,常用于治療各種病原體引起的兒童及成人呼吸道感染,并被多個國家作為肺炎支原體感染的首選藥物��。然而����,AZM 苦味突出��,患者用藥順應(yīng)性差��,且口服給藥容易出現(xiàn)腹痛����、惡心、嘔吐等胃腸道反應(yīng)��,導(dǎo)致用藥效果不佳。Zhao 等[33]采用乳化交聯(lián)法制備阿奇霉素羧甲基殼聚糖微球�,考察了其體外釋藥性能和掩味能力,實驗結(jié)果表明制得的微球載藥量和包封率較高��,藥物體外釋放穩(wěn)定�,掩味效果較好。
4.5 納米技術(shù)
4.5.1 脂質(zhì)納米粒
采用脂質(zhì)材料包裹在藥物周圍制成固體脂質(zhì)微粒�,可建立掩味的物理屏障。與聚合物包衣相比����,脂質(zhì)屏障的優(yōu)勢在于其制備過程無需溶劑蒸發(fā),只需將脂質(zhì)熔融包裹藥物�,且該過程無水的參與,可應(yīng)用于水敏感的藥物��,也降低了微生物污染的風(fēng)險[28]�。二甲雙胍的金屬味可以通過制備脂質(zhì)小丸進行掩蓋[10]。但是需要注意的是��,疏水材料的脂質(zhì)材料會對藥物的溶出造成一定的影響�,使用該方法掩味時要提前對生物利用度進行綜合評估。
4.5.2 納米復(fù)合物
納米復(fù)合物是由有機聚合物和無機材料組成的納米雜化材料�。二氧化硅、膨潤土��、氧化鋁、氧化鋯等無機材料可與有機聚合物納米雜化��。納米雜化形成的基本機制是無機成分和有機成分之間形成氫鍵或強離子鍵[34]����。由無機黏土材料膨潤土組成的納米復(fù)合物被制備出來用于西地那非(sildenafil, SDN)的味道掩蓋[35]。膨潤土的主要成分是蒙脫石(montmorillonite,MMT)����,表面顯負(fù)電荷,陽離子物質(zhì)穿插在層內(nèi)用于平衡過多的負(fù)電荷��。膨潤土的這一特性使得陽離子藥物SDN 以強離子鍵合的方式包裹在蒙脫土的層狀空間中�,從而制備出SDN-MMT 納米復(fù)合物。用堿性聚合物聚乙烯縮醛二乙氨基乙酸酯(polyvinylacetal diethylaminoacetate , AEA)包覆SDN-MMT��,以提高藥物的釋放速率�。AEA 包被的SDN-MMT 納米復(fù)合物延緩藥物在口腔中的釋放��,且具有掩味作用[36]�。Oh 等[37]通過將阿立哌唑(aripiprazole, APZ)與MMT 雜化,制備了APZ-MMT 納米復(fù)合物��,通過AEA 對其進行包裹掩蓋了阿立哌唑的不良味道����,提高了藥物溶解性��,促進藥物釋放��。
4.6 3D 打印技術(shù)
目前�,用于掩味的輔料選擇存在局限性�,供兒童配方的輔料選擇更為狹窄,采用常規(guī)的掩味輔料和劑型很難滿足兒童患者的臨床需求�。近年來,用于味覺掩蔽制劑的新型藥物加工技術(shù)如雨后春筍般興起����,如3D 打印技術(shù)可以根據(jù)患者的口味特征和個人喜好進行定制,正因如此����,我們也需要設(shè)計更好的輔料來跟進這些現(xiàn)代工藝。
Scoutaris 等[38]已經(jīng)對3D 打印在兒科制劑中的使用進行研究��,用吲哚美辛�、醋酸羥丙甲纖維素琥珀酸酯和聚乙二醇的混合物熱熔擠出細(xì)絲,增材制造成Starmix® “糖果狀”����,體內(nèi)味覺掩蔽評價顯示��,其對藥物苦味掩蔽性極佳����,更受兒童歡迎��。Boniatti 的團隊[39]將Kollidon VA 64 和表面活性劑混合����,直接粉末擠出,制備吡喹酮的無定形固體分散體3D 打印片劑����,體外適口性實驗表明,該技術(shù)掩味性能良好�,無需額外添加掩味賦形劑。苯海拉明味苦��,普通掩蔽技術(shù)效果不佳��,Tabriz 等[40]將苯海拉明�、甜味劑三氯蔗糖和草莓香精混合��,擠出長絲����,通過熔融沉積技術(shù)制備3D 打印水果味咀嚼片����,甜味劑和草莓香精的協(xié)同作用完全掩蓋原料藥苦味并實現(xiàn)速釋����。
5、總結(jié)
藥物的不良味道普遍存在��,涉及抗菌藥����、心血管藥、抗腫瘤藥����、解熱鎮(zhèn)痛藥、神經(jīng)系統(tǒng)藥物等多個用藥領(lǐng)域��,嚴(yán)重影響著兒童����、老年患者以及其他特殊用藥人群如吞咽困難者、精神病患者等的用藥順應(yīng)性����,進而影響到藥物療效�。尤其是兒童用藥時����,相比于成人,兒童對藥物的不良味道更加敏感和抗拒�,因此,如何掩蓋藥物的不良味道是兒童制劑開發(fā)和研究的重心�。掩味技術(shù)在提高患者的用藥順應(yīng)性方面起著非常重要的作用。隨著掩味技術(shù)的不斷發(fā)展�,越來越多的新型掩味技術(shù)與思路應(yīng)用到了藥物苦味掩蔽的過程中,這與輔料行業(yè)的進步也息息相關(guān)��,輔料在藥物制劑中雖作為惰性成分不具有直接治療作用��,但可以輔助制劑工藝�,保障或提高藥物的安全性和患者用藥順應(yīng)性,方便藥品的識別����。但輔料特性與工藝特點會對掩味作用的發(fā)揮產(chǎn)生影響,因此需科學(xué)合理地與特定輔料及工藝有機結(jié)合起來����。本文論述了基于制劑工藝的幾種傳統(tǒng)掩味技術(shù)以及基于新型材料的創(chuàng)新掩味技術(shù)和應(yīng)用實例,相信隨著新技術(shù)和新劑型地不斷深入研究����,越來越多的新型的掩味技術(shù)將會應(yīng)用到口服制劑尤其是兒童制劑的研發(fā)和生產(chǎn)中。