導 語
近日�����,天津大學系統(tǒng)生物工程教育部重點實驗室進行的一項研究:基于功能化聚苯胺的時序黏附水凝膠貼片(chronological adhesive hydrogel patch,CAHP)�����,實現(xiàn)了與濕潤動態(tài)心外膜表面的嵌入結(jié)合���,這種結(jié)合具備時序性與保形性���。該研究成果發(fā)表在期刊《Nature Communications》上��。
1��、研究背景
心肌梗死是一種由缺血性動脈閉塞引起的惡性疾病��,具有發(fā)病急���、并發(fā)癥復雜��、致死率高等特點���,需要早期發(fā)現(xiàn)和治療���。已有心外膜貼片能夠?qū)崿F(xiàn)同步電記錄和刺激�����,然而無法克服體內(nèi)電生理檢測容易受到電磁干擾導致信號偽影的缺點�����,從而對心臟功能產(chǎn)生誤判��,且生物電子設(shè)備缺乏對缺血和纖維化病變進行深度修復的功能��。導電聚合物基水凝膠可以響應(yīng)性感知機械變形,同時補償纖維組織的電傳導以進行電耦聯(lián)治療���。但是傳統(tǒng)導電聚合物在疏水處理�����、酸摻雜環(huán)境和侵入性植入等方面的表現(xiàn)不理想�����。
2���、研究概述
基于功能化導電聚合物的設(shè)計,研究團隊設(shè)計了功能化聚苯胺基時序黏附水凝膠貼片��。它可以實現(xiàn)心臟的同步機械生理監(jiān)測和電耦合治療�����,并牢固附著在心臟表面監(jiān)測心臟的機械運動和電活動��。
基于功能化導電聚合物的設(shè)計�����,研究團隊設(shè)計了功能化聚苯胺基時序黏附水凝膠貼片。它可以實現(xiàn)心臟的同步機械生理監(jiān)測和電耦合治療�����,并牢固附著在心臟表面監(jiān)測心臟的機械運動和電活動�����。
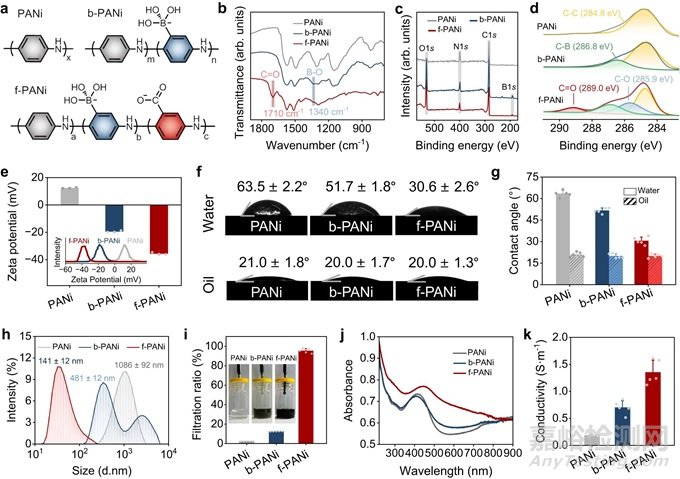
關(guān)鍵創(chuàng)新在于通過側(cè)鏈修飾策略合成了功能化聚苯胺(functionalized polyaniline, f-PANi),從而增強了其在生理介質(zhì)中的電活性和親水性�����。這一進展顯著提高了導電聚合物在生物醫(yī)學應(yīng)用中的潛力�����。f-PANi包含硼酸酯和羧基側(cè)鏈�����,能夠自發(fā)生成動態(tài)共價硼酸酯鍵和非共價氫鍵并與聚乙烯醇(polyvinyl alcohol, PVA)結(jié)合���。這一獨特性使得CAHP能夠在生理環(huán)境中原位形成,無需額外刺激。
圖1:f-PANi的結(jié)構(gòu)與性能(圖片來自原文)
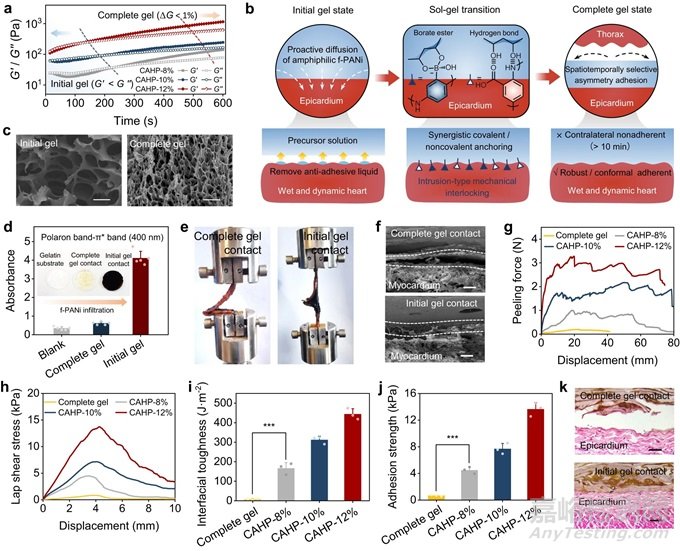
當CAHP的前體溶液涂布在心肌表面時���,兩親性的f-PANi能夠迅速吸附和去除抗粘附的心包液��,從而滲透心外膜���。CAHP利用協(xié)同的化學和物理交聯(lián)機制���,增強了內(nèi)部內(nèi)聚力和界面鎖定力,使貼片牢固地錨定在心肌上���。基于主動擴散�����、界面交聯(lián)和機械鎖定的程序化粘附機制��,使得CAHP能夠在初始凝膠狀態(tài)下逐漸形成與心外膜之間的強大橋接網(wǎng)絡(luò)��。重要的是��,一旦凝膠化過程完成,CAHP表現(xiàn)出對非靶組織的抗粘附性�����。
圖2:CAHP的時序黏附性能及機理(圖片來自原文)
CAHP還展示了通過增加心肌細胞鈣瞬變速度來改善心肌梗死引起的心室電生理功能障礙的潛力��。這是通過補償纖維組織中的電傳導來實現(xiàn)的�����。
該文獻還介紹了此種水凝膠的制備方法與材料以及各特性參數(shù)的測量方法���。
3、研究意義
這種按時間順序的粘附方法具有廣泛的適用性��,可用于探索各種材料和醫(yī)療應(yīng)用��。基于導電聚合物的CAHP能夠同時進行機械生理監(jiān)測和電偶聯(lián)治療�����,為診斷和治療心肌梗死提供了一種一體化方法�����。這種面向醫(yī)療的CAHP可以繼續(xù)為其他可穿戴和植入式電子設(shè)備提供健康管理��,有潛力修復其他電活性組織���,如骨骼肌和神經(jīng)���。未來���,無線、自供電和多模式集成將進一步促進基于水凝膠的生物電診斷和治療系統(tǒng)的臨床轉(zhuǎn)化�����。
參考文獻:Yu, C., Shi, M., He, S. et al. Chronological adhesive cardiac patch for synchronous mechanophysiological monitoring and electrocoupling therapy. Nat Commun 14, 6226 (2023). https://doi.org/10.1038/s41467-023-42008-9