當(dāng)一個(gè)藥物分子不能與其鏡像重合時(shí),該藥物就稱為手性藥物�。這里我們所說的手性藥物主要是指以單一的立體異構(gòu)體開發(fā)的藥物�����,不包括外消旋體藥物 ����。由于手性藥物與其對(duì)映異構(gòu)體在非手性環(huán)境下的理化性質(zhì)均相同,所以在研究手性藥物時(shí)�����,應(yīng)注意從立體化學(xué)的角度考慮問題。本期我們接著化合物結(jié)構(gòu)研究系列來說下仿制藥中手性藥物的研究內(nèi)容和注意事項(xiàng)��。
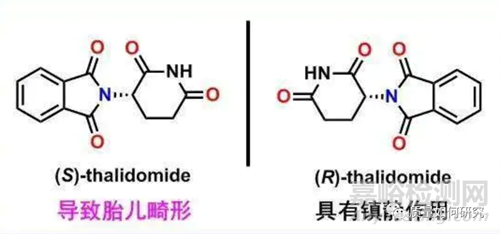
舉一個(gè)經(jīng)常被大家引用的例子來說�����,沙利度胺(Thalidomide)由于其手性異構(gòu)體沒有經(jīng)過嚴(yán)格的安全性評(píng)價(jià)����,從而使得它從“天使”變?yōu)榱?ldquo;魔鬼”,造成了迄今為止最大的藥物安全事件���。當(dāng)然,后面通過老藥新用和二次開發(fā)�,又讓它重新獲得FDA的批準(zhǔn)用于治療麻風(fēng)病人和骨髓瘤的治療。
對(duì)于仿制藥中手性藥物的研究����,我們主要從以下五個(gè)方面來分析,具體如下:
1�、制備工藝
對(duì)于研發(fā)單位來說,藥物的制備工藝是整個(gè)藥物研究的基礎(chǔ) �。若工藝不穩(wěn)定、 不可控,則藥品質(zhì)量的穩(wěn)定�����、可控就成了無源之水����。因此,在手性藥物的制備工藝中應(yīng)注意以下問題 :
所用的合成路線應(yīng)有依據(jù) (文獻(xiàn)或理論 )����, 注意反應(yīng)條件及關(guān)鍵中間體的分離與純化方法的選擇,以及合成工藝中消旋化的可能性���。
需采用具有立體選擇性的方法控制手性原料�����、手性試劑及引入手性中心后的重要中間體的光學(xué)純度���,并提供詳細(xì)檢測方法及圖譜。
對(duì)于含兩個(gè)以上手性中心的藥物��,因最終產(chǎn)品中可能存在的光學(xué)異構(gòu)體雜質(zhì)數(shù)目多����,質(zhì)控難度大���,此時(shí)對(duì)最終產(chǎn)品光學(xué)純度控制可采用加強(qiáng)合成過程中工藝條件的控制,對(duì)各手性中間體及原料的光學(xué)純度嚴(yán)格控制來實(shí)現(xiàn)�。
2、結(jié)構(gòu)確證
結(jié)構(gòu)確證的作用在于回答“產(chǎn)品對(duì)不對(duì)的問題”����。所有的質(zhì)量研究都是基于對(duì)的化合物結(jié)構(gòu)基礎(chǔ)之上的。因此對(duì)手性藥物的特殊要求主要有以下幾點(diǎn) :
應(yīng)確證產(chǎn)品的立體構(gòu)型���??筛鶕?jù)手性中心的多少���、文獻(xiàn)數(shù)據(jù)是否充足、對(duì)照品的有無來選擇合適的確證方法��,必要時(shí)可采用單晶X-射線衍射進(jìn)行確證����。
比旋度通常是必需的檢測項(xiàng)目之一。
已知的起始原料的構(gòu)型和化學(xué)合成方法的立體選擇性也可作為依據(jù)之一��。
3、質(zhì)量研究
由于非對(duì)映異構(gòu)體與普通的非光學(xué)雜質(zhì)一樣�, 可以通過非手性的分析方法進(jìn)行分離控制 ,所以�,手性藥物的質(zhì)量研究應(yīng)重點(diǎn)考察對(duì)映異構(gòu)體的分析方法是否合理即可 。但需注意的地方是:
單用比旋度控制手性藥物的光學(xué)純度不夠完善�,尤其是在藥物本身比旋度數(shù)值小以及有多個(gè)手性中心存在的情況下,用比旋度控制藥物光學(xué)純度是有很大誤差的�。因此,還應(yīng)采用手性色譜法 (手性HPLC及毛細(xì)管電泳等)或手性衍生法進(jìn)行控制�����,并且所用方法應(yīng)提供詳細(xì)方法學(xué)研究資料�,尤其要注意分離度是否符合要求 (建議提供相應(yīng)的消旋化合物的分離圖譜作為佐證)。
對(duì)于含有多個(gè)手性中心的化合物����,由于其非對(duì)映異構(gòu)體可通過普通色譜方法進(jìn)行定性或定量測定,故可作為一般雜質(zhì)處理���,以簡化研究工作��。
4����、質(zhì)量標(biāo)準(zhǔn)
對(duì)于原料藥來說,比旋度作為藥典收載的常規(guī)理化常數(shù)�����,具有儀器簡單���、數(shù)據(jù)直觀的點(diǎn)�,在一定程度上能反映產(chǎn)品的純度���。因此�,該項(xiàng)目一般都應(yīng)列人原料藥質(zhì)量標(biāo)準(zhǔn)之中��。但須注意其范圍不應(yīng)過大�����,否則起不到控制產(chǎn)品光學(xué)純度的目的�����。采用立體專屬性的含量測定或有關(guān)物質(zhì)檢查方法���,能更加精確地控制手性藥物的純度����。因此���,為嚴(yán)格控制產(chǎn)品質(zhì)量����,一般應(yīng)將兩者結(jié)合起來���。即
首先����,應(yīng)制定合理的比旋度范圍��。
其次�����,如含量測定采用非立體專屬性方法��,應(yīng)在 “有關(guān)物質(zhì)”項(xiàng)中增加對(duì)映異構(gòu)體的檢查�,限度應(yīng)根據(jù)實(shí)測情況及穩(wěn)定性考察的結(jié)果確定。
另外�����,對(duì)于含有多個(gè)手性中心的藥物 ,如果根據(jù)所用的合成路線及質(zhì)量研究的結(jié)果�,對(duì)映異構(gòu)體不可能存在,則可不定入對(duì)映異構(gòu)體檢查項(xiàng)���,但應(yīng)對(duì)其他可能產(chǎn)生的非對(duì)映異構(gòu)體進(jìn)行控制���。
而對(duì)于制劑來說,手性藥物制劑的標(biāo)準(zhǔn)中是否定入立體專屬性的鑒別項(xiàng)或?qū)τ钞悩?gòu)體的檢查項(xiàng)應(yīng)從兩個(gè)方面來考慮:一是該手性藥物在制劑的制備及放置過程中有無外消旋化���,二是該手性藥物是否同時(shí)也有其外消旋體或?qū)τ钞悩?gòu)體上市銷售�。
如果該手性藥物在制劑的制備及放置過程中有外消旋化發(fā)生�����,則制劑的標(biāo)準(zhǔn)中一定要制訂對(duì)映異構(gòu)體的檢查項(xiàng)�。
如無外消旋化發(fā)生,但同時(shí)有該手性藥物的外消旋體或?qū)τ钞悩?gòu)上市銷售����,則制劑的標(biāo)準(zhǔn)中不必制訂對(duì)映異構(gòu)體的檢查項(xiàng),但應(yīng)該定入立體專屬性的鑒別項(xiàng),以與該手性藥物的外消旋體或?qū)τ钞悩?gòu)體相區(qū)別�����。
如無外消旋化發(fā)生�����,并且也沒有該手性藥物的外消旋體或?qū)τ钞悩?gòu)體上市銷售���,則制劑的標(biāo)準(zhǔn)中既不必制訂對(duì)映異構(gòu)體的檢查項(xiàng),也不必定立體專屬性的鑒別項(xiàng)����,但企業(yè)可自行選擇。
5���、穩(wěn)定性研究
手性藥物因各自結(jié)構(gòu)的不同�,由于各種因素(如高溫�����、高濕�、酸、堿、強(qiáng)光等)的影響����,在放置過程中有可能發(fā)生外消旋化,因此在穩(wěn)定性研究時(shí)�,應(yīng)采用立體專屬性的分析方法對(duì)此進(jìn)行考察,以給處方及工藝的確定��、成品的儲(chǔ)存����、標(biāo)準(zhǔn)的制定提供依據(jù)。
對(duì)于原料藥來說���,穩(wěn)定性的要求是應(yīng)采用質(zhì)量標(biāo)準(zhǔn)中的方法考察其有無消旋化的傾向����。具體要求如下:
影響因素試驗(yàn)應(yīng)考察本品立體構(gòu)型的穩(wěn)定性���。
如影響因素試驗(yàn)證明本品立體構(gòu)型穩(wěn)定�,則加速試驗(yàn)及長期留樣試驗(yàn)只需在試驗(yàn)開始及結(jié)束時(shí)監(jiān)測立體構(gòu)型的變化��;
如影響因素試驗(yàn)證明本品立體構(gòu)型不穩(wěn)定�,則加速試驗(yàn)及長期留樣試驗(yàn)時(shí)����,應(yīng)多在幾個(gè)時(shí)間點(diǎn)監(jiān)測立體構(gòu)型變化情況����。
對(duì)于制劑來說要求是一樣的�����,即采用立體專屬性的分析方法考察本品有無消旋化的傾向���。