藥包材作為藥品的重要組成部分�,很大程度上保障了藥品性能�,藥品內(nèi)包材對于制劑質(zhì)量的影響也是很大的,在制劑劑型和生產(chǎn)中起著關(guān)鍵作用�,伴隨著藥品的生產(chǎn)、流通和使用全過程�����,直接關(guān)系到藥品的質(zhì)量和患者用藥安全�����。對于藥包材的標準的建設是一個從無到有循序漸進的過程�����,目前可分為三個階段。
階段1:舊版藥包材標準
1981年1月13日���,原國家醫(yī)藥管理總局頒發(fā)實施了《藥品包裝管理辦法(試行)》鼓勵藥包材行業(yè)組織制定相關(guān)藥包材產(chǎn)品標準���;在20世紀80年代至90年代,主要采用國標(GB)�����、醫(yī)藥標準(YY)的方式�����;在2002-2006年���,原國家食品藥品監(jiān)督管理局陸續(xù)頒布國家YBB標準6冊——《直接接觸藥品的包裝材料和容器標準匯編》�,收載了共139個藥包材品種標準�����、測定方法�����、指導原則等。
階段2:2015年版YBB標準
經(jīng)常提到的藥包材標準——YBB標準�,是“藥包標”的拼音首字母的簡稱,2009年開始���,由中國食品藥品檢定研究院作為牽頭單位�����,組織全國藥包材檢驗檢測機構(gòu)對6冊YBB標準進行整理、勘誤和匯編�,2015年12月1日起實施的《國家藥包材標準(2015版)》,對原139項藥包材標準進行了修訂完善���,對部分標準進行了合并和提高���,最終形成130項藥包材國家標準。里面涵蓋了玻璃類���、金屬類�、塑料類�����、橡膠類、預灌封類�����、其它類與方法類七大部分���,其中玻璃類26個標準���、金屬類5個標準、塑料類36個標準���、橡膠類4個標準�、預灌封類11個標準���、其他類1個標準���、方法類47個標準。
階段3:2020年版《中國藥典》標準
2020年12月份�����,發(fā)布了2020年版《中國藥典》,《中國藥典》藥包材標準起步較晚���,國家藥典委員會基于“借鑒國內(nèi)外經(jīng)驗�,立足我國國情�,國家標準保基本”的總原則�����,《中國藥典》2015年版開啟了藥包材標準納入《中國藥典》的序幕���,首次收載了藥包材標準——包裝材料的通用要求內(nèi)容,自2020年版起成功搭建了藥包材標準體系框架�����,收載了應用較廣泛���、相對成熟的2個通則和16種藥包材檢測方法�����,彌補了中國藥典沒有詳細藥包材檢測方法的這塊空白�����,自此中國藥典的中藥包材標準體系已初步搭建���。
從《中國藥典》2020年版標準框架體系來看�����,藥包材系列標準更加側(cè)重于以材料及其容器為主線的通用性標準�,目前2020版的中國藥典四部已有藥包材標準體系的指導原則詳見下表:
二�、2025年版《中國藥典》藥包材標準體系期待與展望
那么《中國藥典》2025年版在藥包材這塊將做出什么創(chuàng)新?下面讓筆者繼續(xù)來聊聊���。
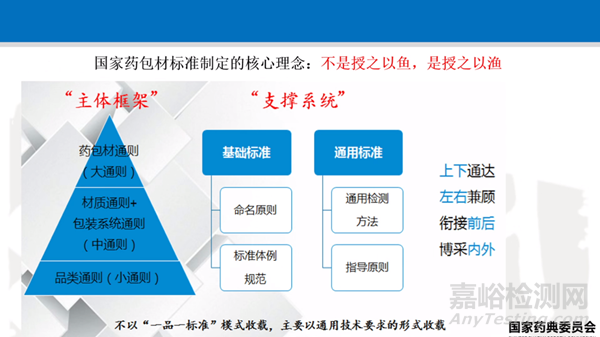
藥包材按種類分主要是:玻璃類�����、塑料類�、橡膠類�、預灌類(注射器)等,《中國藥典》2025年版不以“一品一標準”模式收載�,而主要采取通用技術(shù)要求的形式收載,主體框架采取大通則-藥包材通則�、中通則-材質(zhì)通則+包裝系統(tǒng)通則�、小通則-品類通則�����,同時也提到體系構(gòu)架過程中應特別關(guān)注“上下通達���、左右兼顧�����、銜接前后���、博采內(nèi)外”,后續(xù)將把成熟的相關(guān)通用技術(shù)要求和通用檢測方法逐步收載入藥典�����,比如藥用塑料材料和容器指導原則���、藥用橡膠密封件指導原則,使藥包材內(nèi)容更豐富和全面�����,新構(gòu)建藥包材標準體系主體框架和支撐系統(tǒng)如下圖。
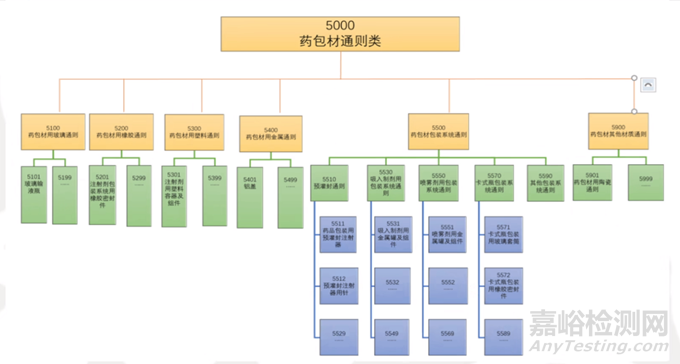
結(jié)合藥典編制大綱的要求和原則�����,根據(jù)現(xiàn)有藥典標準“以凡例為總體要求�����、通用技術(shù)要求為基本規(guī)定���、正文為具體要求”的特點���,2025年版藥典藥包材標準由采取大通則-藥包材通則、中通則-材質(zhì)通則+包裝系統(tǒng)通則���、小通則-品類通則主體框架共同構(gòu)成�����?��?蚣苁疽鈭D如下:
2022年12月19日,國家藥典委員會發(fā)布了《《中國藥典》(2025年版)編制大綱》���,編制大綱對于藥包材的標準���,任務清單梳理如下:
(1) 制定藥包材通則:內(nèi)容包含藥包材分類�����、生產(chǎn)�����、質(zhì)量評價�、使用�����、包裝�、儲運、安全性�����、相容性���、保護性�、功能性�����、穩(wěn)定性等總體要求�。
(2) 制定藥包材基礎標準和規(guī)范:如術(shù)語、命名原則�����、標準體例規(guī)范等�。
(3) 制定不同材質(zhì)藥包材通則:(如玻璃、橡膠���、塑料���、金屬、陶瓷等)和具體品類通則(如玻璃安瓿�、橡膠密封件、塑料硬片�、鋁蓋等),覆蓋常用藥包材的檢測項目�����、技術(shù)要求等。
(4) 制定特殊包裝系統(tǒng)的通則:如預充式包裝系統(tǒng)(包含預灌封注射器和筆式注射器等)�;開展對新型包裝系統(tǒng)或生產(chǎn)工藝的藥包材和新型材質(zhì)的藥包材通用技術(shù)要求的研究,如吸入制劑包裝系統(tǒng)���、一次成型包裝系統(tǒng)(如吹灌封包裝系統(tǒng)BFS�����、自動成型灌封袋FFS等)���、熱塑性彈性密封體、環(huán)烯烴共聚物等�����。
(5) 制定藥包材指導原則:如密封完整性�����、生物學安全性���、塑料和橡膠的穩(wěn)定性等評價指導原則�����;組織開展藥包材化學安全性評估指導原則的研究�。
(6) 制定配套的通用檢測方法�,優(yōu)化現(xiàn)有通用檢測方法。
(7) 組織開展藥包材全生命周期相關(guān)技術(shù)研究�,為科學制定藥包材標準提供技術(shù)支撐。
備注:編制大綱對于藥包材的標準編制內(nèi)容�,詳見國家藥典委員會發(fā)布的《《中國藥典》(2025年版)編制大綱》。
參考資料:
[1] www.chp.org.cn�����、第二屆藥包材標準與法規(guī)公益技術(shù)培訓等