摘要:本文總結(jié)抗體藥物質(zhì)量研究的共性問(wèn)題����,包括 國(guó)內(nèi)外法規(guī)技術(shù)指南介紹�����、細(xì)胞株的質(zhì)量控制��、抗體藥物的表征分析�����、抗體藥物的純度和雜質(zhì)分析和生物學(xué)活性一共五個(gè)部分��,旨在為從事生物制藥研究者提供借鑒。
一�����、 國(guó)內(nèi)外法規(guī)技術(shù)指南介紹
近年來(lái)醫(yī)藥工業(yè)對(duì)于生物大分子藥品質(zhì)量控制實(shí)踐經(jīng)驗(yàn)的不斷積累�����、分析手段的持續(xù)進(jìn)步����,以及質(zhì)量源于設(shè)計(jì)、風(fēng)險(xiǎn)評(píng)估等國(guó)際先進(jìn)藥品質(zhì)量控制理念的逐步推廣�����,推動(dòng)了各類生物藥質(zhì)量控制國(guó)際指南�����、法規(guī)的修訂����。抗體類藥物屬于重組技術(shù)產(chǎn)品,質(zhì)量控制方面應(yīng)滿足國(guó)內(nèi)外重組技術(shù)產(chǎn)品相關(guān)要求��。目前新版《WHO重組DNA產(chǎn)品質(zhì)量安全有效性評(píng)價(jià)指南》(WHO Guidelines on Quality����, Safety�����, and Efficacy of Biological Medicinal Products Prepared by Recombinant DNA Technology)已頒布�����;《歐洲藥典》(Monoclonal Antibodies for Human Use)《美國(guó)藥典》(Control Strategies for RecombinantTherapeutic Monoclonal Antibodies)均設(shè)立了針對(duì)抗體類產(chǎn)品的總論����,即 General Monograph或 General Chapter����;ICHQ5、Q6�����、Q8-Q11等技術(shù)指南為抗體類產(chǎn)品的質(zhì)量控制提供了指導(dǎo)性的范本�����。由于眾多生物藥物面臨專利保護(hù)到期,為了確保生物類似藥的質(zhì)量與安全�����,歐盟于2006年首先頒布實(shí)施了生物類似藥的指南�����,WHO和FDA也先后于200年和2012年頒布了生物類似藥指南��,并影響了亞洲�����、南美洲��、中東�����、非洲等醫(yī)藥工業(yè)相對(duì)欠發(fā)達(dá)的國(guó)家和地區(qū)類似法規(guī)的制定�����。近兩年這些國(guó)家都對(duì)已頒布的生物類似藥指南進(jìn)行了修訂,WHO也新增了針對(duì)單克隆抗體生物類似藥的技術(shù)指導(dǎo)原則����。
中國(guó)也于2015年2月發(fā)布了《生物類似藥研發(fā)與評(píng)價(jià)指導(dǎo)原則》。上述指南和法規(guī)中有大量是關(guān)于生物大分子量控制技術(shù)要求的論述��,使包括抗體在內(nèi)的生物大分子藥物質(zhì)量有了進(jìn)一步提升的空間��。
《中國(guó)藥典》(三部)頒布了我國(guó)單克隆抗體類生物治療藥物的總論和重組DNA技術(shù)產(chǎn)品總論��,在此基礎(chǔ)上制定相應(yīng)品種各論��,對(duì)新產(chǎn)品的質(zhì)量標(biāo)準(zhǔn)化研究具有重要的指導(dǎo)意義����。在抗體類藥物質(zhì)量控制方面����,應(yīng)當(dāng)依據(jù)或參照以上藥典標(biāo)準(zhǔn)進(jìn)行,同時(shí)也應(yīng)參照《人用重組DNA制品質(zhì)量控制技術(shù)指導(dǎo)原則》《人用單克隆抗體質(zhì)量控制技術(shù)指導(dǎo)原則》等相關(guān)國(guó)內(nèi)法規(guī)和技術(shù)指導(dǎo)原則的要求�����。
二、細(xì)胞株的質(zhì)量控制
細(xì)胞株的質(zhì)量控制在《中國(guó)藥典》(2020版)(三部)通則“生物制品生產(chǎn)檢定用動(dòng)物細(xì)胞基質(zhì)制備及檢定規(guī)程”中有非常具體的規(guī)定�����,用于生物制品生產(chǎn)和檢定的細(xì)胞株需通過(guò)全面的檢定����,目前單抗的細(xì)胞株主要有鼠源的SP20、NS0和CHO細(xì)胞株這幾種細(xì)胞除一般的細(xì)胞株的特征外����,還可能攜帶鼠源性的病毒等外源因子的污染,特別是自身攜帶的逆轉(zhuǎn)錄病毒�����,動(dòng)物試驗(yàn)顯示具有致腫瘤性��,因此必須嚴(yán)格控制細(xì)胞株的質(zhì)量����。申報(bào)單位不僅要提供規(guī)定十分詳實(shí)的文件資料��,還要有具體的試驗(yàn)結(jié)果,特別是包括病毒滅活工藝在內(nèi)的工藝驗(yàn)證資料�����,并經(jīng)過(guò)國(guó)家有關(guān)管理部門的認(rèn)可或批準(zhǔn)��。
2.1 重組工程細(xì)胞的構(gòu)建
宿主細(xì)胞的選擇
宿主細(xì)胞的選擇主要基于兩個(gè)方面的考慮:安全性及適用性。基于安全的考慮��,宿主細(xì)胞的來(lái)源及培養(yǎng)歷史應(yīng)十分清楚����,可溯源有關(guān)背景資料����,例如�����,最初分離建立株/系的機(jī)構(gòu)�����、是否有外源添加序列、傳代經(jīng)過(guò)及傳代過(guò)程中所用過(guò)的人源或動(dòng)物源性材料、細(xì)胞可能存在的內(nèi)源病毒及致瘤性等。對(duì)于改良的傳代細(xì)胞、全新構(gòu)建的轉(zhuǎn)化細(xì)胞等��,由于前期研究�����、背景資料和致瘤性風(fēng)險(xiǎn)等積累的認(rèn)識(shí)十分有限�����,其開(kāi)發(fā)應(yīng)用將引人新的安全性隱患��,需要慎重權(quán)衡利弊,在開(kāi)展充分研究的基礎(chǔ)上嚴(yán)格控制潛在的風(fēng)險(xiǎn)性��。
構(gòu)建過(guò)程中的質(zhì)量控制
目前可采用多種表達(dá)載體、基因?qū)敕椒ê秃Y選標(biāo)記等進(jìn)行工程細(xì)胞的構(gòu)建及篩選�����,構(gòu)建成功的標(biāo)志是工程細(xì)胞能夠穩(wěn)定、高效地表達(dá)結(jié)構(gòu)正確且具有生物活性的抗體����。構(gòu)建過(guò)程應(yīng)有詳細(xì)的克隆基因的序列��,包括插入的抗體基因及表達(dá)載體兩側(cè)端制區(qū)的核苷酸序列�����;應(yīng)詳細(xì)說(shuō)明載體引入宿主細(xì)胞的方法、載體在宿主細(xì)胞內(nèi)的狀態(tài)(是否整合到染色體內(nèi))及拷貝數(shù)�����;應(yīng)提供宿主和載體結(jié)合后的遺傳穩(wěn)定性資料;應(yīng)詳細(xì)敘述在生產(chǎn)過(guò)程中����,啟動(dòng)和控制克隆基因在宿主細(xì)胞中的表達(dá)所采用的方法及表達(dá)水平����。
2.2 細(xì)胞庫(kù)的建立
細(xì)胞庫(kù)的建立是為了保證重組單抗生產(chǎn)的穩(wěn)定性及批間一致性。參照《中國(guó)藥典》(2020版)(三部)中“生物制品生產(chǎn)檢定用動(dòng)物細(xì)胞基質(zhì)制備及檢定規(guī)程”的要求����,細(xì)胞庫(kù)為三級(jí)管理,即原始細(xì)胞庫(kù)�����、主細(xì)胞庫(kù)及工作細(xì)胞庫(kù)�����。如為引進(jìn)的細(xì)胞�����,可采用主細(xì)胞庫(kù)和工作細(xì)胞庫(kù)組成的二級(jí)細(xì)胞庫(kù)管理����。在某些特殊情況下��,也可使用主細(xì)胞庫(kù)級(jí)細(xì)胞庫(kù)�����,但須得到國(guó)務(wù)院藥品監(jiān)督管理部門的批準(zhǔn)。
原材料的選擇及細(xì)胞操作要求
用于建庫(kù)的初始工程細(xì)胞株應(yīng)為經(jīng)過(guò)克隆選擇而形成的均一細(xì)胞群體�����,必要時(shí)須經(jīng)與實(shí)際生產(chǎn)過(guò)程采用的無(wú)血清培養(yǎng)基和培養(yǎng)條件相一致的適應(yīng)性培養(yǎng)�����。細(xì)胞培養(yǎng)及擴(kuò)增所用原輔料應(yīng)按照國(guó)家藥品監(jiān)督管理總局有關(guān)規(guī)定執(zhí)行��;動(dòng)物源性原料的使用應(yīng)提供來(lái)源及質(zhì)控檢測(cè)資料����;細(xì)胞培養(yǎng)液不得含有人血清,不得使用青霉素或β-內(nèi)酰胺類抗生素�����;
細(xì)胞操作過(guò)程應(yīng)符合現(xiàn)行版《藥品生產(chǎn)質(zhì)量管理規(guī)范》的要求。生產(chǎn)人員應(yīng)定期檢查身體。為避免微生物污染和實(shí)驗(yàn)室中其他類型細(xì)胞的交叉污染,在生產(chǎn)區(qū)內(nèi)不得進(jìn)行微生物或非生產(chǎn)用細(xì)胞的操作��;在同一工作日進(jìn)行細(xì)胞操作前����,不得操作或接觸有感染性的微生物或動(dòng)物。
原始細(xì)胞庫(kù)(PCB)
重組工程細(xì)胞經(jīng)過(guò)克隆培養(yǎng)形成的均一細(xì)胞群體��,通過(guò)檢定可用于重組單抗的生產(chǎn),在特定條件下����,將一定數(shù)量、成分均一的細(xì)胞懸液�����,定量均勻分裝于安瓿��,于液氮或-130℃以下凍存�����,即為原始細(xì)胞庫(kù)�����,供建立主細(xì)胞庫(kù)用����。
主細(xì)胞庫(kù)(MCB)
取原始細(xì)胞庫(kù)細(xì)胞��,經(jīng)過(guò)一定方式進(jìn)行傳代��、增殖后均勻混合成一批,定量分裝保存于液氮或-130℃以下����,經(jīng)全面檢定合格后,即為主細(xì)胞庫(kù)��,用于工作細(xì)胞的制備�����。
工作細(xì)胞庫(kù)(WCB)
工作細(xì)胞庫(kù)的細(xì)胞由MCB細(xì)胞傳代擴(kuò)增制成����。由MCB的細(xì)胞經(jīng)傳代擴(kuò)增,達(dá)到定代次水平的細(xì)胞�����,合并成一批均質(zhì)細(xì)胞懸液�����,定量分裝于安瓿或適宜的細(xì)胞凍存管����,保存于液氮或-130以下備用����,即是工作細(xì)胞庫(kù)����。生產(chǎn)企業(yè)的工作細(xì)胞庫(kù)必須限定為一個(gè)細(xì)胞代次,凍存細(xì)胞的傳代水平需確保細(xì)胞復(fù)蘇后傳代增殖的細(xì)胞數(shù)量能滿足生產(chǎn)一批制品�����。復(fù)蘇后細(xì)胞的傳代水平不應(yīng)超過(guò)批準(zhǔn)用于生產(chǎn)的最高限定代次����。
2.3 細(xì)胞庫(kù)的管理
細(xì)胞庫(kù)中每支細(xì)胞應(yīng)有明確的標(biāo)記,包括細(xì)胞系/株名��、代次�����、批號(hào)����、編號(hào)����、凍存日期��、儲(chǔ)存容器的編號(hào)等�����;凍存前的活細(xì)胞比例應(yīng)不低于90%��,復(fù)蘇后細(xì)胞存活率應(yīng)不低于80%��,凍存后的細(xì)胞應(yīng)至少做一次復(fù)蘇培養(yǎng)并連續(xù)傳代至衰老期�����,檢查不同傳代水平的細(xì)胞生長(zhǎng)情況����;主細(xì)胞庫(kù)和工作細(xì)胞庫(kù)應(yīng)分別存放�����,非生產(chǎn)用細(xì)胞應(yīng)與生產(chǎn)用細(xì)胞嚴(yán)格分開(kāi)存放�����。上述各級(jí)種子庫(kù)的細(xì)胞應(yīng)按照特定的要求經(jīng)過(guò)全面檢定合格后方可使用。
2.4 細(xì)胞的檢定
合格的生產(chǎn)細(xì)胞是得到合格的重組抗體的前提和基礎(chǔ)����,為保證產(chǎn)品的安全性和有效性,應(yīng)對(duì)生產(chǎn)細(xì)胞進(jìn)行全面的檢定����。《中國(guó)藥典》(2015版)(三部)中“生物制品生產(chǎn)檢定用動(dòng)物細(xì)胞基質(zhì)制備及檢定規(guī)程”及“重組制品生產(chǎn)用哺乳動(dòng)物細(xì)胞質(zhì)量控制技術(shù)評(píng)價(jià)一般原則”對(duì)細(xì)胞的質(zhì)控內(nèi)容作了較為詳細(xì)的闡述����,主要包括細(xì)胞的鑒定及微生物污染的檢定。重組單抗生產(chǎn)細(xì)胞作為經(jīng)過(guò)DNA重組技術(shù)獲得的含有特定基因序列的細(xì)胞系��,在質(zhì)控內(nèi)容方面還增加了細(xì)胞穩(wěn)定性的考察�����、抗體基因或抗體的鑒別試驗(yàn)��、細(xì)胞產(chǎn)物中外源病毒因子的檢測(cè)��。
由于生產(chǎn)細(xì)胞分三級(jí)細(xì)胞庫(kù)管理�����,對(duì)于原始庫(kù)細(xì)胞和/或主庫(kù)細(xì)胞����,通常需要進(jìn)行一次全面系統(tǒng)的研究檢定,包括遺傳學(xué)�����、生物學(xué)和微生物學(xué)檢定��,以保證起始細(xì)胞的一致性并排除污染����。經(jīng)過(guò)傳代穩(wěn)定性研究的主細(xì)胞到工作細(xì)胞,只經(jīng)過(guò)簡(jiǎn)單的傳代��、擴(kuò)增����,可適當(dāng)簡(jiǎn)化檢定項(xiàng)目,重點(diǎn)檢測(cè)外源因子污染和細(xì)胞污染����。
細(xì)胞的鑒定
細(xì)胞鑒別試驗(yàn):現(xiàn)行藥典規(guī)定,新建細(xì)胞庫(kù)(MCB和wCB)及生產(chǎn)終末細(xì)胞應(yīng)進(jìn)行細(xì)胞鑒別試驗(yàn),以對(duì)細(xì)胞的種屬來(lái)源進(jìn)行確證并排除其他細(xì)胞的交叉污染�����。細(xì)胞鑒別可通過(guò)生長(zhǎng)形態(tài)��、生化檢測(cè)法(如同工酶法)免疫學(xué)檢測(cè)(如組織相容性抗原�����、中和特異性免疫血清)遺傳學(xué)檢測(cè)(如染色體核型����、標(biāo)記染色體檢測(cè))遺傳標(biāo)志檢測(cè)(如DNA指紋圖譜、STR圖譜����、基因組二核苷重復(fù)序列)等方法進(jìn)行;
抗體基因及抗體的鑒別試驗(yàn):抗體基因的檢測(cè)是抗體生產(chǎn)細(xì)胞鑒別試驗(yàn)的重要組成部分�����,其目的是保證生產(chǎn)細(xì)胞中抗體基因的正確與完整����,以得到結(jié)構(gòu)正確的抗體產(chǎn)品�����。常用的方法包括:通過(guò)PCR擴(kuò)增樣本DNA或用從細(xì)胞基質(zhì)中分離的RNA制備的cDNA來(lái)進(jìn)行DNA序列分析;通過(guò)限制酶酶譜和 Southern雜交來(lái)檢測(cè)基因的完整性確定目的基因的拷貝數(shù)�����,并檢測(cè)是否有任何序列插入或缺失等����。目的基因的檢測(cè)應(yīng)貫穿于工程細(xì)胞的構(gòu)建及篩選、細(xì)胞庫(kù)的建立和檢定�����,以及生產(chǎn)細(xì)胞培養(yǎng)監(jiān)控的全過(guò)程��?����?贵w產(chǎn)物可通過(guò)免疫斑點(diǎn)或免疫印跡試驗(yàn)等進(jìn)行鑒別��;
致瘤性鑒定:目前生產(chǎn)重組單抗經(jīng)常用到的細(xì)胞株CHO��、NS0、C127等已證明具有致瘤性�����,國(guó)外指導(dǎo)原則通常不再要求進(jìn)行致瘤性檢查�����,但對(duì)于該細(xì)胞來(lái)源的制品����,要優(yōu)化生產(chǎn)工藝,嚴(yán)格限制致瘤性成分如宿主殘余DNA在成品中的含量��;現(xiàn)行藥典也規(guī)定對(duì)于已證明具有致瘤性的傳代細(xì)胞可不必進(jìn)行致��,性檢查����,但一般認(rèn)為生產(chǎn)中應(yīng)用的插入外源基因的工程細(xì)胞應(yīng)當(dāng)視為全新的細(xì)胞,必須進(jìn)行致瘤性的檢查��,并在細(xì)庫(kù)檢定中進(jìn)行傳代/擴(kuò)增過(guò)程中的對(duì)比試驗(yàn)�����,觀察致瘤性特征的改變,并制定后續(xù)處理工藝條件和限制性要求�����,對(duì)致瘤性帶來(lái)的安全性風(fēng)險(xiǎn)進(jìn)行控制�����;
致瘤性試驗(yàn)可通過(guò)體內(nèi)試驗(yàn)和體外試驗(yàn)進(jìn)行�����。體內(nèi)試驗(yàn)有裸鼠法和新生小鼠法��,體外法可采用軟瓊脂克隆形成試驗(yàn)或器官培養(yǎng)試驗(yàn)����,具體實(shí)驗(yàn)操作參見(jiàn)現(xiàn)行藥典中“生物制品生產(chǎn)檢定用動(dòng)物細(xì)胞基質(zhì)制備及檢定規(guī)�����。
病原微生物檢測(cè)
細(xì)菌��、真菌及支原體檢查:對(duì)細(xì)胞培養(yǎng)上清液進(jìn)行無(wú)菌檢查��,結(jié)果須符合規(guī)定要求。使用的培養(yǎng)基應(yīng)適合需氧菌��、厭氧菌和真菌的生長(zhǎng)�����,并且培養(yǎng)基的靈敏度要滿足要求�����。無(wú)菌檢查法包括直接接種法和薄膜過(guò)濾法��,如供試品允許����,應(yīng)優(yōu)先采用薄膜過(guò)濾法。對(duì)于直接接種法�����,若制品中含有防腐劑�����,應(yīng)先行增菌培養(yǎng)。在進(jìn)行支原體檢查時(shí)��,應(yīng)注意同時(shí)進(jìn)行培養(yǎng)法和指示細(xì)胞法兩種方法��;
內(nèi)�����、外源病毒因子檢查:用于確定待檢細(xì)胞中是否存在潛在的可感染的病毒如鼠源性病毒)及操作帶人的外源性病毒�����。檢測(cè)病毒的種類及方法須根據(jù)細(xì)胞的種屬來(lái)源及細(xì)胞特性決定�����,對(duì)于重組工程細(xì)胞來(lái)說(shuō)��,還應(yīng)當(dāng)對(duì)細(xì)胞裂解物或收獲液進(jìn)行外源因子檢測(cè)�����。
一般病毒因子可通過(guò)細(xì)胞形態(tài)觀察及紅細(xì)胞吸附試驗(yàn)����、不同細(xì)胞傳代培養(yǎng)法及接種動(dòng)物和雞胚法檢測(cè)�����,其中《中國(guó)藥典》(2015版)(三部)中新增規(guī)定:用不同細(xì)胞傳代培養(yǎng)法檢測(cè)病毒因子時(shí),應(yīng)設(shè)立病毒陽(yáng)性對(duì)照����,包括可觀察細(xì)胞病變的病毒陽(yáng)性對(duì)照及血吸附陽(yáng)性對(duì)照。另外�����,新版藥典對(duì)檢定用細(xì)胞也增加了明確要求�����,具體參見(jiàn)《中國(guó)藥典》(2015版)中“生物制品生產(chǎn)檢定用動(dòng)物細(xì)胞基質(zhì)制備及檢定規(guī)程”��。對(duì)于逆轉(zhuǎn)錄病毒及其他內(nèi)源性病毒或病毒核酸的檢測(cè)����,現(xiàn)行藥典規(guī)定:小鼠來(lái)源和其他嚙齒類來(lái)源的細(xì)胞系或其雜交瘤細(xì)胞系有可能攜帶潛在的逆轉(zhuǎn)錄病毒。因此����,對(duì)于人-鼠雜交瘤細(xì)胞系應(yīng)進(jìn)行特異性逆轉(zhuǎn)錄病毒檢測(cè)。如用于單克隆抗體生產(chǎn)的小鼠細(xì)胞系,則可不檢測(cè)特異性的逆轉(zhuǎn)錄病毒��,但在生產(chǎn)工藝中應(yīng)增加病毒滅活程序��。根據(jù)待檢細(xì)胞系/株的種屬及組織來(lái)源�����,還應(yīng)進(jìn)行特殊外源病毒因子的檢測(cè)��。如為鼠源細(xì)胞系��,一般檢測(cè)出血熱病毒����、淋巴細(xì)胞脈絡(luò)從腦膜炎病毒、Ⅲ型呼腸孤病毒��、仙臺(tái)病毒����、脫腳病病毒����、小鼠腺病毒、小鼠肺炎病毒、逆轉(zhuǎn)錄病毒等��;如為人源細(xì)胞系��,應(yīng)檢測(cè)人鼻咽癌病毒�����、人巨細(xì)胞病毒��、人逆轉(zhuǎn)錄病型肝炎病毒��、人丙型肝炎病毒等��。
細(xì)胞株的穩(wěn)定性研究
抗體生產(chǎn)細(xì)胞一般為通過(guò)基因工程獲得的重組工程細(xì)胞����,生產(chǎn)者須具有相關(guān)的穩(wěn)定性研究資料,包括重組細(xì)胞的遺傳穩(wěn)定性����、目的基因表達(dá)穩(wěn)定性、目的產(chǎn)品持續(xù)生產(chǎn)的穩(wěn)定性��,以及一定條件下保存時(shí)細(xì)胞生產(chǎn)抗體產(chǎn)品能力的穩(wěn)定性等資料�����。
三、抗體藥物的表征分析
單克隆抗體是迄今為止分子量?jī)H次于重組人凝血因子Ⅷ的藥用蛋白��,其分子結(jié)構(gòu)具備高度的復(fù)雜性�����。IgG型抗體是由兩條重鏈(≈50kDa)和兩條輕鏈(≈25kDa)經(jīng)鏈間二硫鍵相連����,所構(gòu)成的“Y”形四聚體糖蛋白。一般在抗體的恒定區(qū)或可變區(qū)還存在MO糖基化修飾����。抗體藥物與藥物靶標(biāo)特異性結(jié)合后��,通過(guò)阻斷細(xì)胞信號(hào)轉(zhuǎn)導(dǎo)通路��,或誘導(dǎo)效應(yīng)功能�����,如抗體依賴的細(xì)胞介導(dǎo)的細(xì)胞毒性作用(ADCC)補(bǔ)體依賴的細(xì)胞毒作用(CDC)�����、抗體依賴的細(xì)胞介導(dǎo)的細(xì)胞吞噬作用(ADCP)或運(yùn)載偶聯(lián)小分子化藥等多種方式發(fā)揮作用�����。
由于重組抗體的制備工藝采用動(dòng)物細(xì)胞異源表達(dá)�����,其分子結(jié)構(gòu)上存在多種翻譯后修飾�����。因此��,抗體藥物的結(jié)構(gòu)還具有顯著的“異質(zhì)性”或“非均一性”的特點(diǎn)����。根據(jù)IgG型抗體潛在的修飾位點(diǎn)(NO糖基化、焦谷氨酸環(huán)化�����、賴氨酸剪切��、天冬氨酸異構(gòu)及甲硫氨酸氧化等),推測(cè)出的理論變異體至少有108種�����,這些修飾變異又表現(xiàn)為分子大小����、電荷、糖譜等多種形式的差異����。臨床研究已經(jīng)證實(shí),某些抗體藥物的變異體具有不同的藥代����、藥效和免疫原性屬性?�?梢哉f(shuō)����,抗體分子結(jié)構(gòu)上存在的“復(fù)雜性”和“異質(zhì)性”,決定了抗體藥物表征研究的難度與挑戰(zhàn)��。
正確的分子結(jié)構(gòu)是保證抗體藥物安全�����、有效的物質(zhì)基礎(chǔ)�����。質(zhì)量研究中對(duì)抗體藥物進(jìn)行全面的表征研究是進(jìn)行質(zhì)量控制的重要手段�����。因此����,國(guó)內(nèi)外關(guān)于抗體藥物研發(fā)的指導(dǎo)原則均強(qiáng)調(diào),抗體藥物的表征研究應(yīng)采用現(xiàn)有先進(jìn)的分析手段( state-of-the-art)����,從物理化學(xué)、免疫學(xué)��、生物學(xué)等角度對(duì)產(chǎn)品進(jìn)行全面的分析��,并提供盡可能詳盡的信息以反映目標(biāo)產(chǎn)品內(nèi)在的質(zhì)量屬性�����。下文將結(jié)合抗體藥物具體案例,介紹抗體藥物表征研究的主要內(nèi)容與一般方法����。
一級(jí)結(jié)構(gòu)
分子量
由于抗體的恒定區(qū)具有糖基化修飾,一般經(jīng)過(guò)脫糖處理后測(cè)定分子量�����。通過(guò)實(shí)測(cè)值和理論值的比較����,可以初步判定抗體藥物序列是否正確。例如�����,某曲妥珠生物類似藥完整蛋白分子量與原研參比存在64Da差異�����,重鏈分子量與原研參比存在32Da差異��,因此��,可初步判定該生物類似藥重鏈氨基酸序列存在錯(cuò)誤或翻譯后修飾。
氨基酸序列
抗體藥物的一級(jí)結(jié)構(gòu)(氨基酸序列)是其生物活性�����、臨床療效的物質(zhì)基礎(chǔ)�����,尤其是對(duì)于生物類似藥而言��,確保氨基酸序列與原研參比一致是首要條件�����。一般重組抗體經(jīng)蛋白酶切(LsC����、AspN或GuC)后����,利用串聯(lián)液相質(zhì)譜技術(shù)進(jìn)行肽質(zhì)量圖譜分析來(lái)確證氨基酸序列。例如����,上文提及的曲妥珠生物類似藥經(jīng)肽質(zhì)量圖譜分析確定,其分子量差異位于胰蛋白酶酶切肽段T35上。在生物類似藥開(kāi)發(fā)的早期篩選階段也會(huì)出現(xiàn)一級(jí)結(jié)構(gòu)的改變�����,均可以利用質(zhì)譜技術(shù)予以鑒定����。
氨基酸含量分析
重組抗體酸水解后,經(jīng)衍生化試劑處理后可使用液相定量分析其氨基酸含量����。但是由于水解過(guò)程中對(duì)于穩(wěn)定性差的氨基酸(絲氨酸、蘇氨酸等)破壞較大��,或某些氨基酸因空間位阻原因難于水解(異亮氨酸)����,某些氨基酸的實(shí)際測(cè)定值偏低。此外��,對(duì)于生物大分子而言�����,氨基酸含量?jī)H是其一級(jí)序列確證的佐證��,并不能表明其氨基酸序列的正確性。因此�����,氨基酸含量分析在抗體藥物的結(jié)構(gòu)確證研究中意義有限�����。
N/C端異質(zhì)性
N端測(cè)序是抗體藥物一級(jí)結(jié)構(gòu)鑒定的重要方法��,通常將還原后的抗體輕����、重鏈經(jīng)Edman降解依次測(cè)定N端氨基酸序列�����。若抗體的N端存在焦谷氨酰封閉��,需采用焦谷氨肽酶去封閉后再進(jìn)行 Edman降解測(cè)定��。重組表達(dá)的抗體藥物由于工程細(xì)胞內(nèi)羧肽酶D的降解����,還會(huì)導(dǎo)致重鏈C端賴氨酸不完全剪切。目前,已經(jīng)證實(shí)重組抗體普遍存在著NC端異質(zhì)性的現(xiàn)象����,并且沒(méi)有證據(jù)表明NC端異質(zhì)性對(duì)抗體的安全性、有效性產(chǎn)生影響����。但是,通過(guò)NC異質(zhì)性的分析有助于加強(qiáng)重組抗體藥物的質(zhì)量控制�����。為了減少C端的異質(zhì)性����,亦有通過(guò)基因水平去除末端賴氨酸的設(shè)計(jì)。
氨基酸修飾分析
抗體藥物的質(zhì)量肽圖通過(guò)測(cè)定肽段分子量及二級(jí)碎片分子量��,可以進(jìn)一步分析氨基酸的修飾類型及其比例����,如脫酰胺、甲硫氨酸氧化��、糖基化修飾��、N端焦谷氨酸環(huán)化、C端賴氨酸切除等�����。目前已經(jīng)證實(shí)在加速降解條件下����,抗體CDR區(qū)氨基酸的化學(xué)修飾可能會(huì)影響其親和力和生物學(xué)活性。鑒定修飾的類型及位置可作為抗體藥物CQA評(píng)定的重要指標(biāo)�����。
糖基化修飾
除了個(gè)別改構(gòu)的IgG1(N297A)型抗體不具有糖基化修飾外��,絕大多數(shù)抗體和抗本融合蛋白均存在M糖或O-糖修飾��?����?贵w的M糖修飾發(fā)生在“Asn- X-Ser/Thr”(X為除Pro外的任意氨基酸)序列中的Asn位點(diǎn)�����。O糖修飾沒(méi)有特殊基序結(jié)構(gòu)��,多發(fā)生在抗體融合蛋白序列的Ser和Thr的羥基上�����。糖基化修飾在維持抗體正常結(jié)構(gòu)和生物活性上發(fā)揮著重要作用����。例如,高半乳糖修飾可提高抗體的CDC效應(yīng)�����;低巖藻糖修飾可提高抗體的ADCC����、ADCP效應(yīng);而a1,3半乳糖或NGNA等非人糖基化修飾則可在臨床上引起免疫原性等��,
因此�����,需要對(duì)糖基化位點(diǎn)����、寡糖分布及糖鏈結(jié)構(gòu)等進(jìn)行充分研究�����。例如��,阿巴西普存在3個(gè)M糖基化修飾位點(diǎn)和4個(gè)O糖基化修飾位點(diǎn)����;依那西普含有3個(gè)N糖修飾位點(diǎn)和13個(gè)0糖修飾位點(diǎn)����;西妥昔單抗在Fab和Fe區(qū)域均具有M糖修飾。寡糖分布是對(duì)抗體藥物中不同修飾形式的寡糖鏈所占比例進(jìn)行分析����。一般使用糖苷酶酶切糖鏈后,經(jīng)衍生化處理�����,使用液相色譜分析確定各寡糖鏈所占的比例����。在抗體藥物的質(zhì)量控制中��,對(duì)于影響抗體效應(yīng)功能的寡糖分布,應(yīng)重點(diǎn)關(guān)注并進(jìn)行控制����。例如,以ADCC效應(yīng)為主要作用機(jī)制的曲妥珠單抗��,應(yīng)重點(diǎn)關(guān)注影響恒定區(qū)效應(yīng)功能的寡糖分布����,但是曲妥珠單抗原研產(chǎn)品不同批次的糖基化修飾亦有較大的變異。糖鏈的結(jié)構(gòu)分析一般釆用多種糖苷酶分步酶切確定單糖連接方式�����,通過(guò)測(cè)定糖鏈分子量預(yù)測(cè)糖鏈結(jié)構(gòu)��。
二級(jí)結(jié)構(gòu)
二硫鍵
IgG型抗體由兩條輕鏈和重鏈����,通過(guò)鏈間二硫鍵組裝而成。二硫鍵的構(gòu)型有時(shí)可以顯著影響抗體的功能��。二硫鍵的測(cè)定通常采用酶切后質(zhì)量肽圖譜的方法����,通過(guò)測(cè)定還原與非還原狀態(tài)的酶切分子量或通過(guò)二硫鍵肽段的二級(jí)質(zhì)譜碎片來(lái)確證抗體二硫鍵配對(duì)情況�����?���?贵w藥物的表征研究既要驗(yàn)證正確的二硫鍵配對(duì)��,也要關(guān)注二硫鍵錯(cuò)配形式�����。對(duì)于治療性抗體應(yīng)用較多的IgG亞型:IgG1和IgG4抗體分子內(nèi)含有16個(gè)二硫鍵����,其中鏈內(nèi)二硫鍵12個(gè),鏈間二硫鍵4個(gè)�����;1gG2抗體分子內(nèi)含有18個(gè)二硫鍵����,其中鏈內(nèi)二硫鍵12個(gè)����,鏈間二硫鍵6個(gè)�����;而對(duì)于復(fù)雜的抗體融合蛋白依那西普��,則含有29個(gè)二硫鍵和多種錯(cuò)配形式二硫鍵�����。
自由巰基
理論上含完整二硫鍵的IgG抗體分子內(nèi)應(yīng)不存在自由巰基����,但是由于有些抗體存在額外的半胱氨酸或者存在未形成二硫鍵的半胱氨酸殘基����,抗體分子中一般含有少量的自由巰基(0.02 mol/mol蛋白左右〉通常采用 ELLMAN試劑法測(cè)定自由巰基,其原理為DTNB與抗體的自由巰基反應(yīng)后生成TNB�����,根據(jù)TNB吸光度確定抗體的自由巰基含量��。
高級(jí)結(jié)構(gòu)
測(cè)定抗體分子高級(jí)結(jié)構(gòu)的常用方法是圓二色譜法,該方法利用蛋白質(zhì)的圓二色性及不對(duì)稱分子對(duì)左右圓偏振光吸收的不同來(lái)進(jìn)行結(jié)構(gòu)分析�����。遠(yuǎn)紫外區(qū)(190-230mm)光譜可反映蛋白質(zhì)二級(jí)結(jié)構(gòu)��,即α螺旋��、β折疊����、轉(zhuǎn)角和不規(guī)則卷曲的比例。近紫外區(qū)(250-350mm)光譜反映蛋白三級(jí)結(jié)構(gòu)變化�����,即側(cè)鏈生色基團(tuán)色氨酸�����、苯丙氨酸����、酪氨酸等殘基的排布信息和二硫鍵微環(huán)境的變化;此外�����,差示掃描量熱法、氫氘交換質(zhì)譜傅里葉轉(zhuǎn)換紅外光譜X光晶體學(xué)核磁共振技術(shù)等也常用于分析抗體藥物的高級(jí)結(jié)構(gòu)����。
免疫學(xué)活性
可變區(qū)抗原親和力
抗體藥物的靶向特異性體現(xiàn)在其可變區(qū)與靶抗原特異性結(jié)合��,可變區(qū)的抗原親和力一般采用酶聯(lián)免疫吸附法��、流式細(xì)胞術(shù)和BA法等方法進(jìn)行測(cè)定�����。采用競(jìng)爭(zhēng)ELSA法測(cè)定抗體結(jié)合活性時(shí)����,將供試品與標(biāo)準(zhǔn)品與酶標(biāo)抗體竟?fàn)幗Y(jié)合包被抗原,對(duì)抗體濃度與吸光值的量效關(guān)系進(jìn)行四參數(shù)擬合后��,計(jì)算供試品與標(biāo)準(zhǔn)品的ECs值來(lái)評(píng)價(jià)抗體藥物的結(jié)合活性�����;流式細(xì)胞術(shù)通過(guò)測(cè)定抗體與表達(dá)抗原的靶細(xì)胞之間的結(jié)合陽(yáng)性率�����,評(píng)價(jià)抗體與細(xì)胞表面抗原的結(jié)合活性;BIA法是通過(guò)實(shí)時(shí)�����、動(dòng)態(tài)監(jiān)測(cè)抗體與芯片表面固化的抗原之間的結(jié)合解離反應(yīng)�����,計(jì)算出抗體的親和常數(shù)等動(dòng)力學(xué)參數(shù)��。
恒定區(qū)效應(yīng)功能
抗體的恒定區(qū)通過(guò)與FcR結(jié)合介導(dǎo)ADCC����、ADCP等功能,通過(guò)與C1q結(jié)合介導(dǎo)CDC功能�����,通過(guò)與新生兒受體FRn結(jié)合延長(zhǎng)抗體在體內(nèi)的半衰期����。因此,可以通過(guò)測(cè)定抗體與相應(yīng)受體結(jié)合力(CD16�����,C1q)來(lái)間接反映其潛在體內(nèi)效應(yīng)功能,也可以采用基于細(xì)胞的生物測(cè)活方法直接測(cè)定恒定區(qū)介導(dǎo)的效應(yīng)功能�����。例如����,采用新鮮分離的人外周血單個(gè)核細(xì)胞或NK細(xì)胞作為效應(yīng)細(xì)胞�����,或者采用報(bào)告基因法測(cè)定抗體介導(dǎo)的ADCC效應(yīng)��;采用補(bǔ)體與靶細(xì)胞共孵育的方法�����,測(cè)定抗體介導(dǎo)的CDC效應(yīng)��。
生物學(xué)活性
抗體藥物的生物活性直接反映了其臨床應(yīng)用的體內(nèi)效力����,是抗體藥物質(zhì)量控制的重要指標(biāo)��?���?贵w藥物的生物學(xué)活性測(cè)定��,一般采用體外細(xì)胞法或動(dòng)物模型法模擬藥物的體內(nèi)作用機(jī)制��,并通過(guò)與活性標(biāo)準(zhǔn)品的比較對(duì)其量效關(guān)系進(jìn)行賦值評(píng)價(jià)����。
常用生物活性測(cè)定方法主要有細(xì)胞增殖抑制法、細(xì)胞毒性法��、抗體依賴性細(xì)胞介導(dǎo)的細(xì)胞毒性法和補(bǔ)體依賴的細(xì)胞毒性法等��。例如�����,靶向細(xì)胞生長(zhǎng)因子(VEGF����、Her2、BGFR等)抗腫瘤單抗均采用表達(dá)靶抗原的細(xì)胞( HUVEC�����、BT474、DiFi等)進(jìn)行細(xì)胞增殖抑制實(shí)驗(yàn)進(jìn)行生物測(cè)活��;靶向TNF-α的抗體或融合蛋白����,根據(jù)拮抗TNF-α對(duì)敏感細(xì)胞系(L929細(xì)胞)的殺傷活性測(cè)定生物活性;利妥昔單抗通過(guò)測(cè)定介導(dǎo)補(bǔ)體對(duì)靶細(xì)胞的殺傷測(cè)定生物活性等����。
近年來(lái)����,除了上述采用原代細(xì)胞生物測(cè)活外,通過(guò)導(dǎo)入抗體靶標(biāo)和報(bào)告基因構(gòu)建的轉(zhuǎn)基因指示細(xì)胞株開(kāi)始應(yīng)用于抗體藥物的生物測(cè)活��。例如����,靶向PD-1或PDL1單抗采用穩(wěn)轉(zhuǎn)NFAT報(bào)告基因和人PD1的 Jurkat細(xì)胞作為效應(yīng)細(xì)胞,采用高表達(dá)人PDL1的CHO細(xì)胞作為靶細(xì)胞�����。在效應(yīng)細(xì)胞與靶細(xì)胞共孵育條件下加入抗體,根據(jù)熒光素酶檢測(cè)系統(tǒng)評(píng)價(jià)抗PDL1抗體生物活性����。
對(duì)于抗體藥物而言,表征研究始終貫穿著藥物研發(fā)的生命周期�����。申請(qǐng)臨床前����,在工藝開(kāi)發(fā)、CQA�����、CPP評(píng)估����、質(zhì)量研究和穩(wěn)定性研究中對(duì)候選藥物進(jìn)行充分的表征研究有助于盡早鎖定生產(chǎn)工藝,確定批次放行質(zhì)量標(biāo)準(zhǔn)和產(chǎn)品的儲(chǔ)存條件及有效期��;產(chǎn)品申請(qǐng)上市前��,對(duì)工藝驗(yàn)證批次產(chǎn)品的質(zhì)量進(jìn)行表征研究�����,可以證明擬上市規(guī)模下生產(chǎn)工藝的穩(wěn)健性和產(chǎn)品質(zhì)量的一致性;在產(chǎn)品上市后��,如果發(fā)生生產(chǎn)工藝的變更����,要提供變更前后多批次產(chǎn)品的表征研究數(shù)據(jù)����,以支持工藝變更前后產(chǎn)品質(zhì)量具有“可比性”。此外��,近年來(lái)國(guó)內(nèi)外正在興起抗體生物類似藥研發(fā)的熱潮��。其中�����,對(duì)多批次原研參比和生物類似藥進(jìn)行全面表征比對(duì)研究����,也是證實(shí)生物類藥具備“質(zhì)量相似性”�����,進(jìn)而減免非臨床、臨床研究的關(guān)鍵所在��。
四�����、抗體藥物的純度和雜質(zhì)分析
4.1 大小異質(zhì)性分析
純度測(cè)定是重組蛋白藥物的一項(xiàng)重要檢測(cè)指標(biāo)��,該指標(biāo)直接反映了抗體純化工藝水平及產(chǎn)品質(zhì)量的高低�����?����?贵w純度測(cè)定主要涉及兩個(gè)方面的問(wèn)題�����。一是抗體分子與雜質(zhì)的有效分離�����。在實(shí)際測(cè)定中����,某些產(chǎn)品相關(guān)雜質(zhì),如肽鏈截短或延長(zhǎng)形式�����、修飾形式����、聚合體����、多聚體等,由于性質(zhì)與主蛋白比較接近����,分離起來(lái)可能有些困難����,須選用合適的分離方法��。二是對(duì)主蛋白及雜質(zhì)的檢測(cè)與定量��。常用的檢測(cè)器有紫外檢測(cè)器�����、凝膠成像掃描儀����、熒光檢測(cè)器����、電化學(xué)檢測(cè)器�����、示差檢測(cè)器�����、蒸發(fā)光檢測(cè)器��、質(zhì)譜檢測(cè)器等�����。由于各種檢測(cè)器靈敏度的限制����,有些生產(chǎn)純化過(guò)程及操作環(huán)境中引人的微量雜質(zhì)不易檢測(cè)到�����。為避免一種檢測(cè)方法在蛋白純度檢測(cè)中的偏差�����,一般選用至少兩種分離方法進(jìn)行檢測(cè),以得到相對(duì)準(zhǔn)確的純度信息����。測(cè)定抗體純度的常用方法是非還原型或還原型SDSPAGE或 CE-SDS法����、分子排阻色譜法( SEC-HPLC)等方法,對(duì)單體����、聚合體或片段進(jìn)行定量分析����,如供試品具有Fc效應(yīng)子功能�����,則還需關(guān)注非糖基化重鏈的情況��。供試品測(cè)定結(jié)果應(yīng)在規(guī)定的范圍內(nèi)����。
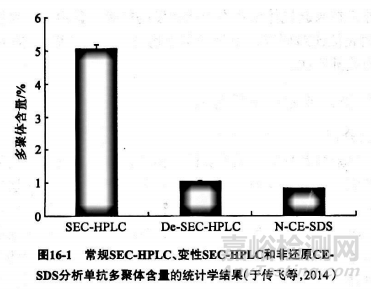
單克隆抗體(單抗)由兩條重鏈和兩條輕鏈構(gòu)成�����,相對(duì)分子量高達(dá)15萬(wàn)Da左右��,結(jié)構(gòu)復(fù)雜,其中大小異質(zhì)性是單抗的重要質(zhì)控指標(biāo)之一��。大小異質(zhì)性一般可分為三類����,即單體、片段和多聚體�����。片段包括降解的單抗和組裝不完全的重輕鏈等����;而多聚體則包括二聚體、寡聚體或更復(fù)雜的聚體等�����,多聚體不僅可能是單抗中的無(wú)效成分����,還是導(dǎo)致單抗免疫原性的重要原因之一�����,所以大小異質(zhì)性是單抗生產(chǎn)工藝優(yōu)化、生產(chǎn)過(guò)程控制及放行分析中不可或缺的檢測(cè)項(xiàng)目����,也是單抗穩(wěn)定性評(píng)價(jià)的重要指標(biāo)之一����。隨著技術(shù)的進(jìn)步,單抗大小異質(zhì)性的分析手段不斷涌現(xiàn)����,不同的分析技術(shù)其分析原理不同,所獲得的結(jié)果反映單抗在大小異質(zhì)性方面不同的特性����。由于 SEC-HPLC及 CE-SDS相對(duì)簡(jiǎn)單易行,成為分析單抗類制品大小異質(zhì)性的兩種常規(guī)方法����。有研究利用非還原(SDS和碘乙酰胺處理)及常規(guī)(無(wú)處理)和變性(SDS和碘乙酰胺處理) SEC-HPLC評(píng)價(jià)了一種抗ⅤEGF單抗的大小異質(zhì)性�����,初步闡明了二者結(jié)果差異的原因�����,為單抗制品的質(zhì)量控制研究提供了理論基礎(chǔ)����。
三種分析的結(jié)果比較如圖16-1所示��,可以看出非還原 CE-SDS的多聚體含量分析結(jié)果顯著低于常規(guī) SEC-HPLO��,但與變性 SEC-HPLC的分析結(jié)果基本一致。多聚體為共價(jià)和非共價(jià)結(jié)合兩種形式總和��,而在 CE-SDS分析的情況下��,由于去垢劑SDs的存在�����,非共價(jià)形式的多聚體被解離成為單體,所以多聚體的含量相比常規(guī) SEC-HPLC明顯降低。在變性 SEC-HPLC分析的情況下����,由于SDS的存在�����,多聚體含量則與非還原CE-SDS的分析結(jié)果基本一致��。所以與非還原 CE-SDS相比, SEC-HPLC可更加客觀地評(píng)價(jià)樣品中總多聚體的百分比含量����。該研究分析的單抗樣品多聚體主要是以非共價(jià)鍵的形式連接��,所以應(yīng)注意兩種方法所得到的多聚體含量結(jié)果具有不同的含義����,在分析多聚體含量時(shí)����,常規(guī) SEC-HPLC分析比 CE-SDS分析更加客觀��。
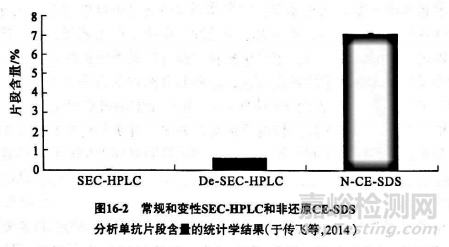
對(duì)于片段分析�����,由圖16-2可以看出��,非還原 CE-SDS所分析的片段比例顯著大于常規(guī)和變性 SEC-HPLC��,其主要原因是 SEC-HPLO的分辨率較低,無(wú)法對(duì)單體及大部分片段進(jìn)行有效分離����。單抗分子中往往有少部分重鏈和/或輕鏈的鏈間二硫鍵連接不完全��,以非共價(jià)鍵與單抗其他部分相連接����。而SDS可打開(kāi)非共價(jià)鍵,所以在非還原CESDS分析結(jié)果中�����,除HHLL(全抗分子)外�����,還可形成HHL�����、H����、H��、H、L����,以及其他與單抗非共價(jià)結(jié)合的降解片段�����;常規(guī) SEC-HPLO由于不能有效解離非共價(jià)結(jié)合的片段����,加之其低分辨率�����,對(duì)片段含量的檢測(cè)有一定的局限性�����,所以非還原 CE-SDS和SEC-HPLC二者片段峰所代表的形式并不相同。
上述研究初步闡明了單抗類制品大小異質(zhì)性的兩種常規(guī)放行分析方法即 SEC-HPLO和非還原 CE-SDS二者結(jié)果差異的原因����,為單抗制品的質(zhì)量控制研究提供了理論基礎(chǔ)��,為單抗分子大小變異體質(zhì)檢策略提供了技術(shù)支撐����。
4.2 電荷異質(zhì)性分析
單抗類制品的多種翻譯后修飾可導(dǎo)致其電荷異質(zhì)性��,而某些電荷異質(zhì)性由于對(duì)單抗穩(wěn)定性及其生物學(xué)功能發(fā)揮具有重要的影響而成為關(guān)鍵質(zhì)量屬性(CQA)��,并且電荷異質(zhì)性可反映其生產(chǎn)工藝的穩(wěn)定性�����,所以受到生物技術(shù)產(chǎn)業(yè)界及監(jiān)管機(jī)構(gòu)密切關(guān)注。成像毛細(xì)管等電聚焦電泳是單抗電荷異質(zhì)性分析的常用分析技術(shù)��,可利用此方法對(duì)單抗電荷異質(zhì)性峰的組成進(jìn)行初步研究����。
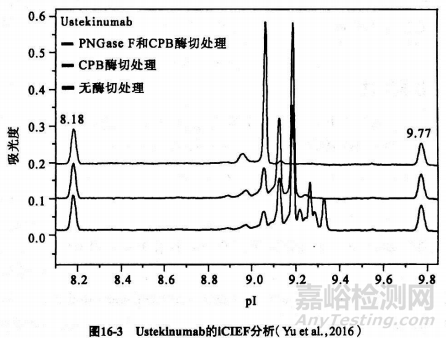
將單抗 Ustekinumab(由SP2/0細(xì)胞表達(dá))用羧肽酶B去除C性峰為C端賴氨酸不均一性所引起�����,如圖16-3所示��。但是經(jīng)羧肽酶B酶切后�����,其主峰前仍有2個(gè)比例較高的酸性峰����。為判斷唾液酸修飾對(duì)其電荷異質(zhì)性的貢獻(xiàn),將羧肽酶B酶切后的抗體繼續(xù)用M糖苷酶酶切����,分析其電荷異質(zhì)性�����,結(jié)果顯示經(jīng)過(guò)2個(gè)酶切處理后抗體2的圖譜基本上只剩1個(gè)主峰��,證明抗體2的電荷異質(zhì)性主要是由C端賴氨酸的不均一性和唾液酸修飾所引起。
由于單抗制品高度復(fù)雜的異質(zhì)性其質(zhì)控需要組合多種理化分析技術(shù)對(duì)其進(jìn)行檢測(cè)如cIEF����、 IEX-HPLC��、 ICIEF�����、疏水高效液相色譜( HIC-HPLO)反相高效液相色譜(RP-HPLC)等方法�����,盡可能對(duì)不同電荷變異體組分進(jìn)行鑒別,并規(guī)定相應(yīng)的可接受標(biāo)準(zhǔn)��。成像毛細(xì)管等電聚焦電泳為對(duì)其進(jìn)行分析提供了一個(gè)快速��、靈敏����、高分離度的選擇,對(duì)保證單抗類生物技術(shù)藥物生產(chǎn)工藝的穩(wěn)定性及控制其質(zhì)量和提高質(zhì)量標(biāo)準(zhǔn)均具有重要意義�����。
4.2 雜質(zhì)分析
采用適宜的方法對(duì)供試品氧化產(chǎn)物��、脫酰胺產(chǎn)物或其他結(jié)構(gòu)不完整分子進(jìn)行定量分析����。采用適宜的方法對(duì)供試品宿主蛋白質(zhì)、宿主細(xì)胞和載體DNA����、蛋白A及其他工藝相關(guān)雜質(zhì)進(jìn)行檢測(cè)����。由于單克隆抗體人用劑量較大�����,基于方法學(xué)靈敏度考慮�����,目前殘余DNA檢測(cè)常用方法是定量PCR法����,樣品需要經(jīng)過(guò)前期抽提處理����,因此應(yīng)對(duì)抽提及定量PCR整個(gè)過(guò)程進(jìn)行方法學(xué)驗(yàn)證。重組抗體多由哺乳動(dòng)物細(xì)胞表達(dá)產(chǎn)生��,在抗體的純化過(guò)程中不可能將宿主細(xì)胞蛋白完全去除�����,殘留的異體蛋白進(jìn)入人體有可能引發(fā)免疫反應(yīng)��,故需對(duì)殘留蛋白量進(jìn)行限制����。宿主細(xì)胞蛋白殘留量檢測(cè)中��,除雜交法(WB�����、2DWB��、2 D-DIGE)和傅里葉轉(zhuǎn)換紅外光譜法外�����,ELSA方法是目前最常用的方法�����,其靈敏度高于上述兩種方法。
ELISA方法檢測(cè)HCP效率受所使用抗體對(duì)殘留HCP的覆蓋率的影響,而殘留FCP種類受生產(chǎn)細(xì)胞株����、細(xì)胞培養(yǎng)工藝和下游純化工藝等多種因素的影響。因此需要對(duì)商用試劑盒的適用性進(jìn)行方法學(xué)驗(yàn)證,并建議開(kāi)發(fā)工藝相關(guān)的HCP檢測(cè)方法�����。在蛋白A殘留量檢測(cè)中�����,對(duì)抗體進(jìn)行純化時(shí)會(huì)應(yīng)用蛋白A親和柱����,柱子型號(hào)不同�����,所用蛋白A也有差異�����,USP制備了包括原料在內(nèi)的4種不同類型的蛋白A標(biāo)準(zhǔn)物質(zhì):Natural Protein A46800, Recombinant Protein A44600Cys-rpA3430����, Mahselec SuRe26700。標(biāo)準(zhǔn)物質(zhì)的建立對(duì)蛋白A含量測(cè)定方法的標(biāo)準(zhǔn)化很有意義����。蛋白A測(cè)定方法多采用ELSA法:將蛋白A的特異性抗體包被96孔板,加入待測(cè)樣品及蛋白A標(biāo)準(zhǔn)溶液��,溶液中的蛋白A與包被抗體結(jié)合,洗滌后加入酶標(biāo)抗體�����,加底物顯色并測(cè)定吸光值,通過(guò)標(biāo)準(zhǔn)曲線法測(cè)定待測(cè)抗體溶液中的蛋白A含量��。
五、生物學(xué)活性
活性測(cè)定是對(duì)抗體類藥物的有效成分和含量及藥物效價(jià)的測(cè)定��,是確保藥物有效性的重要質(zhì)控指標(biāo)�����?����?贵w類藥物可通過(guò)其Fab段結(jié)合抗原發(fā)揮生物學(xué)效應(yīng)����,如大多數(shù)抗細(xì)胞因子類抗體藥物即是通過(guò)和細(xì)胞因子或其受體結(jié)合阻斷從而阻斷信號(hào)通路傳導(dǎo)����;也可通過(guò)Fc段發(fā)揮作用��,單抗藥物與靶細(xì)胞表面分子結(jié)合后,可介導(dǎo)補(bǔ)體clq結(jié)合到抗體的Fe段發(fā)揮補(bǔ)體依賴的細(xì)胞毒效應(yīng)( complement dependent cytotoxicity����,cDC),重組抗CD20����、CD52單抗即是通過(guò)測(cè)定免疫復(fù)合物活化補(bǔ)體產(chǎn)生細(xì)胞毒作用后B淋巴蜜細(xì)胞的死亡評(píng)價(jià)其生物學(xué)活性��;Fc段也可以通過(guò)和不同的FeR結(jié)合介導(dǎo)免疫效應(yīng)抗體依賴性細(xì)胞介導(dǎo)的細(xì)胞毒作用( antibody-dependent cell-mediated cytotoxicity�����,ADCC)和抗體依賴性細(xì)胞介導(dǎo)的吞噬作用( antibody-dependent cell-mediated phagocytosisADCP)����,如圖164所示��。ADCC和ADCP是許多針對(duì)腫蜜及自身免疫病的抗體類藥物重要作用機(jī)制之一��。
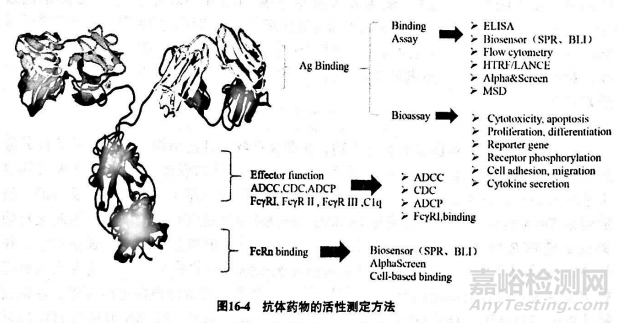
藥物的生物學(xué)活性測(cè)定主要是在體外建立相應(yīng)的細(xì)胞評(píng)價(jià)模型,模擬其作客觀的全程量效反應(yīng)�����,并通過(guò)與活性標(biāo)準(zhǔn)品的比較對(duì)其生物學(xué)活性進(jìn)行評(píng)價(jià)�����。近年來(lái),轉(zhuǎn)基因細(xì)胞技術(shù)和一些新技術(shù)也被應(yīng)用于抗體類藥物的生物學(xué)活性測(cè)定下文將對(duì)應(yīng)用于抗體藥物活性評(píng)價(jià)的傳統(tǒng)方法和前沿技術(shù)進(jìn)行簡(jiǎn)要介紹�����,為新型抗體藥物活性方法的建立提供新的思路。
5.1 基于細(xì)胞的生物學(xué)活性測(cè)定方法
隨著藥物高通量篩選平臺(tái)的建立和生產(chǎn)規(guī)模的擴(kuò)大,以及對(duì)“3R”( reduction��,refinement, replacement)原則理解的不斷深化��,人們?cè)絹?lái)越多地尋求動(dòng)物試驗(yàn)替代方法�����。而基于細(xì)胞系的體外生物活性分析方法����,由于其高通量、高效率��、高精確度等優(yōu)勢(shì)�����,越來(lái)越受到研究者和生產(chǎn)企業(yè)的青睞����。單克隆抗體藥物的作用靶點(diǎn)分為細(xì)胞因子及其受體����、腫瘤細(xì)胞表面抗原�����、CD分子��、病原微生物及其產(chǎn)物��、其他靶點(diǎn)����。根據(jù)抗體藥物作用的特點(diǎn),目前主要有以下幾類基于細(xì)胞的測(cè)活方法�����。
細(xì)胞增殖抑制法
針對(duì)生長(zhǎng)因子靶點(diǎn)的抗體藥物多是釆用細(xì)胞增殖抑制的方法來(lái)反映抗體的生物學(xué)活性��,包括抗血管內(nèi)皮生長(zhǎng)因子單抗�����、抗人表皮生長(zhǎng)因子受體2單抗及抗人表皮生長(zhǎng)因子受體單抗等��。其中��,抗VEGF單抗的經(jīng)典測(cè)活方法是人臍靜脈內(nèi)皮細(xì)胞增殖抑制法����,即在刺激因子EGF存在的情況下,抗ⅤEGF單抗能夠以劑量依賴性的方式抑制HVEC細(xì)胞的增殖�����。抗HER2單抗的活性測(cè)定通常選取HER2陽(yáng)性的乳腺癌細(xì)胞����,如BT474、SK-BR-3�����、SKOV3��、MCF-7等作為靶細(xì)胞��,抗體與靶細(xì)胞表面HER2抗原結(jié)合后����,能夠有效抑制細(xì)胞生長(zhǎng)信號(hào)傳遞,從而抑制細(xì)胞增殖����?�?笶GFR靶點(diǎn)單抗也是通過(guò)特異結(jié)合并封閉表皮生長(zhǎng)因子受體�����,有效抑制腫瘤細(xì)胞生長(zhǎng),如DFi細(xì)胞��、A431細(xì)胞增殖抑制法等����。
細(xì)胞毒性法
細(xì)胞凋亡有兩條途徑��,一是線粒體依賴途徑,另一個(gè)為死亡受體介導(dǎo)途徑����。腫瘤壞死因子a( tumor necrosis factor-alpha��,TNF-a)和受體結(jié)合后��,可啟動(dòng)死亡受體介導(dǎo)途徑,使 procaspe8自我水解��、活化,形成活性 caspase-8����,后者再激活 caspase3、6��、7等引起下面的級(jí)聯(lián)反應(yīng),導(dǎo)致細(xì)胞發(fā)生凋亡����。重組人Ⅱ型腫瘤壞死因子受體·抗體融合蛋白的活性測(cè)定可以利用其能夠抑制TNF-a所引起的敏感細(xì)胞系U937中 caspase3/活化,通過(guò) Caspase-Glo3/7檢測(cè)試劑盒中熒光素酶發(fā)光信號(hào)的改變來(lái)反映該制品的活性此外����,針對(duì)TNF-a的單抗還可以采用對(duì)TNF殺傷敏感的細(xì)胞系,如小鼠成纖維細(xì)胞L929����、小鼠纖維肉瘤細(xì)胞WEH64等����,抗體能夠抑制TNF-a所誘導(dǎo)的細(xì)胞凋亡作用通過(guò)檢測(cè)細(xì)胞存活的染色來(lái)評(píng)價(jià)抗體的生物學(xué)活性。
補(bǔ)體依賴的細(xì)胞毒法
單抗藥物與靶細(xì)胞表面分子結(jié)合后,可介導(dǎo)補(bǔ)體C1q結(jié)合到抗體的Fc段��,并于腫瘤細(xì)胞膜上形成類似于穿孔素效應(yīng)的攻膜復(fù)合體( membrane attack complex�����,MAC)造成細(xì)胞外離子大量?jī)?nèi)流����,最終導(dǎo)致腫蜜細(xì)胞的溶解��。CDC生物學(xué)活性測(cè)定中一個(gè)關(guān)鍵環(huán)節(jié)是補(bǔ)體的選擇及對(duì)其質(zhì)量的控制,補(bǔ)體組分多�����,且熱不穩(wěn)定��,容易失活,目前所用的補(bǔ)體來(lái)源包括正常人血清�����、豚鼠�����、家兔等�����,來(lái)源復(fù)雜�����、劑型不同,因此在CDC實(shí)驗(yàn)中需要考慮補(bǔ)體效力��、穩(wěn)定性��,盡量減少活性測(cè)定反應(yīng)終點(diǎn)和測(cè)定結(jié)果的變異����。以CD( cluster of differentiation)分子為靶點(diǎn)的單抗藥物�����,如抗CD20單抗�����、抗CD52單抗等,其生物學(xué)活性評(píng)價(jià)方法主要為CDC活性測(cè)定�����,即將重組抗體進(jìn)行系列稀釋后與高表達(dá)相應(yīng)CD抗原的靶細(xì)胞結(jié)合,在補(bǔ)體存在的情況下����,抗體與細(xì)胞表面抗原形成抗原-抗體復(fù)合物��,激活補(bǔ)體經(jīng)典活化途徑,完成攻膜復(fù)合物的裝配并在細(xì)胞表面打孔最終導(dǎo)致細(xì)胞溶解����。
ADCC和ADCP
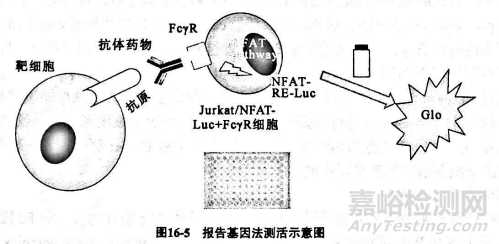
單抗藥物通過(guò)Fc段介導(dǎo)的抗體依賴性細(xì)胞介導(dǎo)的細(xì)胞毒作用(ADCC)和抗體依賴性細(xì)胞介導(dǎo)的吞噬作用(ADCP)的傳統(tǒng)檢測(cè)方法多為基于新鮮制備的外周血單個(gè)核細(xì)胞或者自然殺傷細(xì)胞作為效應(yīng)細(xì)胞的殺傷試驗(yàn),但以上方法存在細(xì)胞分離和培養(yǎng)困難����、變異大����、操作繁瑣、高背景值等缺陷����。近年來(lái)基于轉(zhuǎn)基因細(xì)胞法已建立了穩(wěn)定而可靠的ADCC和ADCP評(píng)價(jià)方法��。ADCC和ADCP報(bào)告基因法均使用工程改造的 Jurkat細(xì)胞作為效應(yīng)細(xì)胞����,分別穩(wěn)定表達(dá)了其效應(yīng)介導(dǎo)的主要受體FcRl和 CyrIlla����,以及由NFAT應(yīng)答元件驅(qū)動(dòng)表達(dá)的熒光素酶報(bào)告基因����。當(dāng)高表達(dá)抗原的靶細(xì)胞與表達(dá)FRa或FcRa的 Jurkat細(xì)胞通過(guò)單抗橋聯(lián)時(shí)����,可引起NFAT熒光素酶報(bào)告基因的活化,通過(guò)檢測(cè)熒光素酶化學(xué)發(fā)光信號(hào)來(lái)反映抗體的ADCC或ADCP效應(yīng)(圖16-5)��。該方法操作簡(jiǎn)便易行�����,專屬性強(qiáng)�����、重復(fù)性好�����、準(zhǔn)確性髙,通過(guò)選擇不同的靶細(xì)胞可作為抗CD20單抗����、抗HER2單抗��、抗EGFR單抗ADCC生物學(xué)活性的常規(guī)檢查方法��,用于評(píng)價(jià)包括人鼠嵌合單抗����、人源化單抗��、全人源單抗和糖基化改造單抗在內(nèi)的各類抗CD20單抗����、抗HER2單抗�����、抗EGFR單抗的ADCC活性;更重要的是�����,該方法可用于評(píng)價(jià)糖基化修飾與單抗Fc效應(yīng)功能的關(guān)系,這也為該類制品工藝穩(wěn)定性評(píng)價(jià)及結(jié)構(gòu)與功能關(guān)系評(píng)價(jià)奠定基礎(chǔ)��。
5.2 轉(zhuǎn)基因細(xì)胞生物學(xué)活性測(cè)定方法
轉(zhuǎn)基因細(xì)胞法為很多沒(méi)有強(qiáng)反應(yīng)性細(xì)胞系,或者沒(méi)有易檢測(cè)的細(xì)胞學(xué)效應(yīng)的生物技術(shù)藥物活性測(cè)定提供了選擇��。轉(zhuǎn)基因細(xì)胞法具有的實(shí)驗(yàn)周期短����、批間差異小等優(yōu)勢(shì)使其更能滿足藥物批間一致性和穩(wěn)定性的測(cè)定以及監(jiān)管的需要,因此��,轉(zhuǎn)基因細(xì)胞法逐漸成為生物技術(shù)藥物活性測(cè)定的趨勢(shì),一些傳統(tǒng)的生物學(xué)活性方法逐漸被轉(zhuǎn)基因細(xì)胞法所替代��。構(gòu)建轉(zhuǎn)基因細(xì)胞生物學(xué)活性測(cè)定法首先應(yīng)該全面深入地研究藥物的作用機(jī)制,包括受體激活����、信號(hào)轉(zhuǎn)導(dǎo)��、信號(hào)傳遞及終效應(yīng),然后�����,選擇合適的靶標(biāo)作為藥物活性測(cè)定的指標(biāo)�����。目前國(guó)內(nèi)在建立轉(zhuǎn)基因細(xì)胞法測(cè)定生物治療藥物生物學(xué)活性領(lǐng)域已走在世界的前列。中國(guó)食品藥品檢定研究院率先建立了干擾素測(cè)活的熒光素酶報(bào)告基因法�����,克服了國(guó)際通用的病毒抑制法中由操作活病毒導(dǎo)致的缺點(diǎn)����,使檢測(cè)周期縮短至原來(lái)的1/3,并最終納入《中國(guó)藥典》(2015版)三部��。將這一理念應(yīng)用于抗體藥物生物學(xué)活性的測(cè)定同樣取得了較好的成果��,不僅實(shí)現(xiàn)了傳統(tǒng)測(cè)活方法改進(jìn)的突破��,還解決了免疫檢查點(diǎn)等一類新藥生物活性測(cè)定的難題��。