今日頭條
長春金賽NK3R拮抗劑獲批婦科臨床���。金賽藥業(yè)1類化藥GS1-144片獲國家藥監(jiān)局臨床默示許可���,擬開發(fā)用于治療絕經(jīng)期血管舒縮癥狀。GS1-144是一款NK3R拮抗劑�����,可阻斷神經(jīng)激肽B(NKB)的信號通路�����,調(diào)控下視丘溫度調(diào)節(jié)中心的神經(jīng)活動(dòng),進(jìn)而降低中重度停經(jīng)血管舒縮癥狀的頻率與嚴(yán)重程度�����。目前中國尚無NK3R靶點(diǎn)藥物獲批上市��。
國內(nèi)藥訊
1.京新引進(jìn)地達(dá)西尼獲批上市�����。京新藥業(yè)從Evotec公司引進(jìn)的1類新藥地達(dá)西尼膠囊(EVT201)獲國家藥監(jiān)局批準(zhǔn)上市��,用于失眠障礙患者的短期治療���。EVT201是一款新型GABAa受體部分正向別構(gòu)調(diào)節(jié)劑(pPAM)�����,通過與α1-亞型結(jié)合導(dǎo)致GABAa受體的變構(gòu)調(diào)節(jié)而中度激活該受體并導(dǎo)致下游信號轉(zhuǎn)導(dǎo)�����,從而抑制中樞神經(jīng)系統(tǒng)�����,發(fā)生睡眠作用��。京新藥業(yè)擁有EVT201在中國區(qū)域的獨(dú)家權(quán)益��。
2.藥明巨諾CD19靶向CAR-T擬納入優(yōu)先審評��。藥明巨諾靶向CD19的CAR-T產(chǎn)品瑞基奧侖賽注射液獲國家藥監(jiān)局?jǐn)M納入優(yōu)先審評��,用于治療成人復(fù)發(fā)或難治性套細(xì)胞淋巴瘤(MCL)���。在Ⅱ期臨床中�����,瑞基奧侖賽治療達(dá)到81.8%的客觀緩解率。該產(chǎn)品此前已獲NMPA批準(zhǔn)兩項(xiàng)適應(yīng)癥��,用于治療既往接受二線或以上治療的復(fù)發(fā)或難治性大B細(xì)胞淋巴瘤(r/r LBCL)���,以及治療經(jīng)過二線或以上系統(tǒng)性治療的濾泡性淋巴瘤(r/r FL)���。
3.奧賽康CLDN18.2單抗啟動(dòng)胃癌Ⅲ期臨床���。奧賽康藥業(yè)靶向CLDN18.2的單抗藥物ASKB589注射液登記啟動(dòng)一項(xiàng)Ⅲ期臨床,評估ASKB589或安慰劑聯(lián)合CAPOX(奧沙利鉑和卡培他濱)及PD-1抑制劑一線治療CLDN18.2陽性的不可切除的局部晚期�����、復(fù)發(fā)性或轉(zhuǎn)移性胃及食管胃交界處腺癌患者的有效性和安全性���。該項(xiàng)試驗(yàn)的主要研究者為北京腫瘤醫(yī)院醫(yī)學(xué)博士沈琳�����。在Ⅱ期臨床中���,ASKB589聯(lián)合CAPOX治療的客觀緩解率達(dá)到79.2%。
4.正大天晴ATR激酶抑制劑獲批臨床���。正大天晴1類化藥TQB3015片獲國家藥監(jiān)局臨床試驗(yàn)?zāi)驹S可�����,擬開發(fā)用于治療晚期惡性腫瘤��。TQB3015是一款A(yù)TR激酶抑制劑���,通過抑制細(xì)胞周期檢測點(diǎn)激酶CHK1的磷酸化�����,觸發(fā)細(xì)胞周期阻滯��,并抑制由ATR激酶介導(dǎo)的修復(fù)通路���,從而阻斷腫瘤細(xì)胞的DNA損傷應(yīng)答,達(dá)到“合成致死”的效果��。在臨床前研究中��,TQB3015單藥以及聯(lián)合用藥均顯示出積極的抗腫瘤活性���。
5.威溶特溶瘤病毒國內(nèi)獲批臨床��。廣州威溶特醫(yī)藥1類生物藥注射用重組溶瘤病毒M1(VRT106)獲國家藥監(jiān)局臨床許可���,擬用于局部晚期/轉(zhuǎn)移性實(shí)體瘤的治療���。VRT106是一款基于甲病毒M1骨架的溶瘤病毒產(chǎn)品�����,比傳統(tǒng)的放化療方法有更好的安全性和耐受性���。在美國���,F(xiàn)DA已授予VRT106用于治療“肝癌”和“惡性膠質(zhì)瘤”的孤兒藥資格認(rèn)定。
6.默沙東IL-2激動(dòng)劑中國報(bào)IND��。默沙東1類生物制品MK-6194注射液(PT101)的臨床試驗(yàn)申請獲CDE受理�����。PT101是一款選擇性IL-2激動(dòng)劑�����,能夠選擇性與Tregs表面包含IL-2Ra亞基的IL-2受體三聚體結(jié)合���,從而特異性激活和擴(kuò)增Tregs�����,擬用于治療自身免疫性疾病��。目前���,該產(chǎn)品正在Ⅰ期臨床中用于治療中重度特應(yīng)性皮炎患者��,以及在Ⅱ期臨床中評估治療非節(jié)段性白癜風(fēng)患者的效果�����。
國際藥訊
1.Autolus公司CD19靶向CAR-T報(bào)BLA��。Autolus公司已向FDA提交其靶向CD19的CAR-T療法obecabtagene autoleucel(obe-cel)的生物制品許可申請(BLA)���,用于治療復(fù)發(fā)/難治性成人B細(xì)胞急性淋巴細(xì)胞白血病(B-ALL)患者。在Ⅱ期臨床FELIX中�����,obe-cel的總緩解率達(dá)到76%��;中位隨訪為9.5個(gè)月時(shí)�����,61%獲得緩解的患者在沒有接受新抗癌療法治療的情況下仍然維持緩解。預(yù)計(jì)明年上半年向歐洲藥品管理局(EMA)提交上市申請�����。
2.89bio公司NASH新藥長期療效積極���。89bio公司FGF21類似物pegozafermin治療非酒精性脂肪性肝炎(NASH)的Ⅱb期ENLIVEN試驗(yàn)擴(kuò)展研究積極。該試驗(yàn)此前已達(dá)到主要終點(diǎn)��,pegozafermin(44mg Q2W和30mg QW)治療在第24周時(shí)顯著提高達(dá)成至少一個(gè)階段的纖維化改善且NASH癥狀沒有惡化的患者比例(27%和26%�����,vs安慰劑為7%)��。48周數(shù)據(jù)顯示�����,pegozafermin治療均顯著的持續(xù)改善肝脂肪和非侵入性檢測(NIT)的肝損傷/炎癥和纖維化標(biāo)志物指標(biāo)��。pegofermin的安全性與之前數(shù)據(jù)一致��。
3.默沙東21價(jià)肺炎球菌疫苗Ⅲ期試驗(yàn)積極�����。默沙東21價(jià)肺炎球菌結(jié)合疫苗V116用于既往未接種肺炎球菌疫苗的成人接種的Ⅲ期試驗(yàn)STRIDE-3結(jié)果積極。與活性對照疫苗PCV20(肺炎球菌20價(jià)結(jié)合疫苗)相比��,V116對于兩種疫苗中共有的所有10種血清型中引起的免疫應(yīng)答達(dá)到非劣效性標(biāo)準(zhǔn)��;V116特有的11種血清型中有10種展現(xiàn)良好的免疫應(yīng)答�����;V116在50-64歲和18-49歲兩隊(duì)列中引起的免疫應(yīng)答呈現(xiàn)非劣效性���。V116的安全性與活性對照組相當(dāng)�����。
4.Immunovant創(chuàng)新FcRn抗體Ⅰ期臨床積極��。Immunovant公司差異化設(shè)計(jì)的FcRn抗體IMVT-1402在健康成人中開展的Ⅰ期臨床結(jié)果積極。初步數(shù)據(jù)顯示���,IMVT-1402可以劑量依賴性地顯著降低IgG�����,但不會影響白蛋白與LDL���。IMVT-1402(600mg)劑量組可將IgG降低高達(dá)80%�����,與巴托利單抗降低IgG的歷史數(shù)據(jù)類似���。此外,IMVT-1402具有良好的安全性�����,無嚴(yán)重治療伴發(fā)不良事件(TEAE)報(bào)告���。
5.禮來與PRISM合作開發(fā)PPI小分子抑制劑���。禮來與PRISM BioLab公司將利用后者專有的PepMetics技術(shù)平臺,針對禮來選擇的蛋白-蛋白相互作用(PPI)靶點(diǎn)�����,合作開發(fā)小分子抑制劑���。PepMetics是一類模仿α-螺旋和β-轉(zhuǎn)角3D結(jié)構(gòu)的小分子��,是胞內(nèi)PPI細(xì)胞間期和受體-配體相互作用中常見的多肽結(jié)構(gòu)。根據(jù)協(xié)議��,PRISM將獲得預(yù)付款��、高達(dá)6.6億美元的臨床前���、臨床和商業(yè)開發(fā)里程碑后期付款,以及產(chǎn)品的銷售分成��。
6.BMS布局抗體寡核苷酸偶聯(lián)藥物��。百時(shí)美施貴寶與Avidity Biosciences將利用后者專有的抗體寡核苷酸偶聯(lián)物(AOC)平臺��,針對多個(gè)心血管靶點(diǎn)合作開發(fā)AOC候選藥物�����。根據(jù)協(xié)議���,Avidity將獲得1億美元的預(yù)付款,高達(dá)13.5億美元的研發(fā)里程碑后期款項(xiàng)��,以及高達(dá)8.25億美元的商業(yè)里程碑付款�����。百時(shí)美施貴寶將負(fù)責(zé)候選產(chǎn)品的臨床開發(fā)���、監(jiān)管和商業(yè)化活動(dòng)�����。
醫(yī)藥熱點(diǎn)
1.南京鼓樓醫(yī)院心腦血管病醫(yī)院揭牌成立��。11月27日���,南京鼓樓醫(yī)院心腦血管病醫(yī)院揭牌成立儀式在南京鼓樓醫(yī)院南部院區(qū)舉行。今年9月22日��,南京鼓樓醫(yī)院南部院區(qū)正式啟用,設(shè)置700張床位���,與院本部實(shí)行“同質(zhì)化管理、同水平醫(yī)療���、同標(biāo)準(zhǔn)服務(wù)”���。南京鼓樓醫(yī)院將南部院區(qū)聚力打造成為以心腦血管疾病為特色、科室建設(shè)較為齊全的“強(qiáng)?��??��、優(yōu)綜合”三級甲等醫(yī)院,目前神經(jīng)內(nèi)科�����、神經(jīng)外科���、心血管內(nèi)科、心臟外科和血管外科等科室已陸續(xù)進(jìn)駐南部院區(qū)���。
2.CDE增設(shè)對外受理服務(wù)窗口��。11月29日�����,CDE發(fā)布通知�����,從2023年12月1日起��,CDE在藥品審評檢查長三角分中心�����、大灣區(qū)分中心增設(shè)對外受理服務(wù)窗口。申報(bào)資料遞交方式及地點(diǎn)不變���,仍由國家藥監(jiān)局藥審中心統(tǒng)一接收���。藥品長三角分中心向長三角區(qū)域內(nèi)(上海市��、江蘇省、浙江省和安徽?�。┧幤纷陨暾埲颂峁┦芾矸?wù)�����;藥品大灣區(qū)分中心向大灣區(qū)區(qū)域內(nèi)(香港特別行政區(qū)���、澳門特別行政區(qū)、廣州市��、深圳市���、珠海市���、佛山市��、惠州市�����、東莞市�����、中山市���、江門市�����、肇慶市)藥品注冊申請人提供受理服務(wù)���。
3.江西將電子耳蝸植入術(shù)等192個(gè)項(xiàng)目納入醫(yī)保��。江西省醫(yī)療保障局印發(fā)的《江西省基本醫(yī)療保險(xiǎn)醫(yī)療服務(wù)項(xiàng)目支付管理目錄(2023年)》將于12月1日零時(shí)起正式執(zhí)行�����。該目錄將“電子耳蝸植入術(shù)”等192個(gè)新增申報(bào)醫(yī)療服務(wù)項(xiàng)目動(dòng)態(tài)評審納入醫(yī)保支付范圍。江西本次通過“提質(zhì)擴(kuò)面”�����,共將4369項(xiàng)醫(yī)療服務(wù)項(xiàng)目納入省醫(yī)保支付范圍�����。
評審動(dòng)態(tài)
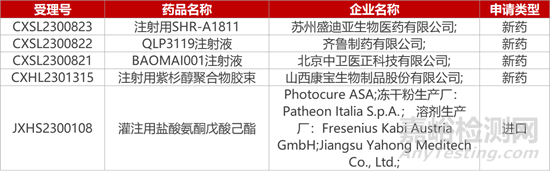
1. CDE新藥受理情況(11月29日)
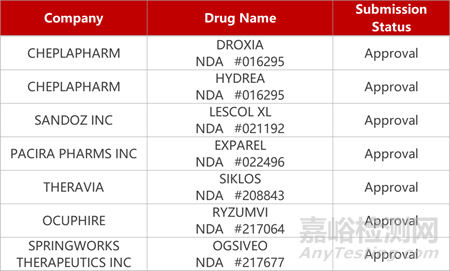
2. FDA新藥獲批情況(北美11月28日)