剛剛,上海市器審中心發(fā)布了《動(dòng)物源性人工心臟瓣膜(外科瓣)生產(chǎn)環(huán)節(jié)風(fēng)險(xiǎn)清單和檢查指南》�����,內(nèi)容如下:
動(dòng)物源性人工心臟瓣膜(外科瓣)生產(chǎn)環(huán)節(jié)風(fēng)險(xiǎn)清單和檢查指南
本指南旨在指導(dǎo)和規(guī)范動(dòng)物源性人工心臟瓣膜(外科瓣)產(chǎn)品的現(xiàn)場(chǎng)核查工作,幫助醫(yī)療器械檢查員把握該類產(chǎn)品風(fēng)險(xiǎn)及核查要求�����,統(tǒng)一核查尺度�����,同時(shí)也為注冊(cè)申請(qǐng)人建立及運(yùn)行質(zhì)量管理體系的工作提供參考�����。
本指南在《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范》及無菌和植入附錄的基礎(chǔ)上,參考動(dòng)物源性醫(yī)療器械監(jiān)管要求和相關(guān)國(guó)家標(biāo)準(zhǔn)和行業(yè)標(biāo)準(zhǔn)�����,對(duì)動(dòng)物源性人工心臟瓣膜開展現(xiàn)場(chǎng)檢查提出指導(dǎo)性要求�����,旨在識(shí)別和關(guān)注該類產(chǎn)品實(shí)現(xiàn)過程中的風(fēng)險(xiǎn)點(diǎn)和要點(diǎn),供檢查員及注冊(cè)申請(qǐng)人參考使用�����,幫助有關(guān)人員系統(tǒng)梳理該類產(chǎn)品生產(chǎn)控制過程中的風(fēng)險(xiǎn)要點(diǎn)�����,不作為法規(guī)強(qiáng)制執(zhí)行�����。注冊(cè)申請(qǐng)人應(yīng)依據(jù)申報(bào)產(chǎn)品的具體特點(diǎn)�����,遵循相關(guān)法規(guī)要求建立質(zhì)量管理體系并保持有效運(yùn)行�����。本指南是在現(xiàn)行法規(guī)和標(biāo)準(zhǔn)體系以及當(dāng)前科技認(rèn)知水平和現(xiàn)有產(chǎn)品技術(shù)基礎(chǔ)上形成的,隨著法規(guī)和標(biāo)準(zhǔn)的不斷完善�����、科學(xué)技術(shù)的不斷發(fā)展�����,相關(guān)人員參考時(shí)應(yīng)注意其適宜性�����,密切關(guān)注適用標(biāo)準(zhǔn)及相關(guān)技術(shù)的最新進(jìn)展,考慮產(chǎn)品的更新和變化�����。隨著對(duì)產(chǎn)品理解的不斷深入�����,本指南相關(guān)內(nèi)容也將適時(shí)進(jìn)行調(diào)整。
一�����、動(dòng)物源性人工心臟瓣膜產(chǎn)品和生產(chǎn)信息
(一) 產(chǎn)品簡(jiǎn)介
1. 概述
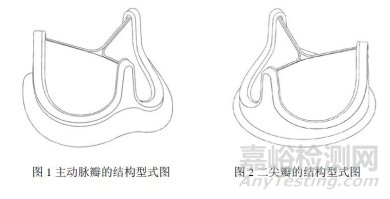
動(dòng)物源性人工心臟瓣膜是可植入人體心臟內(nèi)替代心臟瓣膜�����,能使血液?jiǎn)蜗蛄鲃?dòng)不發(fā)生返流,具有天然心臟瓣膜功能的醫(yī)療器械�����。通過設(shè)計(jì)不同的縫環(huán)形狀來適應(yīng)臨床上的不同瓣環(huán)位置的解剖形狀�����,瓣膜可以區(qū)分為兩大類:主動(dòng)脈瓣和二尖瓣,其形式如圖 1�����、圖 2 所示:
2. 結(jié)構(gòu)組成
動(dòng)物源性人工心臟瓣膜是一種帶支架的生物假體,通常以牛心包或豬主動(dòng)脈瓣為瓣葉原材料�����,經(jīng)前期處理�����、化學(xué)交聯(lián)處理、激光切割/剪裁后被縫制在滌綸布包裹的合金支架上�����,主要用于置換體內(nèi)病變的瓣膜�����。主要由四部分組成:瓣架�����、瓣葉、瓣座和縫環(huán)�����,用縫線連接固定�����。最終產(chǎn)品經(jīng)戊二醛滅菌后被保存在該溶液中。
瓣架是一種由具有耐腐蝕性的鈷-鉻-錳-鐵合金制成�����,被聚酯織物包裹�����,能提供優(yōu)異的彈性和疲勞耐久性�����。
瓣葉是由牛心包組織或豬主動(dòng)脈瓣經(jīng)戊二醛交聯(lián)后再由激光切割整形而得。瓣座是瓣架及連接縫環(huán)的支撐結(jié)構(gòu)�����,由 PET 薄膜內(nèi)外襯衣及鈷-鉻-錳-鐵合金組成,被滌綸布包裹�����?����?p環(huán)是由被滌綸布包裹的襯環(huán)�����,布的表面有 3 道黑色標(biāo)記用于臨床植入時(shí)的定位。持瓣器的設(shè)計(jì)用于外科醫(yī)生植入瓣膜和觀察瓣葉的打開和關(guān)閉�����。瓣膜假體通過縫合固定在瓣膜持瓣器上�����,而瓣膜持瓣器固定在由蓋板和套筒組成的瓣膜保護(hù)裝置上。
3. 預(yù)期用途
動(dòng)物源性人工心臟瓣膜假體旨在用于患有瓣膜性心臟病的患者�����,并且不能通過原瓣膜修復(fù)技術(shù)愈合,而只是更換�����。它僅供醫(yī)療機(jī)構(gòu)用于患心臟瓣膜病的臨床瓣膜置換手術(shù)�����。
3.1 適用于心臟瓣膜?����。ㄖ鲃?dòng)脈瓣或二尖瓣)心臟患者。包括心臟瓣膜障礙或狹窄�����、瓣膜泄漏�����、返流�����、關(guān)閉不全�����、或功能性不全或兩者兼有�����,有時(shí)也被稱為混合性疾病或合并病變。3.2 適用于先天性畸形�����、各類微生物感染�����、退行性鈣化、風(fēng)濕性心臟病所致的瓣膜疾病�����,尤其是對(duì)長(zhǎng)期抗凝治療有禁忌或難以維持抗凝治療的患者�����。
3.3 適用于無法通過修復(fù)得到治愈的瓣膜疾病患者�����,并且適宜采用假體瓣膜替換自體瓣膜的瓣膜疾病患者;或者已經(jīng)植入過人工心臟瓣膜的但其性能已經(jīng)衰敗需要更換瓣膜的患者�����。在后一種情況下,先前植入的假體通過外科手術(shù)切除并由替換假體代替�����。瓣膜可以進(jìn)行瓣環(huán)上或瓣環(huán)內(nèi)植入�����。
4. 規(guī)格型號(hào)
在對(duì)臨床應(yīng)用現(xiàn)狀進(jìn)行調(diào)查后,心臟瓣膜假體可分為兩個(gè)型號(hào):主動(dòng)脈瓣假體和二尖瓣假體�����,分別在支架直徑�����、縫環(huán)外徑、高度等指標(biāo)存在尺寸差異�����。 其規(guī)格尺寸應(yīng)具體參照各企業(yè)的產(chǎn)品技術(shù)要求�����。5. 產(chǎn)品性能
動(dòng)物源性人工心臟瓣膜假體通過同時(shí)打開和關(guān)閉三片瓣葉,使血液從心房向心室�����、動(dòng)脈單向流動(dòng)而不發(fā)生返流�����。
產(chǎn)品的物理和化學(xué)性能應(yīng)符合 GB 12279-2008 《心血管植入物 – 人工心臟瓣膜》(ENISO5840:1996)中規(guī)定的要求。
產(chǎn)品的生物學(xué)性能符合 GB/T 16886.1 《醫(yī)療器械生物學(xué)評(píng)價(jià) 第 1 部分:風(fēng)險(xiǎn)管理過程中的評(píng)價(jià)與試
驗(yàn)》 中規(guī)定�����,例如體外細(xì)胞毒性試驗(yàn)、致敏性�����、皮內(nèi)刺激�����、急性系統(tǒng)毒性�����、亞慢性毒性�����、遺傳毒性�����、植入試驗(yàn)�����、血液相容性、熱原等�����。具體要求應(yīng)參照各企業(yè)產(chǎn)品技術(shù)要求�����。
(二)參考文獻(xiàn)
GB 12279 心血管植入物 人工心臟瓣膜
GB 18278 醫(yī)療保健產(chǎn)品的滅菌 確認(rèn)和常規(guī)控制要求 工業(yè)濕熱滅菌
GB 18279 醫(yī)療器械 環(huán)氧乙烷滅菌 確認(rèn)和常規(guī)控制
GB 18280 醫(yī)療保健產(chǎn)品的滅菌 確認(rèn)和常規(guī)控制要求 輻射滅菌
GB 8369 一次性使用輸血器
GB 19335 一次性使用血路產(chǎn)品通用技術(shù)條件
GB/T 19633 最終滅菌醫(yī)療器械的包裝》
GB/T16886.1 醫(yī)療器械生物學(xué)評(píng)價(jià) 第 1 部分:評(píng)價(jià)與試驗(yàn)
GB/T16886.3 醫(yī)療器械生物學(xué)評(píng)價(jià) 第 6 部分:遺傳毒性、致癌性和生殖毒性試驗(yàn)GB/T16886.4 醫(yī)療器械生物學(xué)評(píng)價(jià) 第 10 部分:與血液相互作用試驗(yàn)選擇
GB/T16886.5 醫(yī)療器械生物學(xué)評(píng)價(jià) 第 5 部分:體外細(xì)胞毒性試驗(yàn)
GB/T16886.6 醫(yī)療器械生物學(xué)評(píng)價(jià) 第 6 部分:植入后局部反應(yīng)試驗(yàn)
GB/T16886.10 醫(yī)療器械生物學(xué)評(píng)價(jià) 第 10 部分:刺激與致敏性試驗(yàn)
GB/T16886.11 醫(yī)療器械生物學(xué)評(píng)價(jià) 第 11 部分:全身毒性試驗(yàn)
GB/T14233.1 醫(yī)用輸液�����、輸血、注射器局檢驗(yàn)方法第 1 部分:化學(xué)分析法
GB/T14233.2 醫(yī)用輸液�����、輸血�����、注射器局檢驗(yàn)方法第 2 部分:生物學(xué)試驗(yàn)方法GB/T19633-1 最終滅菌醫(yī)療器械包裝 第 1 部分:材料、無菌屏障系統(tǒng)和包裝系統(tǒng)的要求GB/T19633.2 最終滅菌醫(yī)療器械包裝 第 2 部分:成形�����、密封盒裝配過程的確認(rèn)的要求GB/T 2828.1 計(jì)數(shù)抽樣檢驗(yàn)程序第 1 部分:按接收質(zhì)量限(AQL)檢索的逐批檢驗(yàn)抽樣計(jì)劃GB/T 2829 周期檢查技術(shù)抽樣程序及表(適用于過程穩(wěn)定性的檢查)
GB/T 9969 工業(yè)產(chǎn)品使用說明書總則
YY 0970 含動(dòng)物源材料的一次性使用醫(yī)療器械的滅菌液體滅菌劑滅菌的確認(rèn)與常規(guī)控制YY 0167 非吸收性外科縫線
YY 0605.7 外科植入物金屬材料第 7 部分可鍛和冷加工的鈷鉻鎳鉬鐵合金
YY/T 0771.1《動(dòng)物源醫(yī)療器械 第 1 部分:風(fēng)險(xiǎn)管理應(yīng)用》
YY/T 0771.2《動(dòng)物源醫(yī)療器械 第 2 部分:來源、收集與處置的控制》
YY/T 0771.3《動(dòng)物源醫(yī)療器械 第 3 部分:病毒和傳播性海綿狀腦?����。═SE)因子去除與滅活的確認(rèn)》YY/T 0771.4《動(dòng)物源醫(yī)療器械 第 4 部分:TSE 因子去除與滅活原則及其驗(yàn)證試驗(yàn)》YY/T 0606.17 組織工程醫(yī)療產(chǎn)品:外源因子評(píng)價(jià)指南
YY/T0606.16 組織工程醫(yī)療產(chǎn)品:保存指南[S]
YY/T 0567 醫(yī)療產(chǎn)品的無菌加工
YY/T 0316 (GB/T 42062) 醫(yī)療器械 風(fēng)險(xiǎn)管理對(duì)醫(yī)療器械的應(yīng)用
YY/T 0313 醫(yī)用高分子制品包裝�����、標(biāo)簽�����、運(yùn)輸和貯存
YY/T 0287 (GB/T 42061) 醫(yī)療器械 質(zhì)量管理體系用于法規(guī)的要求
YY/T 0033 無菌醫(yī)療器具生產(chǎn)管理規(guī)范
YY/T 0606.25《組織工程醫(yī)療產(chǎn)品 第 25 部分:動(dòng)物源性生物材料 DNA 殘留量測(cè)定法:熒光染色法》中華人民共和國(guó)藥典(2020 版第四部)
國(guó)藥監(jiān)注[2002]160 號(hào) 關(guān)于印發(fā)《血液制品去除/滅活病毒技術(shù)方法及驗(yàn)證指導(dǎo)原則》的通知食品藥品監(jiān)管總局關(guān)于發(fā)布動(dòng)物源性醫(yī)療器械注冊(cè)技術(shù)審查指導(dǎo)原則(2017 年修訂版)的通告(2017年第 224 號(hào))
ISO 22442《醫(yī)療器械生產(chǎn)用動(dòng)物組織及其衍生物》
ENISO14971 Medical devices – Application of risk management to medical devices
ENISO5840-2 Cardiovascular implants-cardiac valve prostheses Part 2 Surgically implantedheartvalve substitutes
ENISO10993.1 Biological evaluation of medical devices – Part 1: Evaluation and testingwithina risk management process
ENISO22442-1 Medial device utilizing animal tissues and their derivatives-Part1: Applicationof risk management
ENISO22442-2 Medial device utilizing animal tissues and their derivatives-Part2: Controlsonsourcing, collection and handling
ENISO22442-3 Medial device utilizing animal tissues and their derivatives-Part3: Validationofthe elimination and /or inactivation of viruses and transmissible spongiform encephalopathy(TSE)agents
ENISO11607-1 Packaging for terminally sterilized medical devices – Part 1: Requirementsformaterial, sterile barrier systems and packaging systems
ENISO11607-2 Packaging for terminally sterilized medical devices – Part2: Validationrequirements for forming, sealing and assembly processes
Council Directive 93/42/EEC
Directive 2007/47/EC
(三)生產(chǎn)信息
1.工藝流程示例(以應(yīng)用較為普遍的牛心包為示例)1.1 瓣膜主體:牛心包成形處理�����、瓣葉制作、合金絲制作�����、滌綸包布制作�����、瓣架縫制;1.2 帶環(huán)支架:縫環(huán)制作�����、瓣座縫制、帶環(huán)支架縫制�����;
1.3 組裝:帶環(huán)支架�����、瓣膜主體�����、瓣膜包布組合形成;
1.4 初包裝�����、滅菌
2. 關(guān)鍵原材料(以應(yīng)用較為普遍的牛心包為例,各企業(yè)可能存在差異)2.1 瓣膜:建議采用非疫源地來源的低齡牛的心包�����,如果是新鮮牛心包,應(yīng)在儲(chǔ)存液中應(yīng)嚴(yán)格控制在0-10℃�����,從取材到運(yùn)抵備用不應(yīng)超過 72 小時(shí)�����;如果是已交聯(lián)合格的牛心包取材后應(yīng)在抑菌液中儲(chǔ)存運(yùn)輸,無熱缺血時(shí)效性限制�����。如果選用豬主動(dòng)脈瓣應(yīng)取自成年豬的新鮮瓣膜�����,熱缺血時(shí)間則應(yīng)不超過2 小時(shí)�����。原材料應(yīng)具有可追溯性�����。應(yīng)能提供牛飼養(yǎng)人/場(chǎng)�����、屠宰場(chǎng)、牛心包供應(yīng)商�����、瓣膜生產(chǎn)企業(yè)等相關(guān)信息(例如但不限于:出口國(guó)賣方聲明�����、動(dòng)物屠宰記錄、牛心包材料符合性聲明�����、牛心包產(chǎn)地證明�����、動(dòng)物檢疫證明�����、原材料進(jìn)貨檢驗(yàn)記錄等�����。
2.2 合金絲:較常用 Elgiloy 合金
2.3 包布:較常用滌綸布
2.4 縫線:較常用非吸收外科縫線
2.5 內(nèi)襯:較常用聚對(duì)苯二甲酸乙二醇酯(PET)
2.6 交聯(lián)劑:較常用戊二醛溶液
2.7 滅菌:較常用戊二醛液體滅菌
3.關(guān)鍵過程和特殊過程(以應(yīng)用較為普遍的牛心包為示例)3.1 關(guān)鍵過程:瓣膜成型�����、瓣架縫制、半成品縫制作
3.2 特殊過程:交聯(lián)處理�����、瓣葉滅活�����、清洗�����、初包裝、滅菌
4.質(zhì)量控制點(diǎn)(以應(yīng)用較為普遍的牛心包為示例)4.1 縫合質(zhì)量:按過程檢驗(yàn)規(guī)程執(zhí)行
4.2 流量測(cè)試:按產(chǎn)品技術(shù)要求執(zhí)行
4.3 成品檢驗(yàn):按逐批檢驗(yàn)規(guī)程執(zhí)行
二�����、動(dòng)物源性人工心臟瓣膜風(fēng)風(fēng)險(xiǎn)管理示例(以應(yīng)用較為普遍的牛心包人工心臟瓣膜為例)
1.確立風(fēng)險(xiǎn)可接受標(biāo)準(zhǔn)
為風(fēng)險(xiǎn)管理制定的風(fēng)險(xiǎn)可接受標(biāo)準(zhǔn)如下所示�����。 用半定量分析法計(jì)算損害概率�����,用定性分析法分析損害的嚴(yán)重程度�����。風(fēng)險(xiǎn)可接受性標(biāo)準(zhǔn)用 5×5 矩陣圖表示。
1.1 損害的概率分級(jí)
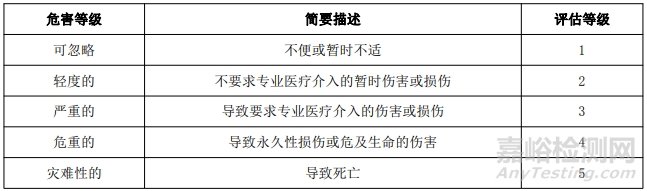
1.2 損害的嚴(yán)重度水平
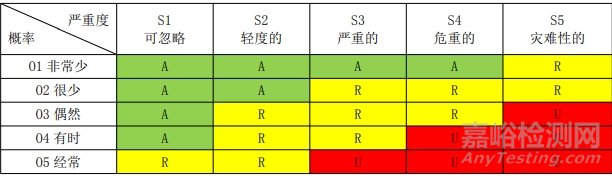
1.3 風(fēng)險(xiǎn)可接受標(biāo)準(zhǔn)
說明:A:可接受的風(fēng)險(xiǎn)�����;R:研究進(jìn)一步降低風(fēng)險(xiǎn);U:不可接受的風(fēng)險(xiǎn)
1.4 風(fēng)險(xiǎn)可接受標(biāo)準(zhǔn)系數(shù)值分析
根據(jù)上述風(fēng)險(xiǎn)可接受標(biāo)準(zhǔn)所構(gòu)成的風(fēng)險(xiǎn)評(píng)價(jià)矩陣圖�����,確定風(fēng)險(xiǎn)可接受區(qū)域�����。? 風(fēng)險(xiǎn)系數(shù)RPN:RPN = 概率×嚴(yán)重程度
可接受區(qū)A:RPN≤4�����,該區(qū)域內(nèi)�����,風(fēng)險(xiǎn)是可以接受的。
進(jìn)一步降低風(fēng)險(xiǎn)區(qū)R:4<RPN≤14 該區(qū)域內(nèi)的風(fēng)險(xiǎn)既不是可忽略的也不是不可接受的�����,應(yīng)盡可能地消除或降低風(fēng)險(xiǎn)�����。
注:此風(fēng)險(xiǎn)降低概念不應(yīng)包含經(jīng)濟(jì)考慮因素�����。
不可接受的區(qū)域“U”:RPN> 14 ? 該區(qū)域內(nèi),風(fēng)險(xiǎn)如果不能予以降低�����,則判斷為是不可接受的
1.5 初始危害分析
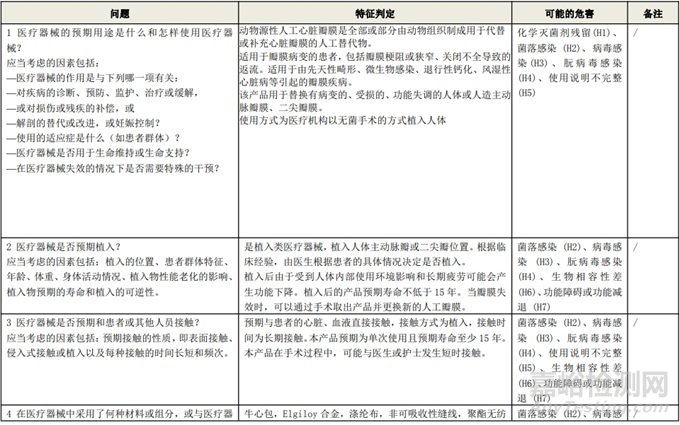
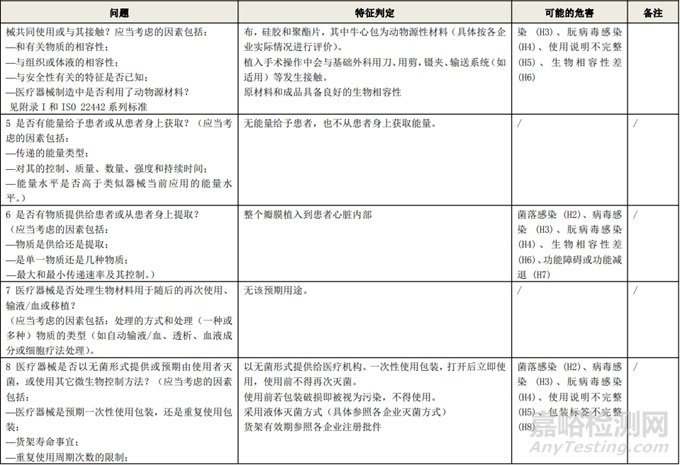
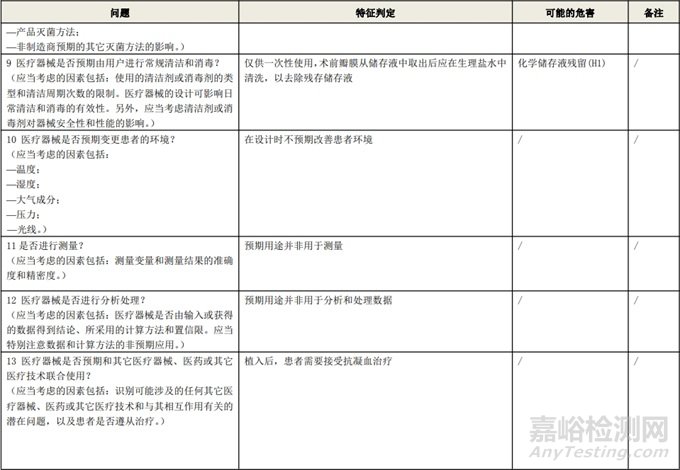
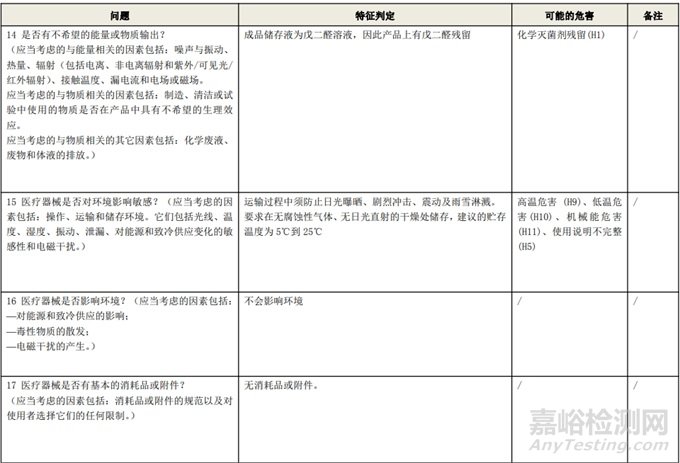
根據(jù)風(fēng)險(xiǎn)管理計(jì)劃和YY/T 0316-2016 《醫(yī)療器械 風(fēng)險(xiǎn)管理對(duì)醫(yī)療器械的應(yīng)用》(ENISO14971-2012)附錄C對(duì)預(yù)期用途和安全相關(guān)特征進(jìn)行了評(píng)估,詳見附表1《動(dòng)物源性人工心臟瓣膜安全性特征清單》(以應(yīng)用較為普遍的牛心包材料制成品為示例)所示�����。
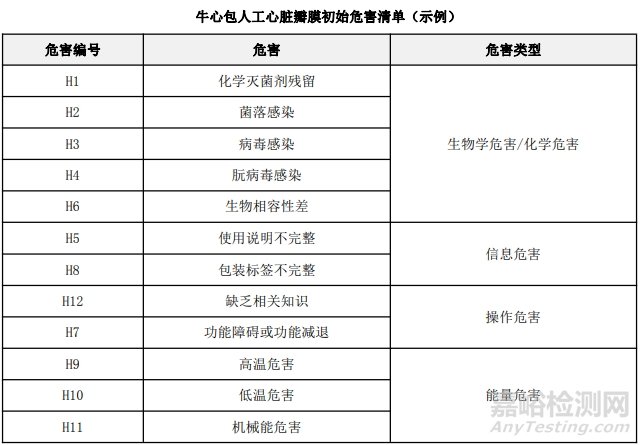
通過填寫安全特征檢查清單�����,對(duì)動(dòng)物源性人工心臟瓣膜的安全特征有了初步的了解�����,并識(shí)別出了初始的危害共計(jì)12個(gè)�����,如下表所示,并分別對(duì)這些危害進(jìn)行了風(fēng)險(xiǎn)分析�����,詳見附表2《牛心包人工心臟瓣膜初始危害分析表(示例)》(以應(yīng)用較為普遍的牛心包材料制成品為示例)�����。
2.風(fēng)險(xiǎn)控制措施
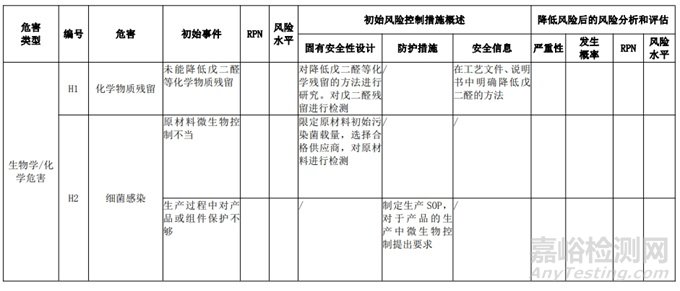
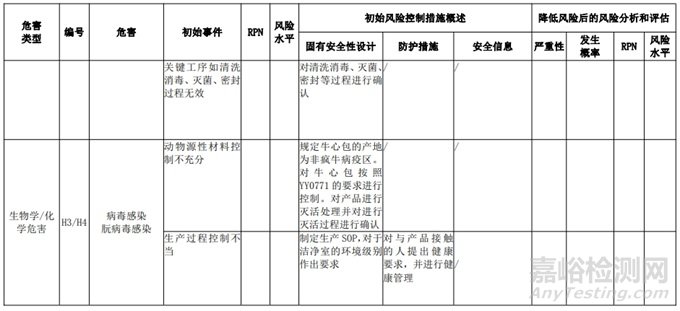
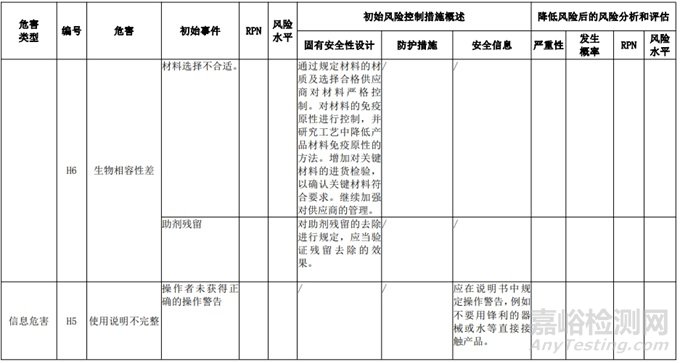
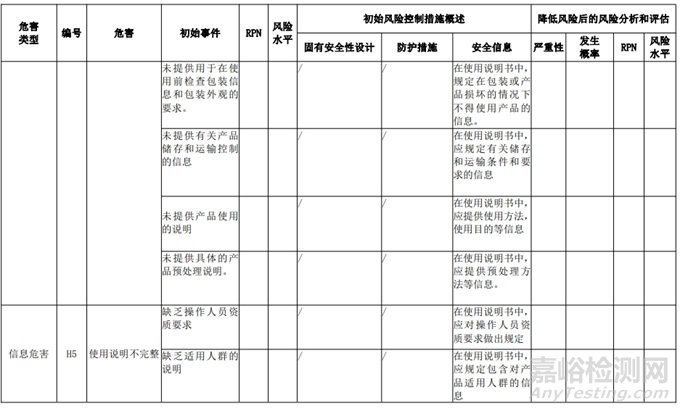
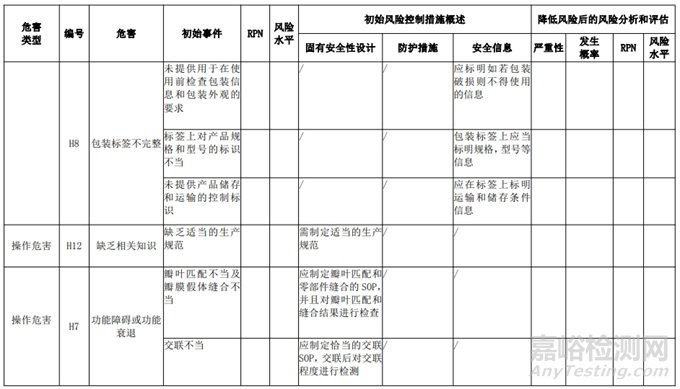
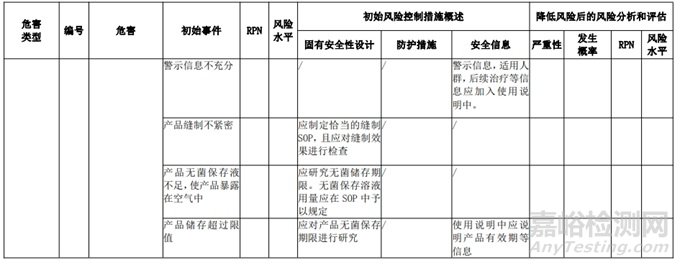
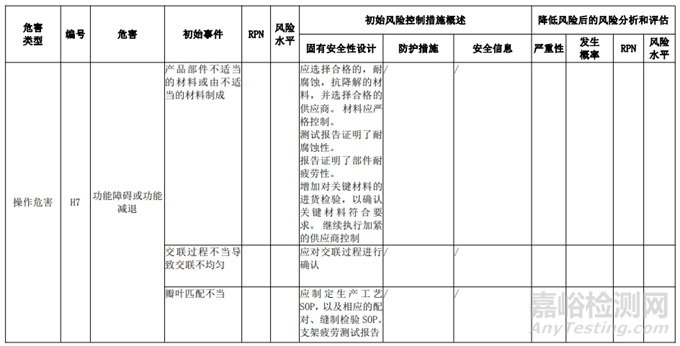
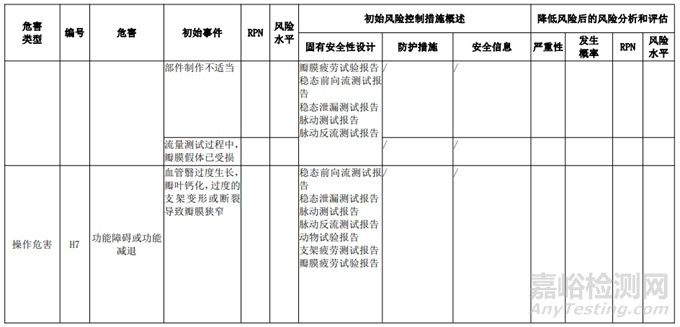
經(jīng)過對(duì)以上危害的風(fēng)險(xiǎn)分析,對(duì)不同的風(fēng)險(xiǎn)在產(chǎn)品實(shí)現(xiàn)全過程中采取了不同的控制措施�����,經(jīng)驗(yàn)證有效�����,風(fēng)險(xiǎn)可控制在可接受范圍�����,詳見附表 3《動(dòng)物源性人工心臟瓣膜風(fēng)險(xiǎn)評(píng)價(jià)、風(fēng)險(xiǎn)控制措施表(示例)》(以應(yīng)用較為普遍的牛心包材料制成品為示例)
三�����、動(dòng)物源性心臟瓣膜生產(chǎn)環(huán)節(jié)風(fēng)險(xiǎn)清單和檢查指南
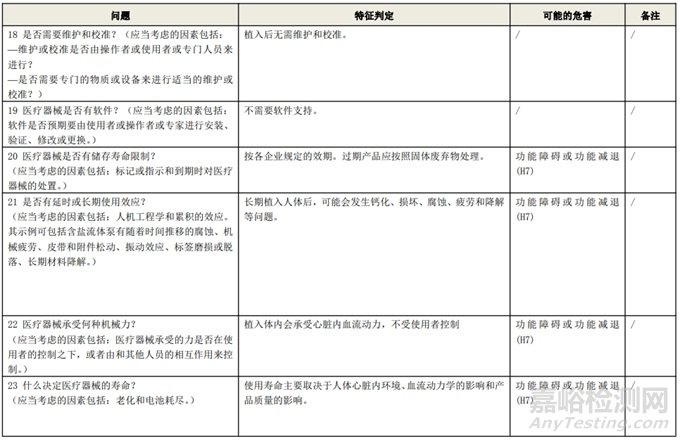
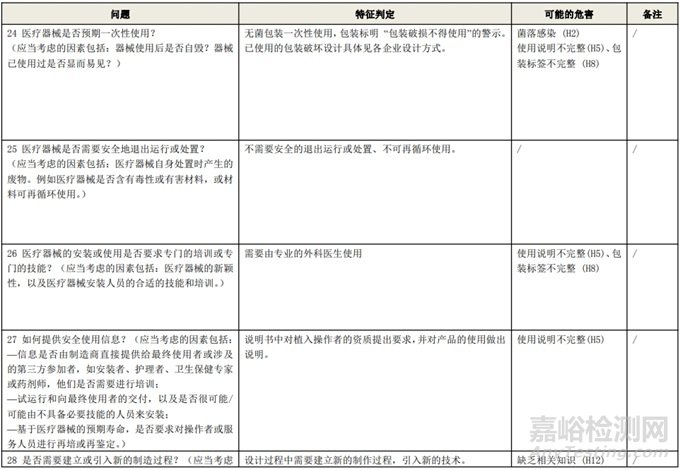
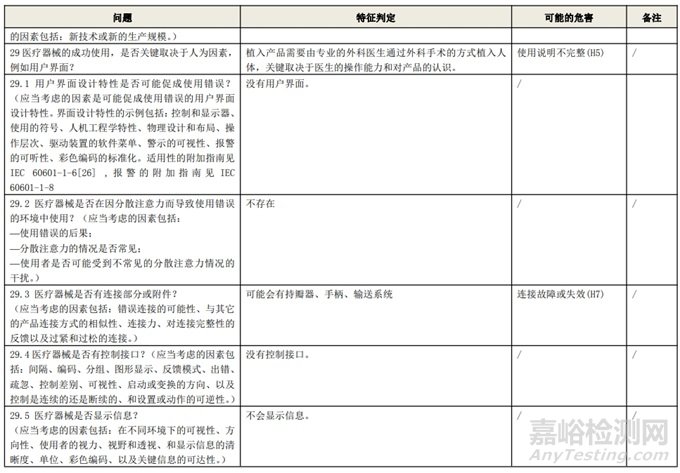
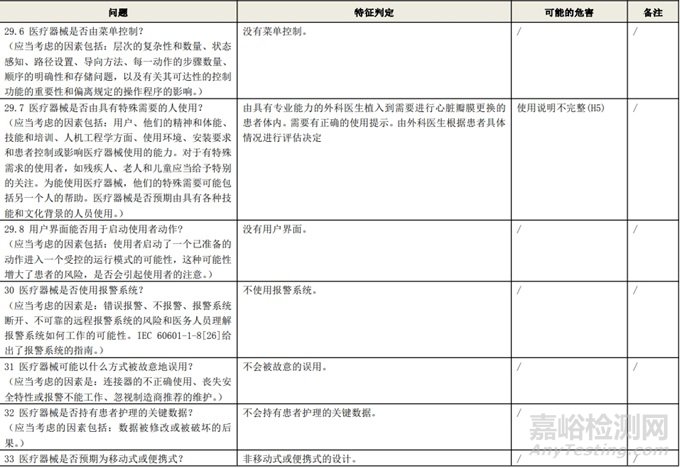
附表 1:動(dòng)物源性人工心臟瓣膜安全性特征清單(示例)(以應(yīng)用較為普遍的牛心包材料制成品為示例)
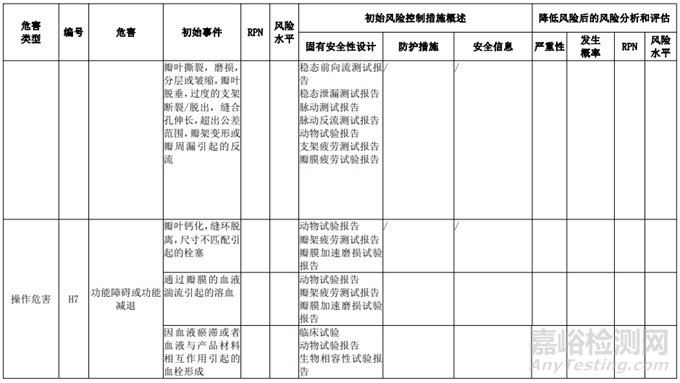
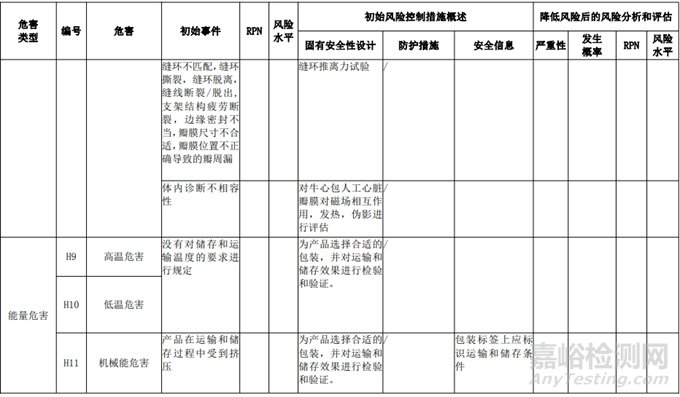
附表 2 動(dòng)物源性人工心臟瓣膜初始危害分析表(簡(jiǎn)要示例)(以應(yīng)用較為普遍的牛心包材料制成品為示例)
表 3 動(dòng)物源性人工心臟瓣膜風(fēng)險(xiǎn)評(píng)價(jià)�����、風(fēng)險(xiǎn)控制措施表(簡(jiǎn)要示例)(以應(yīng)用較為普遍的牛心包材料制成品為示例