實(shí)驗(yàn)室常用的分子診斷技術(shù)包括:PCR���、Sanger 測序����、二代基因測序(NGS)����、原位雜交等���,鑒于實(shí)際臨床工作中進(jìn)行分子診斷的樣本類型(如進(jìn)行原位雜交的樣本有血液����、羊 水穿刺�、腫瘤組織等)以及預(yù)期用途差別較大,而不同樣本類型對性能驗(yàn)證的要求和難易程 度差別較大����,建議結(jié)合實(shí)際情況酌情選擇與之相符合的性能驗(yàn)證方案。
目前�,實(shí)驗(yàn)室常規(guī)開展的分子診斷項(xiàng)目以PCR技術(shù)最為常用,PCR技術(shù)又分為PCR定量檢測技術(shù)和PCR定性檢測技術(shù)����。本文依據(jù)CNAS整理出采用PCR技術(shù)的分子診斷項(xiàng)目宜參考的性能驗(yàn)證參數(shù)及方案����。
一���、PCR定性檢測項(xiàng)目
(一)性能驗(yàn)證參數(shù)
1. PCR 定性檢測選擇驗(yàn)證的性能指標(biāo)宜包括方法符合率����、檢出限���、抗干
擾能力���、交叉反應(yīng)等。
2. 如果檢驗(yàn)程序適用樣本類型包括血清與血漿���,實(shí)驗(yàn)室在臨床檢測時(shí)同時(shí)使用 血清與血漿���,應(yīng)進(jìn)行血清與血漿結(jié)果一致性的驗(yàn)證。
3. 實(shí)驗(yàn)室應(yīng)根據(jù)檢測項(xiàng)目的預(yù)期用途以及生產(chǎn)制造商聲明����,選擇對檢測結(jié)果質(zhì)量有重要影響的參數(shù)進(jìn)行驗(yàn)證。
(二)性能驗(yàn)證方案
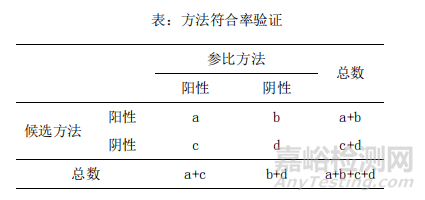
1. 方法符合率:通過參比方法比較。
① 樣本:
◆ 選取陰性樣本至少 5 例���、陽性樣本(宜包含弱陽性/低擴(kuò)增的樣本)�, 一般不少于 10 例樣本�。
注 1:罕見或少見病種的項(xiàng)目,可酌情減少樣本例數(shù)����。
注 2:若弱陽性/低擴(kuò)增樣本不好獲取,可用適當(dāng)稀釋陽性樣本獲得類似的效果����。
② 驗(yàn)證方法:
◆ 按照患者樣本檢測程序���,采用參比方法和候選方法平行檢測�。
◆ 將所有檢測結(jié)果按下表匯總填表���,計(jì)算符合率�。
陽性符合率=a/(a+c)×100%
陰性符合率=d/(b+d)×100%
總符合率=(a+d)/( a+b+c+d)×100%
③ 判斷標(biāo)準(zhǔn):
◆ 實(shí)驗(yàn)室性能驗(yàn)證結(jié)果的判斷標(biāo)準(zhǔn)是廠商或研發(fā)者在試劑盒或檢測系統(tǒng)說明書中聲明的性能指標(biāo)����。
2. 檢出限:驗(yàn)證廠家試劑使用說明書等有聲明檢出限。
① 樣本:
◆ 定值標(biāo)準(zhǔn)物質(zhì)(如:國際參考品、國家參考品�、廠家參考品)。
◆ 對于報(bào)告具體基因型的方法���,其選用的標(biāo)準(zhǔn)物質(zhì)需包括所有的突變類型����。
② 驗(yàn)證方法:
◆ 使用定值標(biāo)準(zhǔn)物質(zhì)的樣本梯度稀釋至廠家聲明的檢出限濃度���。
◆ 可重復(fù)測定 5 次或在不同批內(nèi)對該濃度樣本進(jìn)行 20 次重復(fù)測定(如測定 5 天�, 每天測定 4 份樣本)�。
◆ 稀釋液可根據(jù)情況選用廠家提供的稀釋液或陰性血清,該陰性血清除被驗(yàn)證的目標(biāo)物必須陰性外����,所含干擾物質(zhì)濃度必須在廠家聲明的范圍之內(nèi)。
③ 判斷標(biāo)準(zhǔn):
◆ 如果是 5 次重復(fù)檢測����,必須 100%檢出靶核酸;
◆ 如果是 20 次檢測����,必須檢出 至少 18 次靶核酸����。
3. 交叉反應(yīng):
對于病原體核酸檢測來說����,主要指與檢測對象核酸序列具有同源性、易引起相同或相似臨床癥狀的病原體核酸����,宜在病原體感染的醫(yī)學(xué)決定水平進(jìn)行驗(yàn)證。
① 驗(yàn)證方法:
◆ 對于病原體核酸檢測�,取一定濃度與待測核酸可能存在交叉反應(yīng)的病原體加入樣本保存液或經(jīng)確認(rèn)為陰性的樣本中,與常規(guī)樣本一樣處理���,至少重復(fù)檢測3次;
◆ 對于基因型檢測����,取一定濃度經(jīng)其它方法(如測序等)確認(rèn)為其它基因型的樣本,與常規(guī)樣本一樣處理����,至少重復(fù)檢測3次。
② 判斷標(biāo)準(zhǔn):
◆ 結(jié)果應(yīng)為陰性���。
4. 抗干擾能力
分子診斷常見的干擾物質(zhì)主要包括血紅蛋白���、甘油三酯�、膽紅素���、免疫球蛋白 G����、類風(fēng)濕因子和藥物等�。實(shí)驗(yàn)室可根據(jù)臨床需求、廠家聲明和樣本特點(diǎn)(實(shí)際可能存在的干擾物質(zhì)及達(dá)到的濃度)選擇需要驗(yàn)證的干擾物質(zhì)及濃度���。需要時(shí)�,也應(yīng)評估抗凝劑和樣本保存液等對結(jié)果的影響����。
① 驗(yàn)證方法:
實(shí)驗(yàn)室可根據(jù)實(shí)際情況選擇驗(yàn)證方案。
◆ 方案 1:實(shí)驗(yàn)組為在弱陽性樣本中加入干擾物質(zhì)溶液(對照組加入等量的溶劑)����,使得干擾物質(zhì)的終濃度與廠家聲明的濃度相同,與常規(guī)樣本一樣處理�,至少重復(fù)測定 3 次以上����。
◆ 方案 2:選取含待驗(yàn)證的高濃度水平干擾物質(zhì)且經(jīng)確認(rèn)不含被測物的臨床樣本作為實(shí)驗(yàn)組�,選取含低濃度水平干擾物質(zhì)且經(jīng)確認(rèn)不含被測物的臨床樣本作為對照組。分別在實(shí)驗(yàn)組和對照組中加入弱陽性樣本(量小于 10%)����,與常規(guī)樣本一樣處理,每組至少重復(fù)檢測 3 次�。
② 判斷標(biāo)準(zhǔn):
◆ 方案 1:弱陽性樣本檢測仍為弱陽性結(jié)果,則驗(yàn)證通過���。
◆ 方案 2:如果對照組和實(shí)驗(yàn)組結(jié)果均為弱陽性���,說明在驗(yàn)證濃度下,干擾物質(zhì)對測定無顯著影響�。如果對照組結(jié)果為弱陽性,實(shí)驗(yàn)組結(jié)果為陰性���,說明在驗(yàn)證濃度下,干擾物質(zhì)對測定有顯著影響����。
二���、PCR定量檢測項(xiàng)目
(一)性能驗(yàn)證參數(shù)
1. PCR 定量檢測選擇驗(yàn)證的性能指標(biāo)宜包括測量正確度、測量精密度(含測量重復(fù)性和測量中間精密度)���、測量不確定度�、分析特異性(含抗干擾能力)����、分析靈敏度、檢出限和定量限����、線性區(qū)間(可報(bào)告區(qū)間)等。
2. 如果檢驗(yàn)程序適用樣本類型包括血清與血漿����,實(shí)驗(yàn)室在臨床檢測時(shí)同時(shí)使用 血清與血漿,應(yīng)進(jìn)行血清與血漿結(jié)果一致性的驗(yàn)證�。
3. 驗(yàn)室應(yīng)根據(jù)檢測項(xiàng)目的預(yù)期用途以及生產(chǎn)制造商聲明,選擇對檢測結(jié)果質(zhì)量有重要影響的參數(shù)進(jìn)行驗(yàn)證���。
(二)性能驗(yàn)證方案
1. 正確度驗(yàn)證:實(shí)驗(yàn)室可采用偏倚評估����、回收試驗(yàn)、與參考方法比對等方式進(jìn)行正確度的驗(yàn)證���。
① 偏倚評估:
◆ 樣本: 按照如下優(yōu)先順序選用具有互換性的標(biāo)準(zhǔn)物質(zhì)或基質(zhì)與待測樣本相類似的標(biāo)準(zhǔn)物質(zhì):
1)有證標(biāo)準(zhǔn)物質(zhì)(CRM)����,包括國家標(biāo)準(zhǔn)物質(zhì)(如 GBW)���、國際標(biāo)準(zhǔn)物質(zhì)(如WHO���、IFCC)、CNAS 認(rèn)可的標(biāo)準(zhǔn)物質(zhì)生產(chǎn)者(RMP)提供的有證標(biāo)準(zhǔn)物質(zhì)����、與我國簽署互認(rèn)協(xié)議的其他國家計(jì)量機(jī)構(gòu)提供的有證標(biāo)準(zhǔn)物質(zhì)(如NIST、JSCC)等���;
2)標(biāo)準(zhǔn)物質(zhì)(RM)�,如廠商提供的工作標(biāo)準(zhǔn)品�;
3)正確度控制品;
4)正確度驗(yàn)證室間質(zhì)評樣本�,如 CNAS 認(rèn)可的 PTP 提供的正確度驗(yàn)證樣本����。宜根據(jù)測量區(qū)間選用至少 2 個(gè)濃度水平的標(biāo)準(zhǔn)物質(zhì)樣本�。
◆驗(yàn)證方法:
每個(gè)濃度水平的標(biāo)準(zhǔn)物質(zhì)樣本至少每天重復(fù)測定 2 次���,連續(xù)測定 5 天����,記錄檢測結(jié)果����,計(jì)算全部檢測結(jié)果的均值,并按公式計(jì)算偏倚���。
偏倚 = 結(jié)果均值 − 參考值
② 與參考方法比對:
◆ 樣本:
適宜的臨床樣本���,不少于 8 份,被測物濃度在測量區(qū)間內(nèi)均勻分布�,并關(guān)注醫(yī)學(xué)決定水平。
◆ 驗(yàn)證方法:
按照患者樣本檢測程序���,采用參比方法和候選方法平行檢測����。
按照制造商說明書或作業(yè)指導(dǎo)書規(guī)定的方法對實(shí)驗(yàn)方法進(jìn)行校準(zhǔn)/校準(zhǔn)驗(yàn)證,宜在相同時(shí)段內(nèi)完成對同一樣本的兩種方法平行檢測���,每份樣本每個(gè)檢測方法重復(fù)檢測 3 次���,計(jì)算每份樣本兩種方法檢測結(jié)果的均值,并按照公式計(jì)算偏倚�。
偏倚 = 結(jié)果均值 − 參考值
2. 精密度驗(yàn)證:精密度驗(yàn)證應(yīng)包括重復(fù)性和中間精密度。
① 樣本:
◆ 可采用新鮮或凍存的樣本����。
◆ 當(dāng)樣本中待測物不穩(wěn)定或樣本不易得到時(shí),也可考慮使用基質(zhì)與實(shí)際待檢樣本相似的樣本���,如質(zhì)控品�。
◆ 應(yīng)至少評估 2 個(gè)水平樣本的不精密度�。當(dāng) 2 個(gè)水平樣本的不精密度有顯著差異時(shí),建議增加為 3 個(gè)水平����。
◆ 所選樣本的被測物水平應(yīng)在測量區(qū)間內(nèi),適宜時(shí)���,至少有 1 個(gè)樣本的被測物水平在醫(yī)學(xué)決定水平左右���。
注意:
注 1:通常較高值樣本的不精密度較小,較低值樣本的不精密度偏大����。對低值有臨床意
義的檢測項(xiàng)目,宜評估有判斷價(jià)值的低水平樣本的不精密度�。
注 2:如檢測結(jié)果沒有明確的醫(yī)學(xué)決定水平,可在參考區(qū)間上限左右選一個(gè)濃度���,再根
據(jù)檢驗(yàn)項(xiàng)目的特點(diǎn)在測量區(qū)間內(nèi)選擇另一個(gè)濃度�。
注 3:如與廠商或文獻(xiàn)報(bào)導(dǎo)的不精密度比較����,所選樣本水平宜與被比較的樣本水平接近。
② 重復(fù)性驗(yàn)證:
◆ 驗(yàn)證方法: 對樣本進(jìn)行至少 10 次重復(fù)測定����,計(jì)算均值、SD 和 CV����。
◆ 質(zhì)量控制: 實(shí)驗(yàn)過程中應(yīng)至少檢測一個(gè)質(zhì)控品。當(dāng)質(zhì)控結(jié)果失控時(shí),不論實(shí)驗(yàn)結(jié)果是否滿意都應(yīng)棄去不用�,重新進(jìn)行試驗(yàn)以取得全部實(shí)驗(yàn)數(shù)據(jù)。
◆ 數(shù)據(jù)分析:依據(jù)實(shí)驗(yàn)數(shù)據(jù)計(jì)算均值和標(biāo)準(zhǔn)差�。
③ 同時(shí)驗(yàn)證重復(fù)性和中間精密度:
◆ 驗(yàn)證方法:每天檢測 1 個(gè)分析批,每批檢測 2 個(gè)水平的樣本���,每個(gè)樣本重復(fù)檢測 3~5 次���,連續(xù)檢測 5 天。在每一批次測量中�,應(yīng)同時(shí)測量質(zhì)控品。
◆ 數(shù)據(jù)分析:
3. 可報(bào)告范圍驗(yàn)證::定量分析方法的可報(bào)告范圍是臨床實(shí)驗(yàn)室發(fā)出檢驗(yàn)報(bào)告的依據(jù)之一�,可報(bào)告范圍的驗(yàn)證包括可報(bào)告低限(定量下限)與可報(bào)告高限(定量上限×樣本最大稀釋倍數(shù))。
① 樣本
◆ 宜選擇與待測樣本具有相同基質(zhì)的樣本����。
② 樣本準(zhǔn)備
◆ 以血清樣本為例。
低值樣本準(zhǔn)備:將待測樣本(含被分析物)用混合人血清(含被分析物濃度水平較低)或 5%牛血清白蛋白生理鹽水溶液進(jìn)行稀釋����,產(chǎn)生接近于方法測量區(qū)間低限(定量下限)濃度水平的樣本,通常為 3~5 個(gè)濃度水平�,濃度間隔應(yīng)小于測量區(qū)間低限的 20%。
高值樣本準(zhǔn)備:使用混合血清或 5%牛血清白蛋白生理鹽水溶液或測定方法要求的稀釋液對高值待測樣本(必要時(shí)可添加被分析物�,并計(jì)算出理論值)進(jìn)行稀釋����,使其接近于線性范圍的上 1/3 區(qū)域內(nèi)�,并記錄稀釋倍數(shù)。至少選用 3 個(gè)高濃度樣本�,稀釋倍數(shù)應(yīng)為方法性能標(biāo)明的最大稀釋倍數(shù)并適當(dāng)增加或減小稀釋比例。
③ 驗(yàn)證方法
◆ 在一次運(yùn)行中將每個(gè)低值樣本重復(fù)測定 5~10 次���,每個(gè)高值樣本重復(fù)測定 3次。
④ 數(shù)據(jù)分析
◆ 分別計(jì)算每個(gè)低值樣本的均值�、SD、CV 值�。
◆ 對高值樣本,計(jì)算乘以稀釋倍數(shù)后的還原濃度和相對偏差����。
⑤ 可報(bào)告范圍的確定
◆ 可報(bào)告范圍低限(定量下限)
以方法性能標(biāo)示的總誤差或不確定度為可接受界值,從低值樣本結(jié)果數(shù)據(jù)中選取總誤差或不確定度等于或小于預(yù)期值的最低濃度水平作為可報(bào)告范圍低限���。
◆ 可報(bào)告范圍高限
選取還原濃度與理論濃度的偏差(%)等于或小于方法預(yù)期偏倚值時(shí)的最大稀釋倍數(shù)為方法推薦的最大稀釋倍數(shù)����,測量區(qū)間的高限與最大稀釋倍數(shù)的乘積為該方法可報(bào)告范圍的高限���??蓤?bào)告范圍高限的確定應(yīng)考慮臨床需求。
注:超出可報(bào)告范圍時(shí)����,實(shí)驗(yàn)室檢測結(jié)果不能滿足其預(yù)期總誤差或不確定度的要求。
4. 分析特異性驗(yàn)證
① 樣本
◆ 宜選取被測量水平不同的 2 個(gè)樣本為基礎(chǔ)樣本�,可參考醫(yī)學(xué)決定水平或參考區(qū)間限值。
② 干擾物質(zhì)選擇
◆ 宜根據(jù)檢測方法的原理和預(yù)期用途選擇常見的可能產(chǎn)生干擾作用的物質(zhì)�。
③驗(yàn)證方法
◆ 干擾物原液中干擾物的濃度應(yīng)高于實(shí)驗(yàn)濃度 20 倍以上,以減少對基礎(chǔ)樣本基質(zhì)的稀釋作用���。
◆ 重復(fù)檢測(n≥3)實(shí)驗(yàn)樣本和對照樣本����,分別計(jì)算 2 組結(jié)果均值�,和均值間的差值。
④ 判斷標(biāo)準(zhǔn)
◆ 滿足干擾標(biāo)準(zhǔn)時(shí)的最高干擾物濃度�,應(yīng)符合檢測方法規(guī)定的要求。
5. 分析靈敏度驗(yàn)證
① 樣本
◆ 宜選取與待測樣本相同基質(zhì)的樣本�,濃度或活性已知,且水平處于參考區(qū)間上限(或醫(yī)學(xué)決定水平)附近����。
② 驗(yàn)證方法
◆ 在檢測方法正常運(yùn)行的條件下重復(fù)檢測樣本 3 次���。
③ 判斷標(biāo)準(zhǔn)
◆ 實(shí)驗(yàn)結(jié)果符合檢測程序規(guī)定的范圍,如企業(yè)標(biāo)準(zhǔn)�。
資料來源:
CNAS-GL039:2019《分子診斷檢驗(yàn)程序性能驗(yàn)證指南》
CNAS-GL037:2019《臨床化學(xué)定量檢驗(yàn)程序性能驗(yàn)證指南》