在藥品的開發(fā)和最終商業(yè)化過程中必須指定有效期�����。有效期使用各種因素來確定在合理的儲存條件下產(chǎn)品對病人安全有效的時限��。有效期不僅作為臨床試驗申請?zhí)峤坏牟牧弦矐?yīng)用于商業(yè)化產(chǎn)品�。在某些情況下���,會指定兩個有效期:一個用于原始包裝的散裝劑型,另一個對應(yīng)于從初級包裝中取出制劑后的安全儲存時間����,這對于需給病患用藥前需配制的藥品尤其重要。
1�、化學(xué)穩(wěn)定性
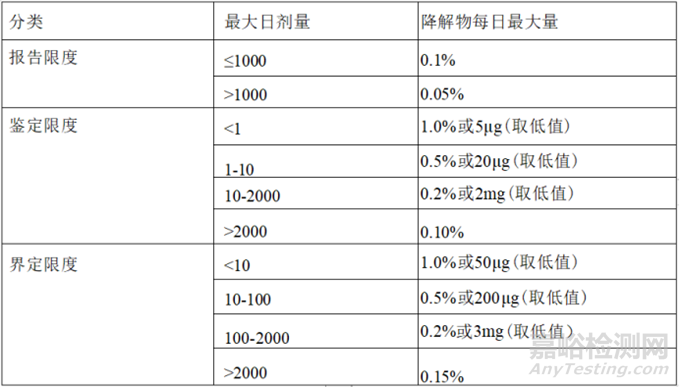
藥物活性成分(APIs),無論是生物成分(即蛋白質(zhì)還是核酸)或小分子�����,容易受到有機化學(xué)降解的影響���,為了保證藥品的安全性和有效性�,監(jiān)管機構(gòu)要求對降解產(chǎn)物進行評估以指定有效期。藥品的有效期是根據(jù)在規(guī)定的可能貯藏條件下發(fā)生某些變化的時間所制定���,這些變化包括降解物水平達到影響安全性或活性成分的含量或活性降至臨界水平以下所需的時間�����。降解物需進行限度規(guī)定�����,降解物限度可根據(jù)攝入API的總?cè)談┝坑嬎?���,并需進行相應(yīng)報告��,鑒別和定量限度��。報告限度為降解物存在的限度��,達到該限度必須向監(jiān)管機構(gòu)報告以提醒他們降解物的含量��,通?��?稍贖PLC檢出峰的存在。鑒定限度定義為一限度,大于該限度的降解產(chǎn)物需鑒定其結(jié)構(gòu)���。最后����,界定限度為需進行毒理學(xué)評估以確保安全性評價的限度����。這些限度定義為API每日總攝入量的百分比或絕對質(zhì)量,取數(shù)值較低者�����。下表說明了特定降解物的不同限度要求�����,該要求與ICH 的建議一致��。各閾值通常允許的特定降解產(chǎn)物水平�。
用于確定特定降解產(chǎn)物水平的容許因素取決于以下因素:
1)如果降解物也是一種代謝物,那么降解物水平的限度允許較高���,因為該類降解物在API的臨床研究中已被證實其安全性����。
2)若原料藥處于低劑量時,在可接受的暴露量下�����,其降解物的比例接受上限可稍微高點�����。
3)若降解物是可能為致癌物����、致畸劑或致突變,則應(yīng)采用更低的限度�。
4)若要長期服用該API,允許的降解物限度可能低于單次給藥下降解物限度。
5)在有效期末��,缺乏安全信息的降解物一般定義其限度為在API的0.2-0.5%���。
值得注意的是�����,在某些情況下���,降解物也可以是工藝雜質(zhì)(如,存在于初始未處理的API 樣品中)�。穩(wěn)定性限度反映了物料的總量,包括最初存在的數(shù)量和在儲存條件下形成的數(shù)量����。
在某些情況下,已知降解物是無害的(如�����,藥物前體的降解)�。在這些情況下,有效期的限制因素將是API含量的下降�。雖然這對患者不會造成直接的安全風(fēng)險,但如果患者沒有接受預(yù)期劑量的原料藥仍可能造成危害���。一般來說��,基于ICH指導(dǎo)原則����,效期末的含量需要保持在標(biāo)示量的95%或以上���。若考慮到初始含量的可變性���,則影響更為顯著��。
大分子藥物如核酸�����、蛋白質(zhì)和寡核苷酸�、化學(xué)降解部分分子與活性位點無關(guān)��,對生物活性可能沒有顯著影響��。正因為如此���,盡管化學(xué)降解量可能相當(dāng)顯著也不至于限制有效期����?��;钚酝ǔJ怯蒙镄Яχ甘緦嶋H的活度��。當(dāng)化學(xué)降解發(fā)生在生物分子的活性位點附近����,其活性損失可能與小分子一樣顯著;然而�����,若降解并不直接或通過二級或三級結(jié)構(gòu)改變影響活性位點�����,即使蛋白質(zhì)的側(cè)鏈降解40%也不會影響它的活性�����。
在確定藥品的有效時�,最具限制性的因素將成為決定型因素���。例如����,如果基于毒性問題某單一降解產(chǎn)物具有非常嚴(yán)格的限度����,即使迅速形成不同的降解產(chǎn)物,其也可能是設(shè)定有效期的限制因素�����。一般來說,在存儲條件下��,即使在效期末�����,制劑產(chǎn)品中原料藥轉(zhuǎn)化為降解物的比例也相對較低����。因此,沒必要在制劑產(chǎn)品的降解過程中全程監(jiān)測此項�����。實際上���,達到有效期后限制因素發(fā)生的情況變得無關(guān)緊要��。該論述可用于加速試驗中�����,并將在后續(xù)章節(jié)討論���。
對于由藥劑師或患者配制的液體制劑,在配制前和配制后應(yīng)單獨注明其有效期。配制前的物理穩(wěn)定性意味著配制前制劑的效期應(yīng)該涵蓋配制后如溶解或分散的穩(wěn)定性�����。配制后�����,穩(wěn)定性問題與其他液體制劑類似���。即使是固體劑型���,藥品運輸(可能帶有更加保護性的包裝)和患者接收時的有效期也不同。
2��、物理穩(wěn)定性
在某些情況下����,有效期的可能是受到制劑物理穩(wěn)定性而不是其化學(xué)穩(wěn)定性限制。物理穩(wěn)定性最重要的是在儲存后引起劑型性能的改變�����。其中特別關(guān)注的是可能改變其API生物利用度的任何因素�����。對于固體劑型,這可能意味著溶解性能發(fā)生了變化(崩解和隨后的溶解)��。片劑和膠囊劑在儲存時出現(xiàn)溶出度變化的原因有很多�����。對于片劑���,大多數(shù)問題與從環(huán)境中吸收水分有關(guān)����,這使得崩解劑的效力改變�。崩解劑能夠吸水迅速膨脹�,使藥片在胃中破裂。在儲存過程中濕氣被緩慢吸收,發(fā)生緩慢的膨脹,這阻礙了崩解劑在胃中快速崩解所需的爆炸性膨脹�����。當(dāng)片劑暴露于胃液(或溶出杯)中時�,崩解劑未能像藥片在干燥時那樣吸收更多的水,因此無法有效崩解���。當(dāng)崩解劑暴露于水冷凝的環(huán)境下�����,這樣的問題尤其顯著,如運輸時藥品從初始包裝的氣候帶經(jīng)過更冷的氣候帶���,此時片劑從較高的溫度和濕度轉(zhuǎn)至低于此前露點����?��?赡馨l(fā)生這種情況�����。
對于明膠膠囊(包括普通膠囊和軟膠囊),膠囊本身在長期保存后容易發(fā)生物理變化���。在某些情況下,由于在制劑或包裝中的雜質(zhì)水平較低��,明膠將發(fā)生交聯(lián)反應(yīng)����。此類反應(yīng)通常是由小分子醛(例如甲醛和乙二醛)引起的����。這種交聯(lián)可能使得明膠在標(biāo)準(zhǔn)溶出介質(zhì)中的溶解變得緩慢�。但應(yīng)注意在許多情況下,由于酶促過程的存在�����,體內(nèi)釋放不會受交聯(lián)反應(yīng)的影響��。該影響可采用含有適當(dāng)消化酶的特定溶出介質(zhì)進行監(jiān)測�����。
固體制劑的另一潛在物理變化涉及API的晶型�。大多數(shù)藥物劑型采用的API具有獨特的晶型。在大多數(shù)情況下����,分子排列不是唯一的��,也就是說��,不同晶型的API具有不同能量�����。若制劑產(chǎn)品使用的API呈現(xiàn)多晶型且為高能形式,在儲存期間則有可能出現(xiàn)晶型的改變��。在極少數(shù)情況下��,這種晶型的改變可能會改變生物利用度���。這可能是由于溶解度的變化(穩(wěn)定的多晶型物通常溶解度較低)��,溶出速率也相應(yīng)被改變�����。即使使用是熱力學(xué)最穩(wěn)定的晶型���,溶劑化或去溶劑化仍然可能隨放置時間而發(fā)生。去溶劑化產(chǎn)生是溶劑分子 (包括水合物)從晶格中丟失�����。溶劑化則通常是向晶格中添加水�。一個晶型變化的極端例子,如去溶劑化導(dǎo)致完全失去晶格���,而使得API形成了無定型����。這種晶型的改變通常提高了藥物溶解度(溶出速率),但卻降低了藥物穩(wěn)定性���。
對于某些API, 制劑可利用其無定型或其他高能型態(tài)增加溶解度���,從而提高生物利用度,此類劑型中的原料藥具有自發(fā)結(jié)晶的潛力�����,因為該過程是放熱的并且通常是自催化的(即一旦晶核產(chǎn)生����,它們可以增加進一步結(jié)晶的速率)。盡管如此�����,通過添加合適的穩(wěn)定劑����,無定型系統(tǒng)可限制晶體生長,從而在較長的放置期間保持穩(wěn)定�����。由于這種隨時間的變化可能會導(dǎo)致API藥效下降���,有效期可能受此因素限制���。
對于液體劑型,在儲存時發(fā)生生物利用度改變通常表現(xiàn)為API或其他制劑組分的沉淀��?�?赡軐?dǎo)致沉淀的因素有很多���。對于小分子�����,沉淀可能是由于溶液(懸浮液)的pH值發(fā)生變化�。這種變化可能是由于吸收二氧化碳��,某種成分發(fā)生化學(xué)降解例如由于氧化產(chǎn)生酸或堿或緩沖成分的損失。小分子化合物沉淀的另一個原因則是由于API粒徑增加�����。這種效應(yīng)稱為奧斯特瓦爾德(Ostwald)熟化�,由于較小的120K.C.Waterman晶體在逐漸溶解過程中,因自身能量低于較大的晶體�,也同時在生長(較大的晶體具有較低的表面體積比,晶體表面很少本身具有更高能量的分子)�����。后續(xù)章節(jié)將進一步討論了原料藥和制劑產(chǎn)品物理穩(wěn)定性��。
對于生物分子�����,懸浮液的特性將取決于分子的二級和三級結(jié)構(gòu)特征��,這又涉及離子��,范德華力和氫鍵合力�����。通常,大分子有多種構(gòu)型它們通常具有相似的能量�����,但凝集趨勢卻大不相同�����,從而導(dǎo)致不同的生物活性����。雖然最初形成的生物API的構(gòu)型可能是單體且懸浮良好�����,但隨放置時間的推移�,大分子可能變性,從而導(dǎo)致聚集和沉淀��。由于聚集狀態(tài)無法與助懸劑重新平衡�,根據(jù)LeChatlier的原理,這一過程可使沉淀加劇����。更多詳細(xì)信息請參見后續(xù)章節(jié)。
3、外觀
有時��,制備成制劑的API可能出現(xiàn)外觀的改變���,其物理穩(wěn)定性或化學(xué)降解幾乎沒有變化���。顏色變化這種化學(xué)變化可以通過肉眼敏感地監(jiān)測出。盡管這種細(xì)微的化學(xué)變化不太可能對病人造成威脅�,但外觀變化可能會影響病人使用,因此這也會限制藥品的有效期�����。
在干燥條件下(例如使用干燥劑)儲存時,明膠膠囊可能會變硬�。雖然脆性可能不會導(dǎo)致生物活性發(fā)生變化,但仍然可能產(chǎn)生不可接受的外觀��。
對于包衣有膜包衣的片劑�����,在某些情況下�����,片芯水分溶脹可能引起包衣破裂。雖然這樣做也不應(yīng)影響性能���,但仍會干擾患者���,因此將限制有效期(或需要特殊包裝)�。
4、微生物生長
對于注射劑��,有效期的限制因素應(yīng)關(guān)注微生物雜質(zhì)�����。對于許多此類制劑�����,通常加入生物穩(wěn)定劑添加以防止或至少減慢微生物的生長��。一旦穩(wěn)定劑被消耗�����,微生物雜質(zhì)可能增長��。對于其他處方,在放置過程中���,包裝的完整性可能決定微生物的生長趨勢��。
5��、光化學(xué)降解
藥品的光敏性會影響其有效期��,在許多情況下也決定了產(chǎn)品的包裝要求�����。在某些情況下��,API可能吸收光照后引發(fā)化學(xué)反應(yīng)并誘發(fā)化學(xué)降解�����。光化學(xué)反應(yīng)通常包括氧化和自由基重排��。間接光化學(xué)過程也是可能的�,在這些情況下�����,光被處方中的某種物質(zhì)吸收,而非API, 然后導(dǎo)致與API發(fā)生反應(yīng)�����。最有問題的環(huán)境光波長是長紫外光和短可見光(藍色)光�����,部分原因是由于能量(高能波長),也有可能是因為吸收光譜的重疊����。大多數(shù)影響API穩(wěn)定性的光過程以互為倒數(shù)的方式響應(yīng)光強度���,即當(dāng)光的總通量是相同的��,則短時間�����、高強度曝光與長時間����、低強度曝光具有相同的影響�����。因此,制劑產(chǎn)品的光照試驗可以在光照箱中進行��,這種光照箱裝有高功率紫外線發(fā)射燈并配備過濾器��,能過濾320nm以下的光�。