MDR法規(guī)要求在醫(yī)療器械的標(biāo)簽上注明各種信息�。
歐洲有24種官方語(yǔ)言���,這就需要根據(jù)器械提供的地方將標(biāo)簽上提供的信息翻譯成多種語(yǔ)言。這個(gè)要求可以通過(guò)使用標(biāo)識(shí)來(lái)處理����。MDR 法規(guī)允許在標(biāo)簽上使用標(biāo)識(shí)作為書(shū)面語(yǔ)言的替代品,具體法規(guī)信息在MDR Annex 1, chapter III中做了具體說(shuō)明��,標(biāo)識(shí)是高效���、節(jié)約成本和國(guó)際理解的概念�����,可向醫(yī)療器械用戶傳達(dá)所需信息�����。
2、歐盟法規(guī)下的要求明細(xì)
在MDR Annex 1, chapter III有關(guān)器械隨附信息的要求, paragraph 23.2 標(biāo)簽上的信息中,概述了標(biāo)簽上必須包括的內(nèi)容,并作為下列標(biāo)識(shí)的立法參考:
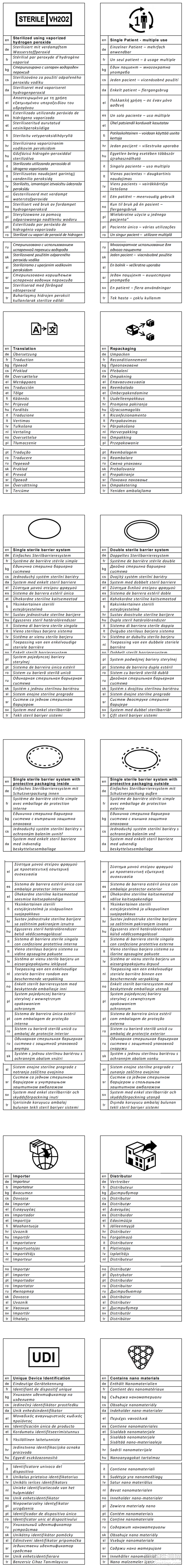
以下標(biāo)識(shí)可在ISO 15223-1:2021中找到����。如果一個(gè)符號(hào)是在ISO 7000中注冊(cè)的���,那么它的數(shù)字引用將包括在符號(hào)標(biāo)題旁邊�。否則����,沒(méi)有在ISO 7000中注冊(cè)的符號(hào)只能在ISO 15223-1:2021中找到。
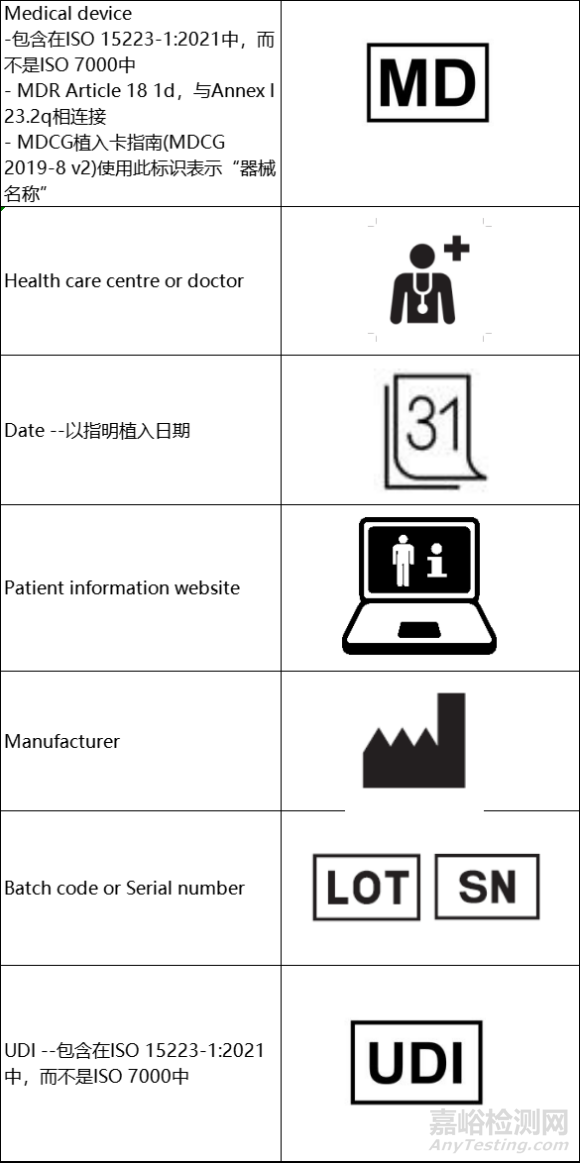
1. 醫(yī)療器械 MDR, Annex 1, 23.2, q.
2. 含有人類(lèi)血液或血漿衍生物(3701) MDR, Annex 1, 23.2, e.
3.含有藥用物質(zhì)(3702) MDR, Annex 1, 23.2, e
4. 含有有害物質(zhì)(3723) MDR Annex 1, 23.2.(f)
5.含有人源的生物材料(3700) MDR, Annex 1, 23.2, e.
-此標(biāo)識(shí)表示其所貼的醫(yī)療器械包含源自人類(lèi)的組織或細(xì)胞����,或其衍生物
6. 含有動(dòng)物源的生物材料(3699) MDR, Annex 1, 23.2, e.
-此標(biāo)識(shí)表示其所貼的醫(yī)療器械含有動(dòng)物源的組織或細(xì)胞或其衍生物。
7.使用蒸汽過(guò)氧化氫消毒 MDR ,AnnexI, 23.2, 1 .(滅菌方法)
8. 翻譯(3728)& 9.再包裝(3727)
•MDR Article 16 Point 3要求在器械/其包裝或隨附文件上提及這些活動(dòng):“進(jìn)行第2段(A -包括翻譯)和(b -包括再包裝)所述活動(dòng)的經(jīng)銷(xiāo)商或進(jìn)口商應(yīng)在器械上��,或者在不可行的情況下���,在其包裝上或在器械隨附的文件中注明所進(jìn)行的活動(dòng)及其名稱(chēng)����,注冊(cè)商號(hào)或注冊(cè)商標(biāo),注冊(cè)營(yíng)業(yè)地點(diǎn)和可以聯(lián)系它的地址����,以便確定其位置。”
這些標(biāo)識(shí)已被開(kāi)發(fā)用于這些實(shí)體���,以促進(jìn)其遵守
10.單患者多次使用(3706)
建議使用當(dāng)前的符號(hào)來(lái)表示“單患者多次使用的意思。
此符號(hào)是ISO 15223標(biāo)準(zhǔn)的一部分��,也是ISO 7000數(shù)據(jù)庫(kù)的一部分���。它的使用得到了ISO和IMDRF文件中引用的支持����。
•參考ISO 20417: 2021 Medical devices — Information to be supplied by the manufacturer and IMDRF 2019‘’Principles of Labelling for Medical Devices and IVD Medical Devices’’, Art. 5.2.18: ‘
11. 單一無(wú)菌屏障系統(tǒng)(3707)
12. 雙重?zé)o菌屏障系統(tǒng)(3704)
13. 內(nèi)置保護(hù)性包裝的單一無(wú)菌屏障系統(tǒng)(3708)
14. 外部有保護(hù)性包裝的單一無(wú)菌屏障系統(tǒng)(3709)
MDR AnnexI GSPR 23.3,保持器械無(wú)菌狀態(tài)的包裝上的信息(“無(wú)菌包裝”)����,具體而言���,該部分a)點(diǎn):“允許無(wú)菌包裝被識(shí)別的指示”形成了這四個(gè)標(biāo)識(shí)被開(kāi)發(fā)的要求�����。
15. 進(jìn)口商(3725)& 16.經(jīng)銷(xiāo)商(3724)
進(jìn)口商和經(jīng)銷(xiāo)商在MDR 下有新的義務(wù),其中包括在標(biāo)簽上標(biāo)明他們的活動(dòng)與再包裝和翻譯有關(guān)(MDR Article 16)���。開(kāi)發(fā)這些標(biāo)識(shí)是為了方便遵守MDR �����。
17. UDI
MDR AnnexVI, Part C UDI系統(tǒng),The UDI System, 4. UDI Carrier, 4.5”如非UDI載體的AIDC載體是產(chǎn)品標(biāo)簽的一部分���,UDI載體必須易于識(shí)別����。”
18. 含有納米材料(3703)
MDR 越來(lái)越重視納米材料(例如 AnnexI GSPR�,chapter II, Article 10.6),雖然沒(méi)有正式要求在標(biāo)簽上注明有關(guān)納米材料的具體信息���,但該符號(hào)的創(chuàng)建被認(rèn)為是有用的。
3����、標(biāo)識(shí)驗(yàn)證和處理
根據(jù)ISO 15223-2流程(ISO 15223-2:2010-01 Medical Devices – Symbols to be used with medical device labels, labelling, and information to be supplied – Part 2: Symbol development, selection and validation)對(duì)上述標(biāo)識(shí)1,2,4,6,8 -10進(jìn)行了驗(yàn)證���。驗(yàn)證在多個(gè)地區(qū)以五種語(yǔ)言運(yùn)行,包括患者和醫(yī)療保健提供者�。根據(jù)上述ISO 15223-2流程對(duì)剩余的新符號(hào)進(jìn)行了驗(yàn)證�����。
所有符號(hào)在5毫米高度(與CE MARK要求的最低高度相同)可伸縮和識(shí)別����。他們將確保醫(yī)療器械以有效的方式符合MDR ����,并將向醫(yī)療保健專(zhuān)業(yè)人員和患者等最終用戶清楚地傳達(dá)相關(guān)信息���。
4、標(biāo)識(shí)注釋:關(guān)于標(biāo)識(shí)使用的注釋
在歐盟��,這些標(biāo)識(shí)必須在符合MDR 23.1. h)直到它們以統(tǒng)一的歐洲標(biāo)準(zhǔn)出版����。請(qǐng)注意,歐盟以外的司法管轄區(qū)可能對(duì)“制造商提供的信息”有不同的要求�。
使用以下標(biāo)簽介紹中提供的模板時(shí):
•如果制造商的特定需求不需要某些符號(hào)����,可以從列表中刪除全部或部分符號(hào)���,但建議您始終保持所附列表中所示的相同順序。制造商總是使用相同的訂單將加快用戶識(shí)別和接受符號(hào)及其含義�����。
•請(qǐng)確保始終使用與ISO 7000或ISO 15223-1:2021相同的標(biāo)題(以避免用戶之間的混淆)�����。
5、標(biāo)識(shí)模板-標(biāo)識(shí)設(shè)計(jì)��、標(biāo)題和翻譯
以下內(nèi)容包含的所有符號(hào)均可在ISO 15223-1(2021) 2021醫(yī)療器械-與制造商提供的信息一起使用的符號(hào)-第1部分:一般要求中找到����。
6����、患者植入卡使用的推薦標(biāo)識(shí)
-作為文本的替代
-根據(jù)MDR Article 18的要求��,推薦使用以下符號(hào)
-以下符號(hào)可以在ISO 15223-1:2021中找到。如果一個(gè)符號(hào)是在ISO 7000中注冊(cè)的�����,那么它的數(shù)字引用將包括在符號(hào)標(biāo)題旁邊����。否則�����,沒(méi)有在ISO 7000中注冊(cè)的符號(hào)只能在ISO 15223-1:2021中找到