【問(wèn)】在非最終滅菌藥液的配制過(guò)程中��,應(yīng)有哪些注意事項(xiàng)?
【答】1、配制開始前關(guān)鍵要素準(zhǔn)備和檢查
(1)環(huán)境及衛(wèi)生檢查: 查配制間的溫濕度��、壓差�、環(huán)境衛(wèi)生狀況符合生產(chǎn)工藝要求,確認(rèn)已完成清場(chǎng)工作且在有效期內(nèi)����。
(2)公用介質(zhì)檢查及準(zhǔn)備: 確保壓縮空氣、保護(hù)氣體等滿足生產(chǎn)需要��,各接口無(wú)泄漏��。
(3)儀器檢查: 檢查如電子天平等儀器完好�,校驗(yàn)標(biāo)識(shí)在有效期內(nèi)。
(4)檢查氣體過(guò)濾濾芯應(yīng)在規(guī)定使用期限內(nèi)����。
(5)設(shè)備/器具清潔檢查:確認(rèn)配制系統(tǒng)各設(shè)備,設(shè)施狀態(tài)完好并已清潔消毒滅菌��,且在有效期內(nèi)����,器具經(jīng)清潔滅菌后無(wú)菌轉(zhuǎn)運(yùn)至配制間待用。如果不是無(wú)菌投料,配制工具可以滅菌后密閉轉(zhuǎn)移�。
(6)檢查A級(jí)區(qū)的層流裝置,確保層流運(yùn)行正常 (如適用)�。
(7)檢查配制所需的記錄、文件��、標(biāo)識(shí)等均符合規(guī)定�。
(8)按照批生產(chǎn)指令和產(chǎn)品工藝規(guī)程,設(shè)置工藝參數(shù)及配制模塊下載產(chǎn)品配方和填寫配方名稱及批次����、批量,包括工藝參數(shù)涉及物料名稱����、物料重量、混粉轉(zhuǎn)速/頻率��、混粉時(shí)間等 (如適用)����。
(9)物料準(zhǔn)備和檢查: 按照批生產(chǎn)指令核對(duì)生產(chǎn)所需原輔料是否齊全,且包裝袋或容器應(yīng)密封且完好����,經(jīng)過(guò)消毒或滅菌后經(jīng)過(guò)無(wú)菌轉(zhuǎn)運(yùn)至稱量處��。如果不是無(wú)菌稱量����,工具滅菌后密閉轉(zhuǎn)移��。
(10)消毒液的領(lǐng)取準(zhǔn)備: 檢查即將使用的消毒液應(yīng)在配制有效期��。
2��、 配制過(guò)程崗位操作
(1)根據(jù)產(chǎn)品工藝規(guī)程計(jì)算復(fù)核批生產(chǎn)指令的原輔料投料量應(yīng)準(zhǔn)確無(wú)誤��,并雙人復(fù)核�。
(2)若使用全無(wú)菌工藝進(jìn)行配制��,應(yīng)在A級(jí)環(huán)境下對(duì)無(wú)菌物料進(jìn)行稱量����,并雙人復(fù)核。若配制后藥液經(jīng)除菌過(guò)濾�,則應(yīng)在A級(jí)送風(fēng)下進(jìn)行稱量。
(3)按產(chǎn)品工藝順序及要求逐一核實(shí)原����、輔料的品名�、性狀��、重量等��,準(zhǔn)確無(wú)誤后開始按工藝要求無(wú)菌投料��,建議采用自動(dòng)投料設(shè)備以降低投料過(guò)程的污染風(fēng)險(xiǎn)��。
(4)應(yīng)按照產(chǎn)品工藝規(guī)程的規(guī)定轉(zhuǎn)速�、時(shí)間等要求,進(jìn)行混合�。配制崗位日常生產(chǎn)監(jiān)控點(diǎn)見表6-5。
3��、 配制結(jié)束后
(1)剩余物料需在對(duì)應(yīng)稱量環(huán)境級(jí)別下進(jìn)行密封��,如若使用全無(wú)菌工藝進(jìn)行配制��,應(yīng)在A級(jí)環(huán)境下對(duì)剩余無(wú)菌物料進(jìn)行密封�,若配制后藥液經(jīng)除菌過(guò)濾,則應(yīng)在A級(jí)送風(fēng)下對(duì)剩余物料進(jìn)行密封�。專人確認(rèn)后進(jìn)行退庫(kù)/處理。對(duì)于已開封剩余物料的包裝流程和密封效果轉(zhuǎn)移及再次使用流程應(yīng)有相關(guān)研究和要求�。
(2)生產(chǎn)結(jié)束后進(jìn)行濾芯完整性測(cè)試,使用前可通過(guò)風(fēng)險(xiǎn)評(píng)估確定濾芯完整性測(cè)試的必要性����。工器具拆卸��、清洗�、消毒����、滅菌��。
(3)崗位清場(chǎng)�,各設(shè)施、設(shè)備��、工器具拆卸��、清洗�、消毒、滅菌��。
(4)配制系統(tǒng)在線清洗 (CIP) 和在線滅菌 (SIP) 等�。
表 6-5 配制崗位日常生產(chǎn)監(jiān)控點(diǎn)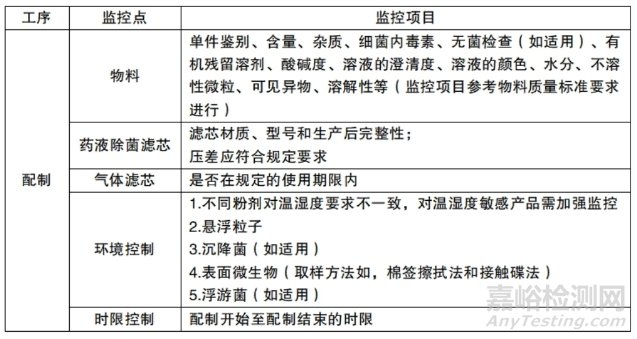
來(lái)源: 藥品GMP指南第2版無(wú)菌制劑上冊(cè) (P164-166)

