引言
外周血管疾?�。≒eripheral Artery Disease����,PAD)是指除了冠狀動脈和顱內(nèi)血管之外的血管病變�,包括上肢動脈、內(nèi)臟動脈����、下肢動脈����、弓上動脈分支及主動脈等��,其病理機制主要為動脈粥樣硬化性血管狹窄[1]�。在全球范圍內(nèi)����,有2億多人存在不同程度的PAD[2]。PAD常見的治療方式包括藥物治療��、手術(shù)治療和腔內(nèi)治療����,腔內(nèi)治療又可分為球囊成形術(shù),又稱經(jīng)皮腔內(nèi)血管成形術(shù)(Percutaneous Transluminal Angioplasty����,PTA)、支架植入術(shù)(裸金屬支架和藥物洗脫支架)��、斑塊切除術(shù)��、藥物涂層球囊(Drug-Coated Balloon�,DCB)等 [2-5],由醫(yī)生根據(jù)患者病情選擇治療方式。球囊成形術(shù)是將球囊擴張導管沿導絲軌道送達動脈的靶病變處��,利用球囊加壓充盈后產(chǎn)生膨脹力而使狹窄的動脈擴張的一種介入治療方法��。自1977年�,臨床開始使用球囊擴張導管(以下簡稱為球囊)行PTA[6],其在冠狀動脈血管疾病和PAD的治療中發(fā)揮重要作用�。球囊根據(jù)設計特性可分為順應性、半順應性和非順應性3種類型����,根據(jù)特殊功能又可分為普通球囊和修飾性球囊,修飾性球囊一般指切割球囊(顯微刀片)����、棘突球囊(尼龍棘突狀)和雙導絲球囊(金屬絲)等[7]。對于輕中度鈣化等高阻力病變��,修飾性球囊能夠使內(nèi)膜鈣化破裂����,改善對鈣化病變的擴張效果。普通球囊對于斑塊的無序擴張造成的撕裂容易導致夾層血腫�,增加血管急性閉塞風險,而修飾性球囊擴張后可引導斑塊撕裂多發(fā)生在血管長軸方向��,減少限流性夾層形成;修飾性球囊擴張易固定于斑塊表面����,避免球囊滑脫��?�?毯矍蚰沂菍㈡団伜辖鸾z����,螺旋狀地環(huán)繞在球囊外表面,其工作原理與雙導絲球囊類似��,也是修飾性球囊的一種��。
美國食品藥品監(jiān)督管理局(Food and Drug Administration����,F(xiàn)DA)將應力集中程度更接近于刀片的球囊稱為切割球囊,應力分布更接近于導絲或普通球囊的導絲球囊����、棘突球囊稱為刻痕球囊,但未明確區(qū)分兩類球囊的應力閾值����,將外周刻痕或切割球囊產(chǎn)品分類為Ⅱ類器械�,通過510(k)路徑注冊[8]�。我國在相關(guān)醫(yī)療器械產(chǎn)品注冊審評審批中,一般認為用于冠脈的����、對斑塊有修飾作用的修飾球囊(刻痕、切割等)需考慮臨床試驗路徑�。隨著外周血管修飾球囊臨床應用的增多,如何確保上市產(chǎn)品的安全性和有效性����,關(guān)系到人民群眾的健康和行業(yè)的發(fā)展,也對科學監(jiān)管提出了更高的要求����。本文擬從刻痕或切割球囊的工作原理、臨床應用出發(fā)�,綜述這類產(chǎn)品的特點,并結(jié)合現(xiàn)行的監(jiān)管框架和要求�,旨在從臨床評價的角度總結(jié)產(chǎn)品審評和審批的思考。
切割球囊由非順應性球囊及黏附表面的縱向平行排列的顯微刀片組成��,刀片切開斑塊����,產(chǎn)生縱向切口�。由于切割球囊與病變的接觸面是由不銹鋼制成的刀片����,局部作用力大,易于切開堅硬的病灶����,但存在造成意外損傷的風險��。
雙導絲球囊由導絲和球囊組成�,兩根導絲縱向平行排列,黏附于球囊的表面�,其結(jié)構(gòu)簡單,類似于醫(yī)生在普通球囊旁放置額外的引導導絲�,但導絲易隨著球囊滑動,不易固定于血管壁�。
1、 刻痕或切割球囊的發(fā)展
球囊擴張導管通過遠端球囊膨脹����,擠壓血管的斑塊,拉伸血管壁��,達到減少血管狹窄的目的,但也可能伴隨如血管內(nèi)膜撕裂����、血管彈性回縮等并發(fā)癥。對于堅硬的狹窄病變(如鈣化病變)��,通常需要提高球囊的充盈壓力����,才能減輕狹窄程度,獲得足夠的管腔容積��。而充盈壓力的增加����,會使血管壁的拉伸作用增加,導致出現(xiàn)血管損傷相關(guān)并發(fā)癥(如嚴重夾層��、回彈)的可能性更大����。對于特別頑固堅硬的病變,可能將球囊充盈至接近爆破壓�,仍無法壓縮斑塊。
醫(yī)生發(fā)現(xiàn)�,在球囊外再置入一條額外的伴行導絲 [9]����,當球囊膨脹時�,外部伴行導絲與狹窄病變(如鈣化病變)交界處,因局部壓強較大��,形成壓槽�,隨著球囊繼續(xù)膨脹,根據(jù)彈性力學的理論�,槽底部位會出現(xiàn)局部應力集中的現(xiàn)象,即壓力聚焦作用�,從而有效地壓碎硬的斑塊�,擴張血管,達到減少血管狹窄的目的����。這種方法被稱為雙導絲技術(shù)[9]。1995年��,Sandeep等[10] 報告使用導引導絲輔助球囊成形術(shù)的效果�,對美國心臟病學院/美國心臟協(xié)會A或B型病變行經(jīng)皮冠狀動脈腔內(nèi)血管成形術(shù),使用雙導絲技術(shù)時�,球囊充盈壓為435697.5Pa,最終殘余狹窄率為21% ��;不使用雙導絲技術(shù)時,球囊充盈壓為678877.5Pa�,最終殘余狹窄率為29%,存在顯著差異(P=0.001)��。
刻痕球囊和雙導絲球囊等產(chǎn)品的設計理念都源于雙導絲技術(shù)��,主要將導絲與球囊相結(jié)合����,形成一個整體。醫(yī)生遇到復雜的纖維鈣化病變或難以擴張病變時��,無須在普通球囊旁邊放置額外的引導導絲��,簡化了臨床操作�。
2、 刻痕或切割球囊的組成和特點
刻痕球囊由修飾性組件(導絲)和球囊組成�,導絲由鎳鈦合金制成,表面經(jīng)電拋光��,與鎳鈦合金的支架相似����,呈螺旋狀,繞在球囊的外表面��。球囊未充盈時,貼附于球囊的表面��,使刻痕球囊擁有與普通球囊類似的通過性��。球囊充盈后����,導絲呈螺旋狀貼附于血管壁,起到類似于螺絲的固定作用��,防止球囊的滑動����。
切割球囊由非順應性球囊及黏附表面的縱向平行排列的顯微刀片組成,刀片切開斑塊�,產(chǎn)生縱向切口��。由于切割球囊與病變的接觸面是由不銹鋼制成的刀片�,局部作用力大,易于切開堅硬的病灶�,但存在造成意外損傷的風險。
雙導絲球囊由導絲和球囊組成��,兩根導絲縱向平行排列��,黏附于球囊的表面,其結(jié)構(gòu)簡單����,類似于醫(yī)生在普通球囊旁放置額外的引導導絲,但導絲易隨著球囊滑動����,不易固定于血管壁。
3����、 刻痕或切割球囊的臨床應用
刻痕或切割球囊在不同外周血管病變的臨床應用的專家共識中存在差異,在一些病變中��,刻痕或切割球囊作為輔助治療(預處理或病變準備)方式�,而對于某些病變,刻痕或切割球囊可作為供選擇的治療方式��。
3.1 輔助治療(預處理或病變準備)
3.1.1 腎動脈狹窄
2017年�,中國醫(yī)療保健國際交流促進會血管疾病高血壓分會發(fā)布了《腎動脈狹窄的診斷和處理中國專家共識》[11],對于大動脈炎引起的非粥樣硬化性腎動脈狹窄(Renal Artery Stenosis����,RAS)的患者,共識指出PTA未成功患者包括球囊擴張后病變即刻發(fā)生彈性回縮或夾層,病變堅硬難以充分擴張����,導致影像結(jié)果不滿意。在該類患者中��,選擇性支架置入術(shù)或加用切割球囊擴張可能是備選的治療方式之一��,針對上述情形�,切割球囊可作為預處理治療選擇方式。對于粥樣硬化性 RAS患者共識指出��,介入治療方法包括PTA和支架置入術(shù)����,該共識建議粥樣硬化性RAS要獲得滿意的血管重建和減少再狹窄率應常規(guī)使用支架置入,但對于小部分不適合支架置入的病變?nèi)钥刹捎们蚰覕U張術(shù)治療�,在此情形下,刻痕和切割球囊可作為支架置入前的預處理器械����。在上述情形下��,使用刻痕或切割球囊擴張后��,減輕了病變部位的堅硬度,減少了發(fā)生回縮或夾層的發(fā)生��,然后醫(yī)生根據(jù)擴張效果進行后續(xù)的支架置入操作��。
3.1.2 部分股腘動脈病變預擴張治療
2018 年����,美國心血管造影和介入學會(Society for Cardiovascular Angiography and Interventions,SCAI)����,發(fā)布了《股腘動脈介入治療中器械選擇的SCAI共識指南》[12],共識指南指出��,在臨床實踐中����,特殊球囊多作為股腘動脈(Femoral-Popliteal,F(xiàn)P)疾病的輔助治療(病變準備)器械����,特殊球囊輔助治療的病變?nèi)绫?所示,刻痕或切割球囊作為特殊球囊預期可治療或輔助治療嚴重鈣化和難以擴張病變����。目前對于病變準備尚無明確定義�,但有多種不同的方法和技術(shù)[13]��。病變準備可用作單獨的治療目的��,但更多的是作為最終治療器械(如DCB或支架)使用前的輔助準備����。病變準備的工具包括減容器械,例如�,定向斑塊切除術(shù)、旋磨術(shù)或旋切術(shù)����、激光消蝕,以及血管內(nèi)碎石術(shù)����。除上述器械以外,還有一些特殊球囊����,如切割球囊、聚力球囊和斑塊修飾球囊�,這些特殊球囊可以作為簡單易用的工具來準備病變。
設計這些特殊球囊是為了更可控的擴張動脈粥樣硬 化斑塊����,從而達到更高的即刻技術(shù)成功率(彈性回彈更 少、球囊滑動更少�、夾層更少),并發(fā)癥發(fā)生率更低(穿 孔更少)��,提高抗增殖藥物的滲透��,與普通球囊血管成 形術(shù)相比更高的手術(shù)通暢率的目的�。它們既可以單獨作 為最終治療器械,也可以在其他最終治療器械前作為輔 助器械使用�。
3.2 病變治療
3.2.1 動靜脈內(nèi)瘺術(shù)中的血管狹窄
2019 年,中國醫(yī)院協(xié)會血液凈化中心分會血管通路
工作組發(fā)布了《中國血液透析用血管通路專家共識(第 2 版)》[14]����,對于自體動靜脈內(nèi)瘺狹窄的治療,共識指出 可應用高壓球囊導管����、超高壓球囊導管及特殊球囊導管 (如帶導絲球囊導管、切割球囊導管����、藥物洗脫球囊導管、 棘突球囊導管等)[15]��。對于動靜脈瘺狹窄的治療,切割 球囊導管及帶導絲的特殊球囊導管可作為臨床治療方式之一����。
在以下情況時可以考慮支架植入:① 血管成形術(shù)后彈性回縮(殘余狹窄超過50%);② 3個月內(nèi)狹窄復發(fā)�。即球囊擴張效果滿意 :殘余狹窄<50%且不影響血流的夾層,則使用產(chǎn)品后無須進一步處理�,或球囊擴張效果滿意:無彈性回縮、殘余狹窄 <50%且預期3個月內(nèi)狹窄不會復發(fā)�,則使用切割球囊導管及帶導絲的特殊球囊 產(chǎn)品后無須支架進一步處理。
3.2.2 部分股腘動脈病變
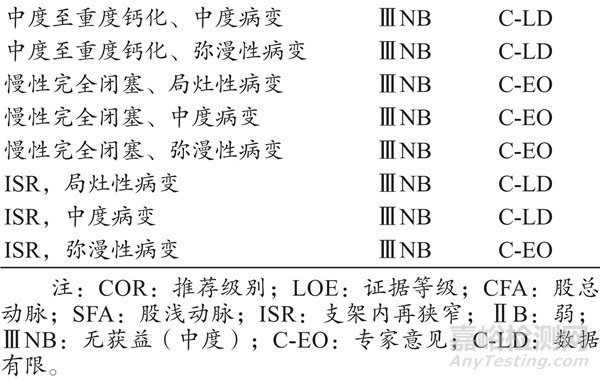
基于有限的已發(fā)表數(shù)據(jù)[16-22]����,可單獨使用特殊球囊(刻痕球囊、外周切割球囊等)治療FP疾病��,推薦情況 如表2所示��。
4����、 刻痕或切割球囊器械注冊審評思考
根據(jù)相關(guān)專家共識和指南,刻痕或切割球囊作為特殊球囊預期可治療或輔助治療嚴重鈣化和難以擴張病變[12]��。在臨床實踐中�,刻痕或切割球囊可以作為血管病變預處理或最終治療方式�。
根據(jù)應用部位的區(qū)分����,常見的有冠脈刻痕或切割球囊和外周刻痕或切割球囊�。外周刻痕或切割球囊的適用范圍通常為預期用于擴張髂動脈、股動脈��、髂股動脈�、腘動脈、腘下動脈和腎動脈內(nèi)的病變����,并用于自體或人工動靜脈透析瘺管的阻塞性病變的治療。冠脈刻痕或切割球囊的風險較外周刻痕或切割球囊高����,但作用機理類似,本文對冠脈刻痕或切割球囊的注冊審評思路進行了總結(jié)����。
4.1 外周刻痕或切割球囊臨床評價
美國FDA將外周PTA刻痕或切割球囊分為Ⅱ類器械,通過510(k)路徑注冊[23]�,刻痕或切割球囊可通過鈣化實驗室模型、具有鈣化病變的動物模型�、尸體模型和/或臨床試驗證明刻痕或切割器械的安全有效性����。
根據(jù)我國現(xiàn)行的注冊監(jiān)管要求����,外周刻痕或切割球囊為Ⅲ類器械,臨床評價可以基于申報產(chǎn)品自身的臨床試驗數(shù)據(jù)����,也可以基于同品種產(chǎn)品的臨床資料。當通過同品種臨床評價路徑時�,選擇的同品種產(chǎn)品應為已上市的,具有基本相同的預期用途和相似技術(shù)特征的產(chǎn)品�。
對比申報產(chǎn)品和同品種產(chǎn)品在適用范圍以及臨床使用相關(guān)信息的相同性和差異性,建議重點考慮以下內(nèi)容:適應證��、適用部位及血管類型以及使用方法��、禁忌證等�。技術(shù)特征的對比需考慮:① 基本原理,包括聚力原理等����;② 結(jié)構(gòu)組成,重點關(guān)注刻痕組件的設計及規(guī)格參數(shù),提供各組件的尺寸�、公差和工程圖紙等 ;③ 制造材料����,與人體直接或間接接觸的原材料 ;④ 性能要求����,常用需進行對比的性能要求包括 :尺寸(球囊直徑�、球囊長度、導管軸的工作長度��、兼容的導絲及導引導管)��、壓力(標稱壓力��、額定爆破壓力)��、涂層性能����、刻痕組件相關(guān)性能(如刻痕或切割組件的牢固性、防滑性能等)����。
上述對比內(nèi)容的差異可通過性能����、涂層性能����、防滑性能、尺寸�、壓力臺架試驗、動物試驗(可為無病理模型)的驗證論述等同性��,需要注意的是刻痕或切割球囊對于斑塊的擴張效果需要提供能夠模擬臨床的驗證方法����,例如,鈣化實驗室模型�、具有鈣化病變的動物模型、符合法規(guī)要求的尸體試驗模型和/或臨床試驗�。美國FDA對于動物試驗和/或尸體試驗研究一般關(guān)注器械的輸送通過性能、可跟蹤性�、對血管壁的損傷,包括夾層的發(fā)生率及嚴重程度�、血栓及穿孔的發(fā)生率,鈣化病變的擴張治療效果�,需在動物試驗和/或尸體試驗的研究方案中給出接受標準。
考慮到冠狀動脈與外周動脈管脈系統(tǒng)存在一定的相似性,如血管壁各層(內(nèi)膜����、中膜及外膜)的厚度相當、動脈粥樣硬化斑塊的成分及病理進程相似����、冠狀動脈與外周膝下動脈的血管直徑相近,但冠狀動脈相較外周動脈血管并發(fā)癥風險更高(如冠脈動脈血管穿孔可能導致心包填塞����、心梗等需進行緊急開胸手術(shù),而外周動脈可通過加壓或止血帶或相對直觀的外科手術(shù)控制并發(fā)癥)����。設計特征相同的冠狀動脈產(chǎn)品臨床使用中的安全有效性數(shù)據(jù)(如臨床試驗數(shù)據(jù))��,可以作為外周動脈產(chǎn)品臨床應用安全有效性的重要支持證據(jù)的一部分����。
與同品種產(chǎn)品詳細對比,所有差異均應逐一分析��,提供支持性資料�,并提交相應非臨床或臨床證據(jù)證明該差異不對產(chǎn)品的臨床使用產(chǎn)生不利影響,相關(guān)內(nèi)容需符合《醫(yī)療器械臨床評價技術(shù)指導原則》[24]。
4.2 冠脈刻痕或切割球囊臨床評價
冠脈刻痕或切割球囊的臨床評價方式一般采用臨床試驗路徑�。試驗設計應參考《醫(yī)療器械臨床試驗設計指導原則》[25] 的相關(guān)要求。例如��,可采用前瞻性����、單組目標值的臨床試驗設計。主要評價指標可考慮從如下幾個方面選擇:① 安全性指標�,主要為術(shù)后14d內(nèi)無主要心血管不良事件)事件率,主要有效性終點為手術(shù)成功率(術(shù)后即刻殘余直徑狹窄≤50%��,圍術(shù)期無死亡��、MI心肌梗死��、冠脈搭橋術(shù)[26-27]�;② 器械成功率,包括試驗球囊能夠成功輸送��、擴張��、收縮和撤出�,術(shù)后即刻無血管穿孔、限流性夾層(C級以上)或與試驗球囊有關(guān)的心肌梗死溶栓(Thrombolysis In Myocardial Infarction�,TIMI)血流減少(相較基線)�,經(jīng)皮冠狀動脈介入治療(Percutaneous Coronary Intervention�,PCI)術(shù)后即刻TIMI血流分級為3級 [28]。
次要有效性及安全性評價指標可考慮 :① 器械使用成功率(成功輸送�、擴張、收縮和撤出�,且擴張后殘余病變狹窄<50%);② 30 d 內(nèi)靶病變失敗復合終點��,即出現(xiàn)心源性死亡��、靶病變相關(guān)的心肌梗死及臨床驅(qū)動的靶病變血運重建 �;③ 術(shù)后30d內(nèi)患者相關(guān)的心血管臨床復合終點,包括全因死亡����、有所心肌梗死以及任何再次血運重建 ;④ 器械操作使用性能評價 ��;⑤ 術(shù)后即刻的手術(shù)成功率�,即PCI術(shù)后靶病變的管腔狹窄<20%����,TIMI血流3級,且圍手術(shù)期無心源性死亡�、靶病變MI或臨床驅(qū)動的血運重建 [29] ��;⑥ 夾層發(fā)生率和夾層類 ��;⑦ 不良事件等����。
臨床試驗目標值/界值以及樣本量應當綜合當前臨床診療實際(如參考臨床指南�、專家共識或臨床文獻薈萃分析等)和產(chǎn)品自身設計特征科學設定。球囊各型號規(guī)格在臨床試驗中的確認����,一般可考慮四角矩陣的原則,即長度�,直徑最長、最短�、最大、最小的組合�。申請人聲稱的各種特殊病變類型(如慢性完全閉塞病變、血管內(nèi)再狹窄����、原位小血管等)宜納入臨床試驗分組中,并給出各特殊病變的亞組結(jié)果��。
5�、 總結(jié)與展望
在全球范圍內(nèi)��,刻痕或切割球囊已成為介入治療中重要的醫(yī)療器械��。根據(jù)相關(guān)專家共識和指南�,刻痕或切割球囊在臨床使用中可以作為輔助準備治療(預處理)或最終治療�。該類產(chǎn)品在中國和美國的注冊監(jiān)管審評中,冠脈刻痕或切割球囊的臨床評價����,一般采用臨床試驗。外周刻痕或切割球囊的臨床評價�,可基于臨床試驗,也可基于同品種的臨床資料��,還可將設計特征相同的冠狀動脈產(chǎn)品臨床安全有效性數(shù)據(jù)��,作為外周動脈產(chǎn)品臨床安全有效性的一部分支持證據(jù)����。隨著人民對醫(yī)療和健康的要求日益提高,新的醫(yī)療器械不斷涌現(xiàn)����,在審評過程中�,充分了解產(chǎn)品的作用機理����、結(jié)構(gòu)和組成和臨床應用����,才能準確地判斷臨床證據(jù)的可接受性和可外推性。同時��,吸收和借鑒美國�、歐盟、日本等國家或地區(qū)的審評思路和經(jīng)驗��,也是優(yōu)化和擴展審評思路的有效途徑����。以更有效地促進國內(nèi)醫(yī)療器械產(chǎn)業(yè)的發(fā)展,更好地為人民群眾的健康服務�。
[參考文獻]
[1] 苗雨晴, 李擁軍. 藥物涂層球囊在外周血管疾病中的應用及展望[J]. 中國臨床醫(yī)生雜志, 2020, 48(8): 898-900.
[2] Kokkinidis DG, Armstrong EJ. Armstrong, emerging and futuretherapeutic options for femoropopliteal and infrapoplitealendovascular intervention[J]. Interv Cardiol Clin, 2017, 6(2):279-295.
[3] van der Vijver-Coppen RJ, Mannetje YW, Menting TP, et al.Treating complex femoropopliteal lesions[J]. J CardiovascSurg, 2018, 59(2): 158-163.
[4] Bradbury AW, Adam DJ, Bell J, et al. Bypass versusAngioplastyin Severe Ischaemia of the Leg (BASIL) trial:a survival predic tion model to facilitate clinical decisionmaking[J]. J Vasc Surg, 2010, 5195(l): 52S-68S.
[5] Adam DJ, Beard JD, Cleveland T, et al. Bypass versusangioplasty in severe ischaemia of the leg (BASIL):multicentre, randomised controlled trial[J]. Lancet, 2005,366(9501): 1925-1934.
[6] Grüntzig A. Transluminal dilatation of coronary arterystenosis—experimental report[R]. Heidelberg: PercutaneousVascular Recanalization , 1978: 263.
[7] 國家衛(wèi)生健康委. 國家衛(wèi)生健康委辦公廳關(guān)于印發(fā)冠狀動脈球囊成形術(shù)與支架植入術(shù)操作規(guī)范(2022年版)和髖膝關(guān)節(jié)置換術(shù)操作規(guī)范(2022年版)的通知(國衛(wèi)辦醫(yī)函〔2022〕77號) [EB/OL]. (2022-03-21) [2022-11-21]. http://www.nhc.gov.cn/yzygj/s7659/202203/d5cb0d71f5db461da0097c54b8296814.shtml.
[8] U.S. Food and Drug Administration. Peripheral percutaneoustransluminal angioplasty (PTA) and specialty catheters -premarket notification (510(k)) submissions draft guidancefor industry and food and drug administration staff (FDA2019-D-5422)[EB/OL]. (2020-01-13)[2022-11-21]. https://www.fda.gov/regulatory-information/search-fda-guidancedocuments/peripheral-percutaneous-transluminal-angioplastypta-and-specialty-catheters-premarket-notification.
[9] Carlson TA, Teirstein PS. The “Concorde” stent: a novel use ofa stiff bent guidewire to facilitate stent deployment[J]. CathetCardiovasc Diagn, 1997, 40(3): 277-280.
[10] Sandeep K, Donovan B, Theodore S, et al. Facilitated lumenen largement by longitudinal force focused angioplasty[J]. JInvasive Cardiol, 1995, 25(2): 345A-346A.
[11] 中國醫(yī)療保健國際交流促進會血管疾病高血壓分會專家共識起草組. 腎動脈狹窄的診斷和處理中國專家共識[J]. 中國循環(huán)雜志, 2017, 32(9): 835-842.
[12] Dmitriy N. Feldman EJ, Aronow HD, et al. SCAI consensusguidelines for device selection in femoral-popliteal arterialinterventions[J]. Catheter Cardiovasc Interv, 2018, 92: 124-140.
[13] Blessing E, Lugenbiel I, Holden A. The evidence to supportthe use of focal force balloon technology to improve outcomesin the treatment of lower extremity arterial occlusive disease[J].J Cardiovasc Surg, 2019, 60(1): 14-20.
[14] 中國醫(yī)院協(xié)會血液凈化中心分會血管通路工作組. 中國血液透析用血管通路專家共識(第2版)[J]. 中國血液凈化, 2019,18(6): 365-381.
[15] Nikam MD, Ritchie J, Jayanti A, et al. Acute arteriovenousaccess failure: long-term outcomes of endovascular salvage andassessment of co-variates affecting patency[J]. Nephron, 2015,129(4): 241-246.
[16] Poncyljusz W, Falkowski A, Safranow K, et al. Cuttingballoon angioplasty versus balloon angioplasty as treatment forshort atherosclerotic lesions in the superficial femoral artery:randomized controlled trial[J]. Cardiovasc Intervent Radiol,2013, 36: 1500-1507.
[17] Amighi J, Schillinger M, Dick P, et al. De novo superficialfemoro-popliteal artery lesions: peripheral cutting balloonangioplasty and restenosis rates -randomized controlled trial[J].Radiology, 2008, 247: 267-272.
[18] Canaud L, Alric P, Berthet JP, et al. Infrainguinal cuttingballoon angioplasty in de novo arterial lesions[J]. J Vasc Surg,2008, 48: 1182-1188.
[19] Cotroneo AR, Pascali D, Iezzi R. Cutting balloon angioplastyin short femoropopliteal arterial stenoses[J]. J Endovasc Ther,2008, 15: 283-291.
[20] Dick P, Sabeti S, Mlekusch W, et al. Conventional balloonangioplasty verses peripheral cutting balloon angioplasty fortreatment of femo- ropoliteal artery in-stent restenosis: initialexperience[J]. Radiology, 2008, 248: 297-302.
[21] Peeters P J, Bosiers M, Scheinert D, et al. Role of theAngioSculpt scoring balloon catheter for the treatment offemoro-popliteal disease: 1-year results from the MASCOTTrial[J]. Cardiovasc Revasc Med, 2010, 11(4): 272-273.
[22] Bouras G, Lansky A, McClure J, et al. Outcomes from thechocolate BAR: a large, multicenter, prospective, post-market study on use of the chocolate percutaneous transluminalangioplasty (PTA) balloon[J]. J Am Coll Cardiol, 2016, 68:B314.
[23] U.S. Food and Drug Administration. Certain PercutaneousTransluminal Coronary Angioplasty (PTCA) Catheters - ClassⅡ SpecialControls Guidance for Industry and FDA[EB/OL].(2010-09-08)[2022-11-21]. https://www.fda.gov/medicaldevices/guidance-documents-medical-devices-and-radiationemitting-products/certain-percutaneous-transluminal-coronaryangioplasty-ptca-catheters-class-Ⅱ-special-controls.
[24] 國家藥品監(jiān)督管理局醫(yī)療器械技術(shù)審評中心. 國家藥監(jiān)局關(guān)于發(fā)布醫(yī)療器械臨床評價技術(shù)指導原則等5項技術(shù)指導原則的通告(2021年第73號)[EB/OL]. (2021-09-28)[2022-11-21]. https://www.cmde.org.cn/flfg/zdyz/fbg/fbgqt/20210929092409574.html.
[25] 國家藥品監(jiān)督管理局醫(yī)療器械技術(shù)審評中心. 總局關(guān)于發(fā)布醫(yī)療器械臨床試驗設計指導原則的通告(2018年第6號)[EB/OL]. (2018-01-04)[2022-11-21]. https://www.cmde.org.cn/flfg/zdyz/fbg/fbgqt/20180205150300135.html.
[26] U.S. Food and Drug Administration. Premarket approval(PMA)-P050018 AngioSculpt® Evo RX PTCA scoring balloon catheter with hydrophilic coating[EB/OL]. (2021-12-23)[2022-11-21]. https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfpma/pma.cfm?id=P050018S030.
[27] U.S. Food and Drug Administration. Premarket approval(PMA)- p020037 FX minirail RX percutaneous transluminalcoronary angioplasty (PTCA) catheter [EB/OL]. (2003-06-11) [2022-11-21]. https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfpma/pma.cfm?id=P020037.
[28] U.S. Food and Drug Administration. Premarket approval(PMA)- P200041 scoreflex NC scoring PTCA catheter [EB/OL]. (2021-12-21)[2022-11-21]. https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfpma/pma.cfm?id=P200041.
[29] 朱丹丹, 高婧, 夏慧琳, 等. 切割球囊系統(tǒng)在治療冠狀動脈血管疾病中的有效性和安全性分析[J]. 中國醫(yī)學裝備, 2022,4(19): 49-53.
Zhu DD, Gao J, Xia HL, et al. Analysis on the effectivenessand safety of cutting balloon system in the treatment of vasculardisease of coronary artery[J]. China Med Equip, 2022, 4(19):49-53.本