今日頭條
濟(jì)民可信抗耐藥抑菌劑獲批臨床���。濟(jì)民可信旗下杭煜制藥1類(lèi)化藥注射用JMKX003801獲國(guó)家藥監(jiān)局臨床許可���,擬開(kāi)發(fā)用于治療革蘭陰性菌引起的嚴(yán)重感染。據(jù)悉�,JMKX003801在機(jī)制上可以很好地克服現(xiàn)有碳青霉素出現(xiàn)的耐藥,臨床前研究表明具有抗菌譜廣的特點(diǎn)���,預(yù)期能夠解決現(xiàn)有臨床上抗生素的耐藥問(wèn)題���。
國(guó)內(nèi)藥訊
1.再鼎DLL3-ADC上Ⅰ期臨床���。再鼎醫(yī)藥靶向DLL3的ADC藥物ZL-1310(YL212)在Clinicaltrials.gov網(wǎng)站上注冊(cè)一項(xiàng)美國(guó)Ⅰ期臨床�����,計(jì)劃入組140例小細(xì)胞肺癌(SCLC)患者���,評(píng)估ZL-1310治療的安全性與有效性�����。該項(xiàng)試驗(yàn)預(yù)計(jì)2027年完成�。YL212是基于宜聯(lián)生物自有的TMALIN®平臺(tái)開(kāi)發(fā)的1類(lèi)生物藥���,再鼎醫(yī)藥擁有YL212的全球開(kāi)發(fā)及商業(yè)化獨(dú)家授權(quán)�。12月上旬�����,該新藥的中國(guó)IND申請(qǐng)已獲得CDE受理�����。
2.愛(ài)科諾RIPK1抑制劑獲孤兒藥資格。愛(ài)科諾生物創(chuàng)新藥AC-003膠囊獲FDA授予孤兒藥資格�,用于治療急性移植物抗宿主病。這是一款RIPK1抑制劑���,能夠保持移植物抗白血病活性(GVL)�,不會(huì)引起免疫抑制�,對(duì)造血細(xì)胞沒(méi)有負(fù)面影響。在中美同時(shí)開(kāi)展的I期臨床中���,AC-003顯示出良好的安全性和耐受性���。該新藥也正被開(kāi)發(fā)用于治療特發(fā)性肺纖維化(IPF)。
3.寧丹新藥改良型鎮(zhèn)痛復(fù)方獲批臨床�。寧丹新藥改良型新藥Y-4片獲FDA批準(zhǔn)開(kāi)展I期臨床,針對(duì)的適應(yīng)癥為“神經(jīng)病理性疼痛”�。臨床前研究表明,Y-4復(fù)方組合在多個(gè)神經(jīng)痛動(dòng)物模型中可發(fā)揮協(xié)同增效作用���,鎮(zhèn)痛藥效顯著�,且安全性良好���、藥代性質(zhì)合理�,有望為多種類(lèi)型神經(jīng)病理性疼痛患者提供新的治療選擇。
4.上海元宋溶瘤病毒獲FDA臨床許可�。上海元宋生物自主研發(fā)的溶瘤病毒抗癌藥物“重組L-IFN腺病毒注射液”獲FDA批準(zhǔn)開(kāi)展新藥研究。重組L-IFN腺病毒注射液(YSCH-01)利用具有靶向腫瘤雙重調(diào)控的溶瘤腺病毒載體攜帶了抗癌多功能的重組免疫抗癌基因L-IFN���。在臨床前研究中���,YSCH-01在至少7個(gè)實(shí)體腫瘤類(lèi)別上抗癌效果顯著���,其抑瘤率達(dá)到90-100%�����。
5.諾和諾德PKR激動(dòng)劑中國(guó)報(bào)IND�����。諾和諾德1類(lèi)化藥etavopivat的臨床試驗(yàn)申請(qǐng)獲CDE受理�����。etavopivat是一款選擇性丙酮酸激酶-R(PKR)激動(dòng)劑,正被開(kāi)發(fā)用于治療鐮狀細(xì)胞貧血病(SCD)���。在Ⅰ期臨床中�����,etavopivat已顯示出具有改善紅細(xì)胞健康���、增加血紅蛋白含量、減少病患復(fù)發(fā)性血管閉塞危象(VOC)癥狀與改善患者生活品質(zhì)的潛力���,并具有良好的耐受性�。
6.瑞博PCSK9小核酸新藥授權(quán)齊魯制藥�。瑞博生物與齊魯制藥簽訂技術(shù)許可協(xié)議,將臨床早期抗PCSK9小核酸新藥RBD7022在大中華區(qū)(中國(guó)大陸�、香港及澳門(mén))的開(kāi)發(fā)、生產(chǎn)和商業(yè)化權(quán)利授權(quán)許可給齊魯制藥���。根據(jù)協(xié)議�����,瑞博生物將獲得總計(jì)超過(guò)7億元人民幣的首付款和里程碑付款���、以及最高兩位數(shù)的特許權(quán)使用費(fèi)率�。
國(guó)際藥訊
1.創(chuàng)新FcRn抗體格雷夫斯?、蚱谂R床積極。Immunovant公司FcRn單抗batoclimab治療格雷夫斯病的Ⅱ期臨床結(jié)果積極���。此前接受過(guò)抗甲狀腺藥物(ATD)治療的經(jīng)治患者接受batoclimab(680mg)治療1年后再接受batoclimab(340mg)為期12周治療�����。與batoclimab(340mg)相比�����,batoclimab(680mg)治療后患者的抗TSHR自身抗體的降幅更大(平均IgG降幅為81%);減少ATD劑量的患者比例和停用ATD的患者比例也更高�;且Batoclimab的耐受性總體良好。
2.“致幻蘑菇”治療PTSD啟動(dòng)Ⅱ期臨床���。Compass Pathways公司裸蓋菇素療法COMP360治療創(chuàng)傷后應(yīng)激障礙(PTSD)的Ⅱ期臨床結(jié)果積極���。患者接受單次COMP360(25mg)治療24小時(shí)后�,初步數(shù)據(jù)顯示COMP360耐受性良好�����,沒(méi)有治療伴發(fā)嚴(yán)重不良事件的報(bào)道。目前受試者正在接受為期12周的監(jiān)測(cè)���,其安全性和有效性數(shù)據(jù)預(yù)計(jì)將于2024年春季公布�。2018年�����,F(xiàn)DA已授予該產(chǎn)品用于治療難治性抑郁癥的突破性療法認(rèn)定�����。
3.Incyte公司KRAS G12D抑制劑上Ⅰ期臨床�����。Incyte公司KRAS G12D抑制劑新藥INCB161734在Clinicaltrials.gov網(wǎng)站上注冊(cè)一項(xiàng)Ⅰ期臨床���,擬評(píng)估INCB161734用于治療晚期實(shí)體瘤患者的安全性與初步療效�。該項(xiàng)試驗(yàn)終點(diǎn)探索的適應(yīng)癥包括胰腺癌、結(jié)直腸癌�、非小細(xì)胞肺癌。就在上個(gè)月�,阿斯利康以4.2億美元購(gòu)進(jìn)祐森健恒臨床前期小分子KRAS G12D抑制劑UA022的全球獨(dú)家開(kāi)發(fā)和商業(yè)化權(quán)益。目前�����,全球尚無(wú)KRASG12D抑制劑獲批上市�。
4.FDA拒絕加速批準(zhǔn)漸凍癥納米療法上市。Clene公司納米療法CNM-Au8用于治療肌萎縮側(cè)索硬化癥(ALS)的加速上市申請(qǐng)未獲得FDA批準(zhǔn)���。在II期研究(HEALEY ALS)中,與歷史數(shù)據(jù)集的匹配安慰劑受試者相比�,CNM-Au8(30mg)治療使死亡風(fēng)險(xiǎn)降低49%(p=0.046)���。Clene公司計(jì)劃明年上半年向FDA提供新的長(zhǎng)期療效數(shù)據(jù)及生物標(biāo)志數(shù)據(jù)�,并開(kāi)展CNM-Au8治療ALS的確證性III期臨床�����。
5.禮來(lái)擬5億美元開(kāi)發(fā)肥胖癥新靶點(diǎn)���。禮來(lái)與Fauna Bio公司將利用后者Convergence人工智能(AI)平臺(tái)�,針對(duì)多個(gè)藥物靶點(diǎn)合作開(kāi)發(fā)肥胖癥候選藥物�。Convergence整合了人類(lèi)患者數(shù)據(jù)和能天然抵抗疾病動(dòng)物的數(shù)據(jù)���,構(gòu)建了的生物醫(yī)學(xué)知識(shí)圖譜�����;并使用圖像神經(jīng)網(wǎng)絡(luò)(Graph Neural Network)挑選藥物靶點(diǎn)�����,使快速發(fā)現(xiàn)創(chuàng)新靶點(diǎn)成為可能���。根據(jù)協(xié)議,F(xiàn)auna Bio將獲得預(yù)付款���,總額高達(dá)4.94億美元的臨床前�����、臨床期和商業(yè)里程碑潛在付款。
6.強(qiáng)生超4億美元購(gòu)進(jìn)眼科基因療法���。強(qiáng)生將以高達(dá)4.15億美元收購(gòu)MeiraGTx公司臨床后期AAV基因療法botaretigene sparoparvovec(bota-vec,曾用名AAV-RPGR)的研發(fā)權(quán)益�����。Bota-vec目前已在治療X連鎖視網(wǎng)膜色素變性(XLRP)的Ⅲ期Lumeos臨床完成患者招募。根據(jù)協(xié)議,MeiraGTx將獲得1.3億美元的預(yù)付款和近期里程碑付款���。此外,MeiraGTx還有望在bota-vec在美國(guó)和歐盟首次商業(yè)銷(xiāo)售及制造技術(shù)轉(zhuǎn)讓成功后�����,獲得高達(dá)2.85億美元的里程碑付款�。
醫(yī)藥熱點(diǎn)
1.中國(guó)大學(xué)醫(yī)科實(shí)力評(píng)級(jí)發(fā)布。12月25日�,“軟科”正式發(fā)布2023年“中國(guó)大學(xué)醫(yī)科實(shí)力評(píng)級(jí)”。本次評(píng)級(jí)將學(xué)校在醫(yī)科領(lǐng)域入選第二輪“雙一流”建設(shè)的學(xué)科納入“學(xué)科實(shí)力”和“學(xué)科精度”維度���;在“科研平臺(tái)”維度新增“全國(guó)重點(diǎn)實(shí)驗(yàn)室”“國(guó)家醫(yī)學(xué)中心”“衛(wèi)生健康委員會(huì)重點(diǎn)實(shí)驗(yàn)室”等變量�。醫(yī)科實(shí)力全國(guó)前五名(相當(dāng)于醫(yī)科領(lǐng)域有得分高校的前2%)分別為上海交通大學(xué)�����、北京大學(xué)�����、北京協(xié)和醫(yī)學(xué)院���、浙江大學(xué)和復(fù)旦大學(xué)�����。
2.嚴(yán)禁公立醫(yī)院舉債購(gòu)置大型醫(yī)用設(shè)備�����。近日�����,國(guó)家衛(wèi)健委印發(fā)《關(guān)于進(jìn)一步加強(qiáng)公立醫(yī)院內(nèi)部控制建設(shè)的指導(dǎo)意見(jiàn)》指出���,強(qiáng)化資產(chǎn)管理,嚴(yán)格按規(guī)定程序配置各類(lèi)設(shè)備資產(chǎn)���,嚴(yán)禁舉債購(gòu)置大型醫(yī)用設(shè)備�,規(guī)范國(guó)有資產(chǎn)出租出借和處置行為���,落實(shí)定期清查盤(pán)點(diǎn)制度�。嚴(yán)格控制對(duì)外投資���,明確對(duì)外投資的可行性評(píng)估與投資效益分析等相關(guān)內(nèi)容�。
3.消化健康全國(guó)重點(diǎn)實(shí)驗(yàn)室在北京友誼醫(yī)院成立���。12月21日�,消化健康全國(guó)重點(diǎn)實(shí)驗(yàn)室揭牌儀式暨消化健康前沿醫(yī)學(xué)科技論壇在首都醫(yī)科大學(xué)附屬北京友誼醫(yī)院(通州院區(qū))舉行�����。實(shí)驗(yàn)室的總體目標(biāo)將圍繞消化健康領(lǐng)域的新藥物�、新器械、新策略�����、新體系�,完成六個(gè)重大研究任務(wù),培養(yǎng)醫(yī)學(xué)高層次人才�,開(kāi)拓消化研究領(lǐng)域,創(chuàng)造尖端技術(shù)產(chǎn)品���,形成消化健康診療新體系���,全面提高消化健康水平�����。
評(píng)審動(dòng)態(tài)
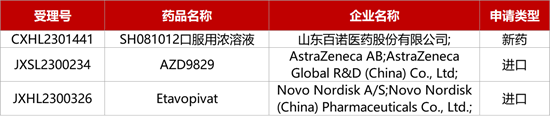
1. CDE新藥受理情況(12月25日)
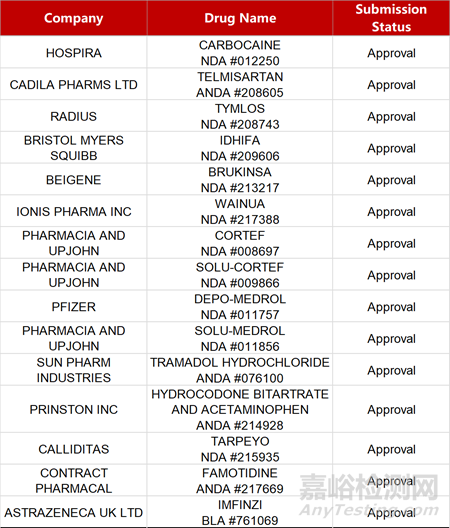
2. FDA新藥獲批情況(北美12月21日)