今日頭條
阿斯利康擬12億美元收購亙喜生物����。阿斯利康宣布已與亙喜生物簽署最終協(xié)議�,以約12億美元的總價(jià)格收購后者�。亙喜生物將作為阿斯利康全資子公司繼續(xù)在中國及美國運(yùn)營����。12月22日,亙喜生物靶向BCMA/CD19雙靶點(diǎn)自體FasTCAR-T產(chǎn)品GC012F已獲得CDE臨床許可�,擬開發(fā)用于治療難治性系統(tǒng)性紅斑狼瘡(SLE)。在美國�,F(xiàn)DA已批準(zhǔn)GC012F針對復(fù)發(fā)/難治性多發(fā)性骨髓瘤(R/R MM)和SLE開展Ⅰ/Ⅱ期臨床。
國內(nèi)藥訊
1.明濟(jì)Claudin18.2抗體啟動III期臨床��。明濟(jì)生物Claudin18.2抗體藥物M108在Clinicaltrials.gov官網(wǎng)注冊一項(xiàng)III期臨床�,擬評估M108聯(lián)合化療與安慰劑+化療對比,一線治療Claudin(CLDN)18.2陽性�、HER2陰性、PD-L1 CPS<5��、局部晚期或轉(zhuǎn)移性胃/GEJ腺癌的有效性和安全性��,M108能充分利用抗體的免疫學(xué)抗腫瘤機(jī)制��,通過增強(qiáng)型的ADCC效應(yīng)充分調(diào)動患者機(jī)體的免疫細(xì)胞來殺傷腫瘤細(xì)胞����。該項(xiàng)試驗(yàn)預(yù)計(jì)在2027年完成�。
2.信達(dá)瑪仕度肽啟動頭對頭III期臨床�。信達(dá)生物GLP-1R/GCGR激動劑IBI362(瑪仕度肽)登記啟動一項(xiàng)頭對頭III期臨床,擬評估IBI362與司美格魯肽相比��,用于經(jīng)單純飲食運(yùn)動干預(yù)伴/不伴二甲雙胍單藥治療血糖�、體重控制不佳的中國早期2型糖尿病合并肥胖受試者的療效和安全性。該項(xiàng)試驗(yàn)主要研究者由北京大學(xué)人民醫(yī)院醫(yī)學(xué)博士紀(jì)立農(nóng)擔(dān)任��。本月月初����,瑪仕度肽(9mg)已啟動了一項(xiàng)減重III期臨床。
3.深圳未知君FMT藥物獲批II期臨床��。未知君腸菌移植(FMT)藥物XBI-302獲FDA批準(zhǔn)開展II期臨床��,評估用于治療急性移植物抗宿主病(aGvHD)的有效性與安全性����。XBI-302將患者體內(nèi)遭破壞的腸道菌群置換成健康菌群,在不影響移植物抗宿主病治療的前提下����,幫助機(jī)體重建免疫系統(tǒng)��,最終實(shí)現(xiàn)減少疾病復(fù)發(fā)����、改善愈合����。
4.信達(dá)OX40L單抗啟動I期臨床����。信達(dá)生物靶向OX40L的新型免疫調(diào)節(jié)劑IBI356登記啟動一項(xiàng)I期臨床,擬評估IBI356首次在中國健康成人受試者中單次給藥和中重度特應(yīng)性皮炎成人受試者中多次給藥的安全性�、耐受性及藥代動力學(xué)特征。該項(xiàng)試驗(yàn)主要研究者由上海市皮膚病醫(yī)院醫(yī)學(xué)博士史玉玲和朱全剛共同擔(dān)任����。今年11月,CDE也批準(zhǔn)了該新藥針對特應(yīng)性皮炎的IND申請����。
5.阿斯利康CD123靶向ADC中國報(bào)IND。阿斯利康1類生物藥AZD9829的臨床試驗(yàn)申請獲CDE受理�。AZD9829是一款靶向CD123的拓?fù)洚悩?gòu)酶1抑制劑(TOP1i)-抗體偶聯(lián)藥物(ADC),能夠?qū)OP1i載荷遞送到表達(dá)CD123的癌細(xì)胞中��,導(dǎo)致DNA損傷和細(xì)胞凋亡。目前��,該新藥正在Ⅰ/Ⅱ期臨床中評估用于單藥或聯(lián)合治療CD123陽性血液惡性腫瘤患者的安全性和初步抗腫瘤活性����。
6.遠(yuǎn)大醫(yī)藥收購天津田邊75.35%股權(quán)。遠(yuǎn)大醫(yī)藥宣布與日本田邊三菱制藥株式會社簽訂股權(quán)收購協(xié)議�,將以約港幣4.0億元(等同約人民幣3.677億元)收購天津田邊制藥75.35%的股權(quán)。天津田邊主要從事心腦血管�、內(nèi)分泌代謝、胃腸道等慢性疾病領(lǐng)域高質(zhì)量原研藥品的生產(chǎn)與銷售�。本次收購是遠(yuǎn)大醫(yī)藥在心腦血管急救板塊的一次重大的產(chǎn)業(yè)布局。
國際藥訊
1.新冠/流感二聯(lián)mRNA疫苗啟動Ⅲ期臨床����。輝瑞與BioNTech聯(lián)合開發(fā)的針對新冠病毒病和流感的聯(lián)合修飾RNA候選疫苗在Clinicaltrials.gov網(wǎng)站上注冊一項(xiàng)Ⅲ期臨床,計(jì)劃入組7500例受試者��,評估聯(lián)合修飾RNA候選疫苗與已上市流感疫苗對比的的安全性�、耐受性和免疫原性,預(yù)計(jì)2024年8月完成��。輝瑞與BioNTech目前重點(diǎn)探索包括新冠/流感��、新冠/RSV�、流感/RSV�、新冠/流感/RSV等聯(lián)合疫苗�。
2.禮來Tirzepatide啟動降糖減重II期臨床。禮來GLP-1R/GIPR雙靶點(diǎn)激動劑Tirzepatide(替爾泊肽)在ClinicalTrials.gov官網(wǎng)注冊一項(xiàng)II期臨床����,擬評估與單獨(dú)使用胰島素相比,替爾泊肽與胰島素聯(lián)合治療1型糖尿病合并肥胖患者的有效性與安全性��。主要終點(diǎn)是受試者體重變化�。此前,替爾泊肽已獲FDA批準(zhǔn)用于治療2型糖尿病�,以及肥胖適應(yīng)癥����。
3.額顳葉癡呆基因療法早期臨床積極。Passage Bio公司基于AAV1載體的基因療法PBFT02在治療GRN基因突變��、額顳葉癡呆(FTD)患者的國際Ⅰ/Ⅱ期臨床獲積極結(jié)果�。前3例患者接受單劑PBFT02治療后30天,患者腦脊液中的PGRN水平較基線增加3.6-6.6倍(10.7-17.3ng/mL)��,高于健康成人對照組生理水平(3.3-8.2ng/mL)��;其中1例患者療效維持長達(dá)6個(gè)月��。此外,藥物耐受性良好����。
4.核苷酸DNA聚合酶抑制劑早期臨床積極。Medivir公司核苷酸DNA聚合酶抑制劑口服前藥Fostrox(Fostroxacitabine bralpamide)聯(lián)合激酶抑制劑Lenvima(lenvatinib)治療晚期肝細(xì)胞癌(HCC)經(jīng)治患者的Ⅰb/Ⅱa期臨床結(jié)果積極�。12周的隨訪期間,聯(lián)合治療的疾病控制率(DCR)達(dá)到80%��;超過75%患者的靶病灶縮?�?;聯(lián)合用藥總體耐受性良好,沒有出現(xiàn)新的安全性事件�。
5.賽諾菲終止CEACAM5靶向ADC開發(fā)。賽諾菲靶向癌胚抗原相關(guān)細(xì)胞粘附分子5(CEACAM5)的抗體偶聯(lián)藥物(ADC)tusamitamab ravtansine(SAR408701��,IBI-126)用于二線治療CEACAM5陽性轉(zhuǎn)移性非鱗狀非小細(xì)胞肺癌(nsqNSCLC)的III期CARMEN-LC03研究未達(dá)到主要終點(diǎn)����。與多西他賽相比,tusamitamab ravtansine單藥治療的患者總生存期 (OS) 顯示改善趨勢�,但未達(dá)到無進(jìn)展生存期(PFS)的雙重主要終點(diǎn)。目前����,賽諾菲已終止tusamitamab ravtansine的全球臨床開發(fā)計(jì)劃��。
6.AI蛋白質(zhì)藥物公司Cradle完成A輪融資����。基于人工智能設(shè)計(jì)和制造蛋白質(zhì)的生物技術(shù)公司Cradle宣布完成2400萬美元A輪融資����。本輪融資由Index Ventures領(lǐng)投,Kindred Capital參投����。Cradle的專有生成式人工智能模型是在數(shù)十億蛋白質(zhì)序列以及他們自己的實(shí)驗(yàn)室生成的數(shù)據(jù)基礎(chǔ)上訓(xùn)練而成的。目前�,該公司正在開展12個(gè)以上的研發(fā)項(xiàng)目,重點(diǎn)關(guān)注各種蛋白質(zhì)療法的工程設(shè)計(jì)�,包括酶����、疫苗、肽和抗體�。
醫(yī)藥熱點(diǎn)
1.羅鳳鳴任四川大學(xué)華西醫(yī)院院長。12月26日����,四川大學(xué)華西臨床醫(yī)學(xué)院(華西醫(yī)院)召開全院干部大會�,宣布四川大學(xué)領(lǐng)導(dǎo)任命決定:羅鳳鳴同志任四川大學(xué)華西臨床醫(yī)學(xué)院(華西醫(yī)院)院長�;因年齡原因,李為民同志不再擔(dān)任四川大學(xué)華西臨床醫(yī)學(xué)院(華西醫(yī)院)院長職務(wù)��。公開資料顯示��,羅鳳鳴����,1970年8月出生,研究生��,醫(yī)學(xué)博士����,中共黨員,教授����,博士生導(dǎo)師。曾任四川大學(xué)華西臨床醫(yī)學(xué)院(華西醫(yī)院)內(nèi)科黨總支書記����、黨委副書記、黨委常務(wù)副書記。
2.《第三批鼓勵(lì)仿制藥品目錄》發(fā)布��。近日�,國家衛(wèi)健委等部門發(fā)布《第三批鼓勵(lì)仿制藥品目錄》。第三批目錄收錄39個(gè)品種�,涉及75個(gè)品規(guī)、13種劑型����,覆蓋抗腫瘤藥及免疫調(diào)節(jié)劑、抗感染用藥��、神經(jīng)系統(tǒng)用藥����、放射性診斷劑、心血管系統(tǒng)用藥等12個(gè)方面治療用藥�。其中包括治療成人遺傳性轉(zhuǎn)甲狀腺素介導(dǎo)的淀粉樣變性的多發(fā)性神經(jīng)病的小干擾RNA藥品帕替司蘭,聯(lián)合免疫抑制劑治療成人活動性狼瘡腎炎的口服藥品伏環(huán)孢素等����。
3.人用疫苗����、部分抗癌藥、罕見病藥實(shí)施零關(guān)稅。12月21日�,國務(wù)院關(guān)稅稅則委員會發(fā)布公告,2024年將調(diào)整部分商品的進(jìn)出口關(guān)稅��。2024年1月1日起�,人用疫苗、部分抗癌藥��、罕見病藥的藥品和原料等實(shí)施零關(guān)稅�。此外,2024年還將對吸入用異丙托溴銨溶液實(shí)施零關(guān)稅�,該藥品在臨床上被廣泛用于兒童哮喘類疾病的治療。
評審動態(tài)
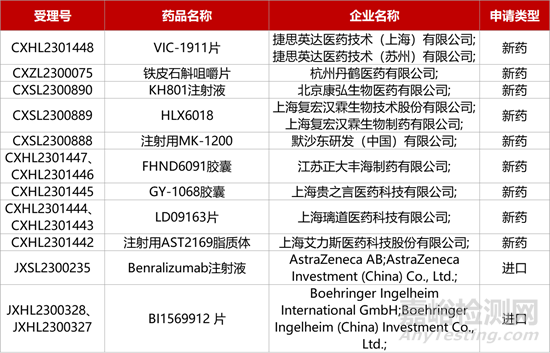
1. CDE新藥受理情況(12月26日)
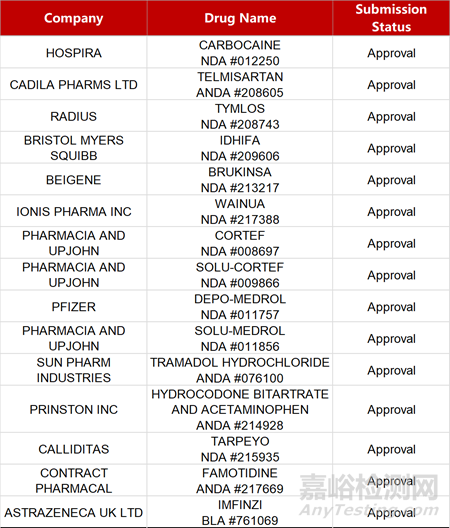
2. FDA新藥獲批情況(北美12月21日)