近日����,眼科醫(yī)療技術(shù)兼制藥公司Glaukos(紐約證券交易所代碼:GKOS)宣布FDA已批準(zhǔn)新藥申請(qǐng)(NDA),該公司裝載75微克曲伏前列素前房的iDose ® TR植入物可用于治療青光眼��。
Glaukos計(jì)劃在2024年第一季度下半年開始商業(yè)化iDose® TR植入物����,目前已經(jīng)確定該植入物的批發(fā)購(gòu)置成本為每枚/劑13,950美元。同時(shí)該公司還推出了“iDose Your Dose計(jì)劃”�����,表示每銷售一枚iDose® TR植入物�����,就會(huì)捐贈(zèng)同等數(shù)量的產(chǎn)品用于符合資格的慈善捐贈(zèng)請(qǐng)求�����,支持有需要的人群����。
關(guān)于iDose® TR曲伏前列素前房植入物
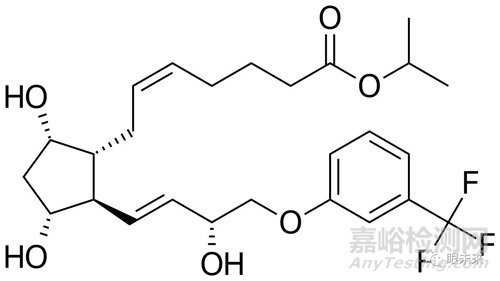
曲伏前列素是一種人工合成的前列腺素類似物�����,適應(yīng)癥為降低開角型青光眼或高眼壓癥患者升高的眼壓��,一般是做成滴眼液讓患者手動(dòng)施用。
Travoprost (曲伏前列素)
而Glaukos公司另辟蹊徑��,首次做出了這種藥物遞送植入物����,可以長(zhǎng)時(shí)間在眼內(nèi)全天候提供治療水平的曲伏前列素專有制劑。這樣做既能解決患者施藥不及時(shí)的普遍問題��,又能減少局部青光眼藥物相關(guān)的慢性副作用����,有望成為一種新的護(hù)理標(biāo)準(zhǔn)。
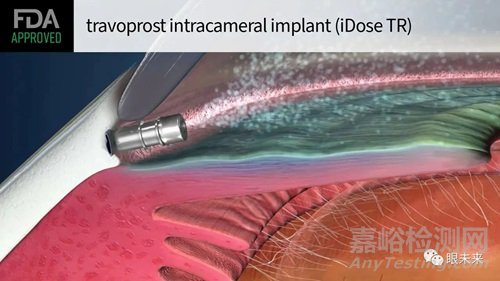
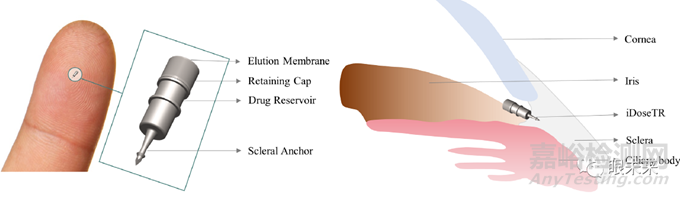
iDose® TR植入物由醫(yī)用級(jí)鈦制成����,尺寸為1.8毫米×0.5毫米,是通過(guò)一個(gè)小角膜切口放置在前房中��,并由鞏膜錨固定在那里����。植入物表面覆蓋含有78.0μm曲伏前列素的膜,這層膜長(zhǎng)時(shí)間在治療水平下連續(xù)洗脫��。藥物洗脫的速率有緩釋和快速釋放兩種方式,因此設(shè)備有兩種型號(hào)����。設(shè)備可以在4-5年后安全地更換為新設(shè)備。
手術(shù)時(shí)要?jiǎng)?chuàng)建一個(gè)2.2毫米的切口����,然后用凝聚性凝膠填充前房。而后使用房角鏡觀察鼻角�����,其方式與其他微創(chuàng)青光眼手術(shù)(MIGS)手術(shù)相同�����。接著iDose® TR裝載器瞄準(zhǔn)小梁網(wǎng)��,施加直接垂直壓力將iDose® TR植入物固定在鞏膜壁上��,然后松開插腳��。該裝載器用于輕推器件�����,以確保器件遠(yuǎn)離虹膜��。隨后進(jìn)行沖洗和抽吸以去除凝膠����,并用平衡鹽溶液水合端口。
不過(guò)iDose® TR曲伏前列素前房植入物不適用于以下患者:患有活動(dòng)性或疑似的眼部或眼周感染的患者��;患有角膜內(nèi)皮細(xì)胞營(yíng)養(yǎng)不良的患者�����;曾進(jìn)行過(guò)角膜移植手術(shù)或內(nèi)皮細(xì)胞移植手術(shù)的患者����;對(duì)曲前列素或產(chǎn)品的任何其他成分過(guò)敏的患者。
實(shí)驗(yàn)基礎(chǔ)
FDA批準(zhǔn)的基礎(chǔ)是兩項(xiàng)前瞻性��、隨機(jī)����、多中心、雙盲�����、第3階段關(guān)鍵試驗(yàn)(GC-010和GC-012),旨在比較兩種iDose® TR型號(hào)(緩釋型和快速釋放型)的單次給藥與局部施用0.5%噻嗎洛爾滴眼液(每天兩次)在降低開角型青光眼或眼內(nèi)高壓患者眼內(nèi)壓(IOP)方面的安全性和有效性�����。
兩項(xiàng)3期試驗(yàn)均在3個(gè)月內(nèi)成功達(dá)到預(yù)先設(shè)定的主要療效終點(diǎn)��,并在12個(gè)月內(nèi)顯示出良好的耐受性和安全性��。因此FDA得出結(jié)論�����,iDose® TR植入物前3個(gè)月內(nèi)降低眼壓的效果不輸噻嗎洛爾滴眼液����,不過(guò)該植入物在后來(lái)的9個(gè)月里療效與滴眼液存在一些差異。
在12個(gè)月時(shí)����,81%的iDose® TR受試者在兩項(xiàng)試驗(yàn)中完全沒有使用降低眼壓的局部藥物�����。98%的iDose® TR受試者在12個(gè)月時(shí)選擇繼續(xù)參加試驗(yàn)��,而噻嗎洛爾滴眼液對(duì)照受試者的比例為95%。在對(duì)照研究中��,2%-6%的iDose® TR患者報(bào)告的最常見的眼部不良反應(yīng)是眼壓升高�����、虹膜炎����、干眼癥和視野缺損,其中大多數(shù)是輕度和短暫的����。
Glaukos的董事長(zhǎng)兼首席執(zhí)行官Thomas Burns表示:“我們的這個(gè)治療概念已經(jīng)有15年了,F(xiàn)DA的批準(zhǔn)對(duì)我們來(lái)說(shuō)是一次里程碑事件?���,F(xiàn)在iDose ® TR植入物有望在美國(guó)成為治療開角型青光眼和高眼壓癥的新護(hù)理標(biāo)準(zhǔn)。”
關(guān)于Glaukos
Glaukos成立于1998年��,是一家眼科醫(yī)療技術(shù)和制藥公司����,專注于開發(fā)和商業(yè)化治療青光眼、角膜疾病和視網(wǎng)膜疾病的新療法��。公司于2015年6月完成了首次公開募股,在紐約證券交易所交易上市����。公司2023財(cái)年第三季度凈銷售額為7800萬(wàn)美元,同比增長(zhǎng)10%�����。青光眼業(yè)務(wù)第三季度凈銷售額為5830萬(wàn)美元����,同比增長(zhǎng)9%。
Glaukos開創(chuàng)了微創(chuàng)青光眼手術(shù)(MIGS)以作為傳統(tǒng)青光眼治療模式的替代方案�����,Glaukos于2012年在美國(guó)推出了其首款MIGS設(shè)備iStent®����。iStent是一種微型旁路支架,可與白內(nèi)障手術(shù)配合插入��,以降低成年人輕度至中度開角型青光眼患者的眼內(nèi)壓��,現(xiàn)在的相關(guān)產(chǎn)品型號(hào)為iStent inject® W和iStent infinite®。
iStent inject® W