今日頭條
江蘇威凱爾P2Y12R拮抗劑美國報產(chǎn)�。江蘇威凱爾醫(yī)藥宣布已向FDA遞交其維卡格雷膠囊用于治療冠心病ACS���、缺血性腦卒中以及確診外周動脈性疾病等血栓性心腦血管疾病的新藥上市申請(NDA)。維卡格雷是新一代口服P2Y12R拮抗劑���,其在體內(nèi)代謝生成的活性代謝物可有效抑制血小板的活化聚集���,同時有望解決“氯吡格雷抵抗”問題。這也是江蘇威凱爾創(chuàng)新藥管線中的首個新藥上市申請�。
國內(nèi)藥訊
1.羅氏眼科雙抗中國獲批新適應(yīng)癥。羅氏眼科VEGF-A/ANG-2雙抗法瑞西單抗(羅視佳®���,Vabysmo®)獲國家藥監(jiān)局批準(zhǔn)新適應(yīng)癥�,用于治療新生血管性年齡相關(guān)性黃斑變性�。Ⅲ期臨床(TENAYA和LUCERNE)兩年治療數(shù)據(jù)顯示,在達(dá)到與以每2個月接受活性對照治療患者相似視力改善的前提下���,有超過60%的Vabysmo組患者可以每隔4個月的間隔接受治療����。此前����,該新藥已在中國獲批用于治療糖尿病黃斑水腫����。
2.珠海貝海改良型多西他賽美國報產(chǎn)����。貝海生物多西他賽改良型抗腫瘤新藥BH009的上市申請獲得FDA受理。BH009不含吐溫80���,可消除與吐溫80相關(guān)的嚴(yán)重毒副作用如超敏反應(yīng)���、體液潴留����、腎毒性和神經(jīng)毒性等,臨床給藥時不需要給予預(yù)防性使用糖皮質(zhì)激素地塞米松�,臨床安全性及用藥依從性更優(yōu)。BH009已在治療晚期三陰性乳腺癌的Ⅱ期臨床達(dá)到主要終點�,患者接受BH009治療后,過敏反應(yīng)發(fā)生率為0%����。
3.AZ/第一三共HER2-ADC擬納入突破性品種。阿斯利康與第一三共開發(fā)的HER2靶向ADC德曲妥珠單抗(DS-8201a����,Enhertu)獲CDE擬納入突破性治療品種����,擬定適應(yīng)癥為:存在激活HER2(ERBB2)突變且既往接受過至少一種系統(tǒng)治療的不可切除或轉(zhuǎn)移性非小細(xì)胞肺癌成人患者�。在DESTINY-Lung02研究中,Enhertu達(dá)到58%的確認(rèn)客觀緩解率���,中位緩解持續(xù)時間為8.7個月����。
4.本導(dǎo)基因創(chuàng)新地貧療法獲批臨床���。本導(dǎo)基因1類生物制品“BD211自體CD34+造血干細(xì)胞注射液”獲國家藥監(jiān)局臨床許可���,擬開發(fā)用于治療輸血依賴型β-地中海貧血。BD211通過一系列優(yōu)化技術(shù)�,高效表達(dá)β珠蛋白,對β0/β0����、β0/β+等多種基因型地貧有效。研究者發(fā)起的臨床研究(IIT)顯示�,兩例β0/β0地貧患者均擺脫了輸血依賴����,隨訪時間超過兩年����,初步驗證了BD211的有效性和安全性。
5.普利抗腫瘤納米新藥美國獲批臨床���。普利制藥納米創(chuàng)新藥注射用PLAT001獲FDA臨床許可����,擬開發(fā)用于治療胰腺癌等晚期或轉(zhuǎn)移性實體瘤患者�。這是一款聚合物偶聯(lián)小分子藥物,已在臨床前藥效試驗中的胰腺癌����、肝癌等動物模型上顯示出顯著的腫瘤抑制作用����,有望為晚期或轉(zhuǎn)移性實體瘤患者的治療提供新的選擇。目前����,我國尚無本土原創(chuàng)納米藥物獲批上市���。
6.BI與瑞博合作開發(fā)治療NASH的RNAi療法。蘇州瑞博生物及瑞博國際研發(fā)中心與勃林格殷格翰達(dá)成研發(fā)合作���,將利用瑞博的RIBO-GalSTAR技術(shù)平臺合作開發(fā)治療非酒精性脂肪性肝炎(NASH)或代謝功能障礙相關(guān)脂肪性肝炎(MASH)的RNAi療法�。根據(jù)協(xié)議����,瑞博將獲得預(yù)付款,臨床研究���、藥物注冊和商業(yè)化里程碑后期付款���,以及產(chǎn)品的銷售分成,總金額超過20億美元����。
國際藥訊
1.FIC丙酮酸激酶激活劑地貧Ⅲ期臨床成功。Agios公司“first-in-class”口服丙酮酸激酶激活劑mitapivat治療成年非輸血依賴性(NTD)α或β地中海貧血患者的Ⅲ期臨床ENERGIZE達(dá)到主要終點和關(guān)鍵性次要終點���。與安慰劑相比����,Mitapivat治療第24周與基線相比平均血紅蛋白水平增加≥1g/dL的患者比例顯著更高(42.3%vs1.6%,雙側(cè)p<0.0001)�;兩組不良事件發(fā)生率相當(dāng)。預(yù)計2024年底遞交其用于治療地中海貧血的監(jiān)管申請�。
2.靶向藥物遞送器械A(chǔ)D臨床見刊NEJM。Insightec公司開發(fā)的能夠安全����、暫時地打開血腦屏障的聚焦超聲系統(tǒng),聯(lián)合抗β淀粉樣蛋白抗體治療阿爾茨海默病(AD)的首次人體研究成果發(fā)表于《新英格蘭醫(yī)學(xué)雜志》上����。帶有1,000多個超聲換能器的FUS MRI引導(dǎo)治療頭盔被引導(dǎo)到具有高淀粉樣蛋白-β斑塊的特定大腦區(qū)域,并經(jīng)過六個月的抗體治療�。結(jié)果顯示,與沒有血腦屏障開放的區(qū)域相比�,血腦屏障開放的大腦區(qū)域的淀粉樣蛋白-β斑塊平均減少32%。
3.羅氏超10億美元開發(fā)RNA靶向小分子藥物����。羅氏與Remix公司將利用后者專有REMaster藥物發(fā)現(xiàn)平臺���,聯(lián)合開發(fā)調(diào)節(jié)RNA序列以控制基因表達(dá)的小分子候選療法����。根據(jù)協(xié)議,Remix將獲得3000萬美元的預(yù)付款和1200萬美元的近期里程碑付款����,以及臨床前、臨床�、商業(yè)和銷售里程碑后期款項,總交易金額可能超過10億美元�。Remix將與羅氏一起進(jìn)行發(fā)現(xiàn)和臨床前活動,羅氏將負(fù)責(zé)產(chǎn)品的開發(fā)和商業(yè)化���。
4.Galapagos公司超7億美元開發(fā)小分子藥物���。Galapagos公司與BridGene公司將利用后者專有化學(xué)蛋白質(zhì)組學(xué)平臺IMTAC™,針對Galapagos指定的腫瘤靶點���,合作開發(fā)新型小分子候選藥物�。根據(jù)協(xié)議����,BridGene將獲得2700萬美元的預(yù)付款和臨床前研究里程碑付款,超過7億美元的臨床和商業(yè)里程碑潛在付款�,以及產(chǎn)品凈銷售額的分層版稅。Galapagos將擁有小分子候選藥物的開發(fā)和商業(yè)化的獨家權(quán)利。
5.基因編輯公司Tome擬1.85億美元收購Replace公司�。Tome Biosciences公司宣布收購Replace公司,并獲得該公司新型程序化基因組整合(PGI)技術(shù)平臺����。Replace的技術(shù)將CRISPR/Cas9的位點特異性與DNA連接酶相結(jié)合,從而能夠精確地編輯小DNA序列���。Replace的這種小DNA編輯技術(shù)將補(bǔ)充Tome公司的大DNA整合技術(shù)�。根據(jù)協(xié)議�,Tome公司將支付6500萬美元的預(yù)付款和近期里程碑付款,以及高達(dá)1.85億美元的股票和現(xiàn)金���。
6.CG Oncology公司申請納斯達(dá)克IPO����。CG Oncology公司宣布遞交了納斯達(dá)克IPO申請并獲得受理�。CG Oncology的核心管線CG0070是一款臨床后期的溶瘤病毒療法,已在去年12月獲得FDA同時授予突破性療法認(rèn)證和快速通道資格����,用于治療高危、卡介苗治療不響應(yīng)非肌肉侵襲性膀胱癌(NMIBC)���。在Ⅲ期試驗中����,CG0070單藥治療的完全緩解率為75.7%����。樂普生物擁有CG0070的大中華區(qū)權(quán)益。
醫(yī)藥熱點
1.新版醫(yī)保目錄1月1日起執(zhí)行���。2024年1月1日�,新版醫(yī)保目錄正式落地實施���。新版醫(yī)保目錄新增126種���,調(diào)出一種,目錄內(nèi)藥品總數(shù)增至3088種���,其中西藥1698種���、中成藥1390種;中藥飲片仍為892種���。本次調(diào)整���,慢性病����、罕見病�、兒童用藥等領(lǐng)域的保障水平得到進(jìn)一步提升。疊加談判降價和醫(yī)保報銷因素����,預(yù)計未來兩年將為患者減負(fù)超400億元。
2.張金保任首都兒科研究所黨委書記���。2023年12月29日�,首都兒科研究所召開中層干部大會����。會上,市委組織部行政干部處處長代金鵬同志宣布了市委任命決定�,張金保同志任中共首都兒科研究所委員會委員、黨委書記(副局長級)�,免去劉中勛同志中共首都兒科研究所委員會書記、委員職務(wù)���,調(diào)首都醫(yī)科大學(xué)附屬北京中醫(yī)醫(yī)院工作�。張金保同志表示,將盡快進(jìn)入角色���,依靠班子,帶領(lǐng)全所干部職工謀事���、創(chuàng)業(yè)�,攻堅克難�,推進(jìn)首兒所高質(zhì)量發(fā)展。
3.GSK前高管入職Biotech����。騰盛博藥宣布,Brian Alvin Johns自2024年1月3日起擔(dān)任首席科學(xué)官����,他將全面負(fù)責(zé)新藥開發(fā)項目,并制定公司的未來管線策略和優(yōu)先事項�。Brian Alvin Johns擁有化學(xué)博士學(xué)位,在創(chuàng)新藥物的發(fā)現(xiàn)和早期開發(fā)項目方面擁有豐富的經(jīng)驗�。此前,Brian Alvin Johns曾在HemoShear Therapeutics擔(dān)任首席科學(xué)官�,以及曾在ViiV Healthcare和葛蘭素史克擔(dān)任新藥開發(fā)副總裁�。
評審動態(tài)
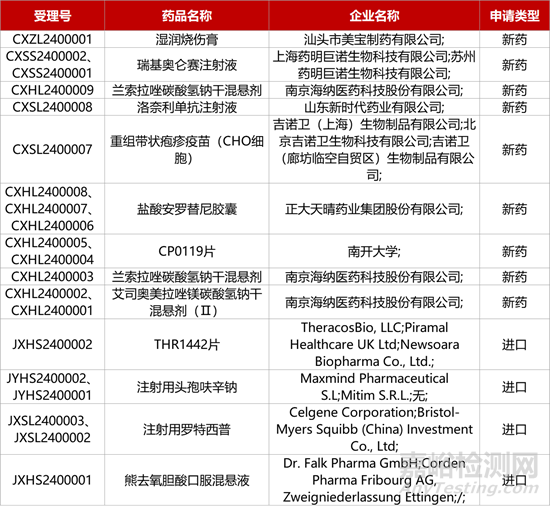
1. CDE新藥受理情況(01月04日)
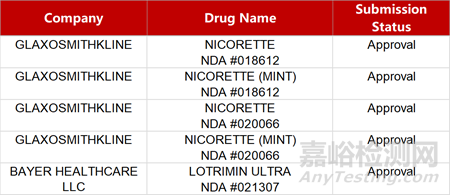
2. FDA新藥獲批情況(北美01月03日)