【問】單抗產(chǎn)品上游共線生產(chǎn)的污染控制關(guān)注點(diǎn)是什么����?
【答】上游共線生產(chǎn)的基本原則及流程: 《藥品共線生產(chǎn)質(zhì)量管理指南》已對藥品研發(fā)�、技術(shù)轉(zhuǎn)移及生產(chǎn)階段中生物制品的共線生產(chǎn)要求進(jìn)行了詳細(xì)的闡述,對于單抗上游的生產(chǎn)�,企業(yè)在考慮共線生產(chǎn)時(shí)還應(yīng)特別關(guān)注以下風(fēng)險(xiǎn)點(diǎn):
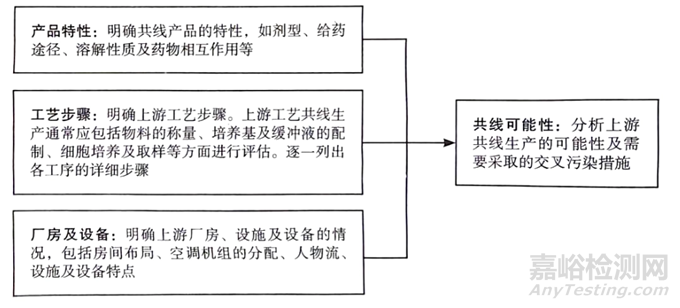
原則上,單克隆抗體不應(yīng)與激素類生物制品�、細(xì)胞毒類及高活性的藥品共線生產(chǎn)。對于其他考慮共線生產(chǎn)的產(chǎn)品����,需要經(jīng)過充分的共線生產(chǎn)風(fēng)險(xiǎn)評估判斷是否可以共線生產(chǎn)。典型的共線評估流程見下圖�。
上游共線評估流程圖
上游共線生產(chǎn)的污染控制要求: 在單抗的共線生產(chǎn)過程中����,相對于傳統(tǒng)的不銹鋼系統(tǒng)��,一次性使用技術(shù)能更好地防止交叉污染��,在充分確認(rèn)系統(tǒng)密閉性的條件下���,單抗多產(chǎn)品的共線應(yīng)首先考慮使用一次性系統(tǒng): 不銹鋼系統(tǒng)用于單抗多產(chǎn)品共線生產(chǎn)時(shí)���,需要更詳細(xì)的風(fēng)險(xiǎn)評估和系統(tǒng)性的清潔驗(yàn)證來避免產(chǎn)品的交叉污染。
另外�,GMP 中明確規(guī)定企業(yè)不得在同一生產(chǎn)操作間同時(shí)進(jìn)行不同品種和規(guī)格藥品的生產(chǎn)操作,除非沒有發(fā)生混淆或交叉污染的可能���。因此����,單抗上游的共線生產(chǎn)中應(yīng)考慮采用時(shí)間隔離 (錯時(shí)生產(chǎn)) 的形式����,或采取可靠的措施來支持同時(shí)生產(chǎn) (如同一區(qū)域的獨(dú)立密閉系統(tǒng))。
·對于在生產(chǎn)過程中可能出現(xiàn)活性物質(zhì)暴露的工藝步驟��,在共線生產(chǎn)中考慮采用時(shí)間隔離 (錯時(shí)生產(chǎn)) 的形式����,如培養(yǎng)基配制、細(xì)胞接種等�����。錯時(shí)生產(chǎn)的形式應(yīng)建立生產(chǎn)線換產(chǎn)品管理的流程��,確保在下一產(chǎn)品入場前完成清場及清潔����,其操作應(yīng)符合 GMP 的相關(guān)要求。作為密閉發(fā)酵階段�,可以同時(shí)進(jìn)行產(chǎn)品的共線生產(chǎn),但是仍然應(yīng)該制定明確的管理流程來明確異常事件 (如泄漏) 的處理要求����。
來源: 2023年藥品GMP指南-無菌制劑下冊P857-858