一、 概述
物料從供應(yīng)商處到企業(yè)端接收直至放行�����,主要的大致流程包括接收-入庫(kù)-存放-檢驗(yàn)-放行等過(guò)程�,在整個(gè)過(guò)程中需要建立合理合規(guī)的SMP/SOP有序地管理和運(yùn)行,才能確保物料的質(zhì)量和可追溯性�,從而保證最終產(chǎn)品的質(zhì)量。
二�、 GMP條件下對(duì)物料從接收到放行的管理要求
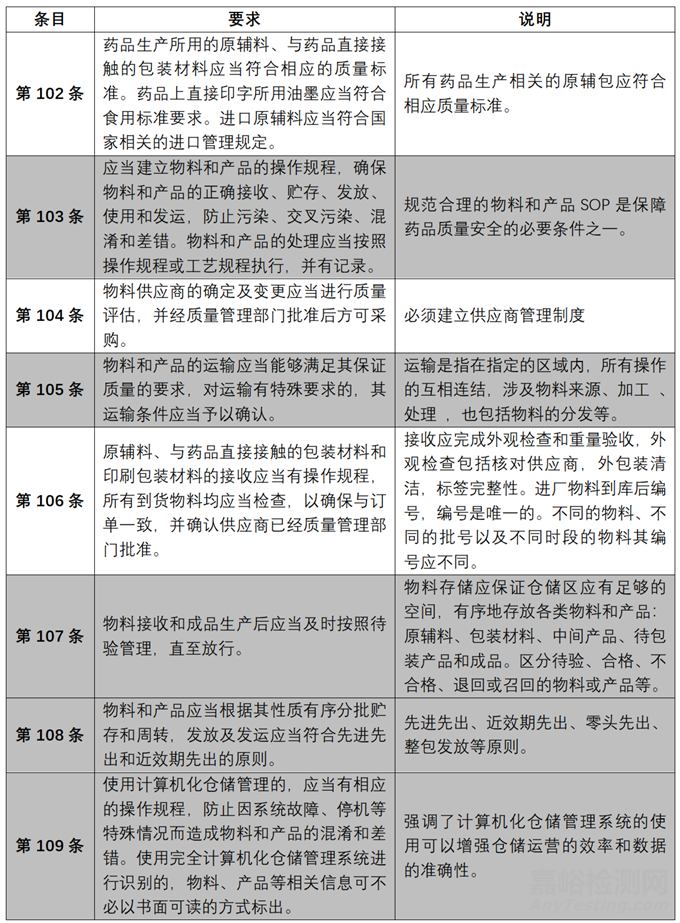
在我國(guó)2011年版藥品生產(chǎn)質(zhì)量管理規(guī)范中,第六章 物料與產(chǎn)品�����,第一節(jié) 原則:第102條到109條相關(guān)描述中���,明確指出了對(duì)于物料管理的基本原則�。明確指出了對(duì)于物料管理的基本要求和原則���,涉及從接收到放行過(guò)程的內(nèi)容主要是第103條�����、105條�����、107-109條(見表1:灰色區(qū)域)�����。第103條:從合規(guī)實(shí)施的角度�,要求企業(yè)應(yīng)當(dāng)建立物料和產(chǎn)品的操作規(guī)程�,確保物料和產(chǎn)品的正確接收、貯存�、發(fā)放、使用和發(fā)運(yùn)�����,防止污染�、交叉污染、混淆和差錯(cuò)�����;第105條:關(guān)于物料的正確運(yùn)輸要求,側(cè)重于從物料運(yùn)輸屬性(廠區(qū)內(nèi)/外�、潔凈/非潔凈區(qū)、特殊/非特殊物料等)角度���,防止和減小風(fēng)險(xiǎn)���,并制定控制策略;第107條至第109條:分別關(guān)于物料接收�����、待驗(yàn)和倉(cāng)儲(chǔ)管理等要求�����。
▲表1-藥品生產(chǎn)質(zhì)量管理規(guī)范(2011)中物料管理基本原則
三�����、 物料從接收到放行的管理流程和要點(diǎn)
藥企的物料管理是GMP體系下的重要環(huán)節(jié)���,通過(guò)規(guī)范合理的流程化管理�����,包括供應(yīng)商管理�、采購(gòu)、驗(yàn)收���、入庫(kù)�����、檢測(cè)和放行等環(huán)節(jié)���,可以確保物料的穩(wěn)定供應(yīng)和質(zhì)量�,進(jìn)而保障產(chǎn)品的質(zhì)量和安全。
3.1 物料從接收到放行的管理流程
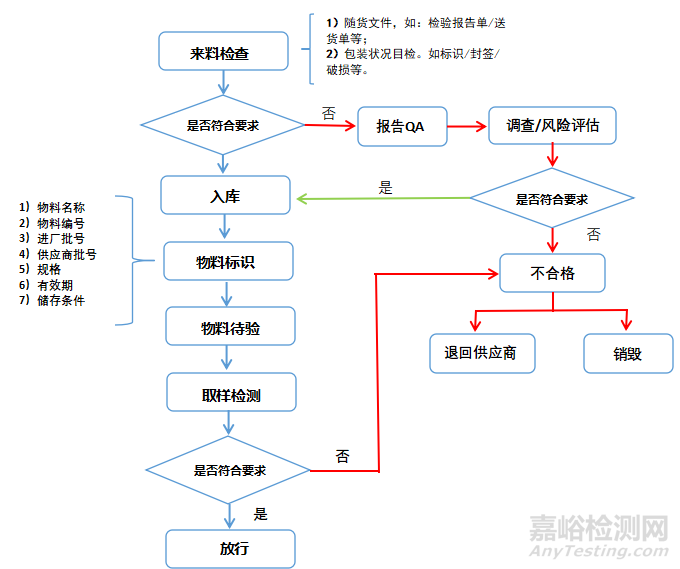
物料從接收到放行是物料供應(yīng)鏈管理過(guò)程中的重要環(huán)節(jié)���,一般的流程步驟�����,見下圖1:
▲圖1-物料從接收到放行一般流程
來(lái)料檢查:倉(cāng)庫(kù)人員和采購(gòu)部門配合對(duì)物料進(jìn)行外觀(包裝/標(biāo)簽/標(biāo)識(shí)等)和文件資料(檢驗(yàn)報(bào)告單���、送貨單�����、發(fā)票等)核驗(yàn)���,以確保其符合要求和規(guī)范。符合規(guī)定的���,辦理入庫(kù)登記�。若不符合�����,需報(bào)告QA�����,經(jīng)QA調(diào)查/評(píng)估后�,根據(jù)結(jié)果入庫(kù)或退回/銷毀;
入庫(kù):倉(cāng)庫(kù)一般劃分三個(gè)區(qū)并以顏色區(qū)分�,分別是“合格區(qū)(綠色標(biāo)識(shí))”、“不合格區(qū)(紅色標(biāo)識(shí))”�、“待驗(yàn)區(qū)(黃色標(biāo)識(shí))”,倉(cāng)庫(kù)收到物料后,初驗(yàn)合格的物料及時(shí)放至待驗(yàn)區(qū)���;初驗(yàn)不合格的���,轉(zhuǎn)移至不合格區(qū),由倉(cāng)庫(kù)按照《不合格品管理規(guī)程》處理�,并登記《不合格品登記臺(tái)賬》。
物料標(biāo)識(shí):倉(cāng)管員在每件包裝醒目處張貼《物料進(jìn)廠標(biāo)簽》并填寫《貨位卡》���,包括但不限于名稱�����、代碼���、批號(hào)、生產(chǎn)廠家�、性狀/理化性質(zhì)�����、生產(chǎn)日期���、化學(xué)品安全標(biāo)志等���。
物料待驗(yàn):待驗(yàn)區(qū)物料掛待驗(yàn)標(biāo)識(shí)和黃色警戒線同時(shí)倉(cāng)管員填寫《物料入庫(kù)單》及《物料臺(tái)賬》�。倉(cāng)儲(chǔ)部責(zé)任人負(fù)責(zé)審核監(jiān)督倉(cāng)庫(kù)管理員對(duì)物料狀態(tài)的標(biāo)識(shí)�����。倉(cāng)庫(kù)管理員負(fù)責(zé)對(duì)物料的狀態(tài)進(jìn)行標(biāo)識(shí)�。
取樣檢測(cè):在 GMP體系下,物料取樣檢測(cè)是非常重要的一環(huán)���,需制定合理合規(guī)的SOP用于確保產(chǎn)品在制造過(guò)程中的質(zhì)量和安全性���,通常包括如下:1)取樣計(jì)劃;2)取樣操作���;3)樣品標(biāo)識(shí)和記錄�����;4)樣品檢測(cè)�;5)結(jié)果分析與評(píng)估�����;6)結(jié)果處理等程序。
放行:在 GMP體系下���,物料放行是指對(duì)經(jīng)過(guò)取樣檢測(cè)和質(zhì)量控制審核后符合規(guī)定標(biāo)準(zhǔn)的物料進(jìn)行批量放行���,以供后續(xù)生產(chǎn)和使用。物料放行一般包括:
● 質(zhì)量數(shù)據(jù)審核:質(zhì)量部門評(píng)估樣品是否符合規(guī)定的質(zhì)量標(biāo)準(zhǔn)���。同時(shí)會(huì)對(duì)該批物料的相關(guān)文件�、記錄和質(zhì)量控制程序進(jìn)行審核�;
● 放行決策:倉(cāng)儲(chǔ)部根據(jù)分析結(jié)果和質(zhì)量控制審核報(bào)告,評(píng)估物料的質(zhì)量狀況�����。如果物料符合規(guī)定要求�,對(duì)批次進(jìn)行放行決策;
● 放行記錄:倉(cāng)管員對(duì)放行決策進(jìn)行書面記錄�,包括批號(hào)、日期�����、放行人員等信息�����,以便追溯和審計(jì)�;
● 放行通知:倉(cāng)儲(chǔ)部通知相關(guān)部門該批物料已經(jīng)放行,可以用于后續(xù)生產(chǎn)或使用�。
以上是一個(gè)基本的物料從接收到放行的流程,在實(shí)際操作中�,不同企業(yè)需要根據(jù)自己的具體情況來(lái)進(jìn)行相應(yīng)的調(diào)整和優(yōu)化。
3.2 物料從接收到放行管理的要點(diǎn)和內(nèi)容
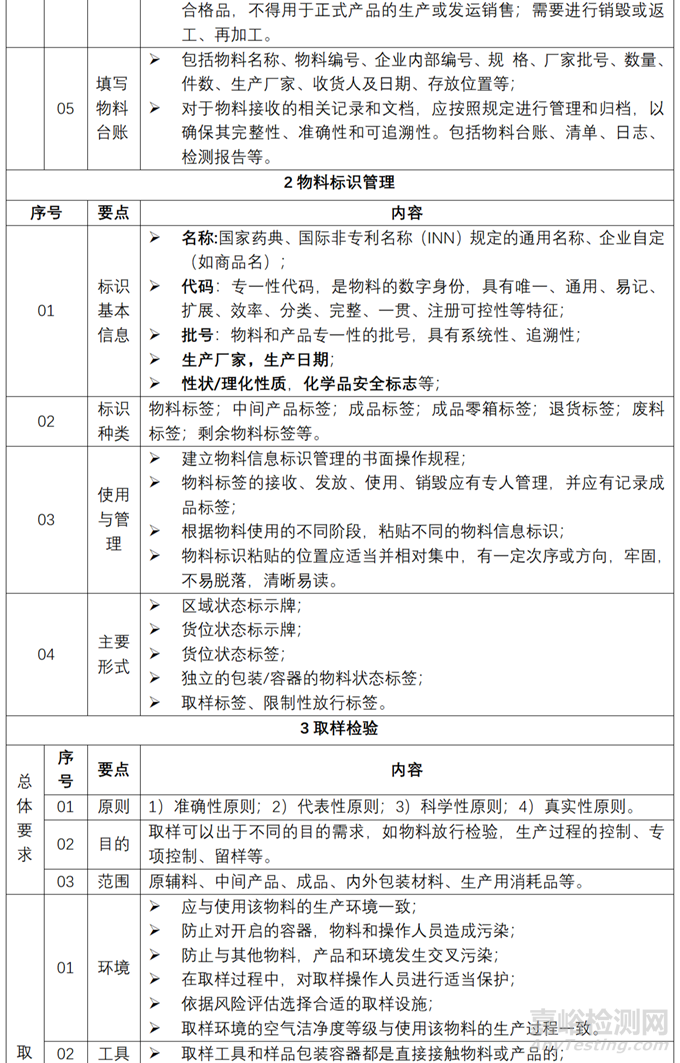
物料從接收到放行的管理要點(diǎn)和內(nèi)容�,在 GMP體系下,藥企通?��?梢砸罁?jù)相關(guān)規(guī)定和標(biāo)準(zhǔn)進(jìn)行處理�。以下是一些常見的要點(diǎn)和內(nèi)容�����,見表2���。
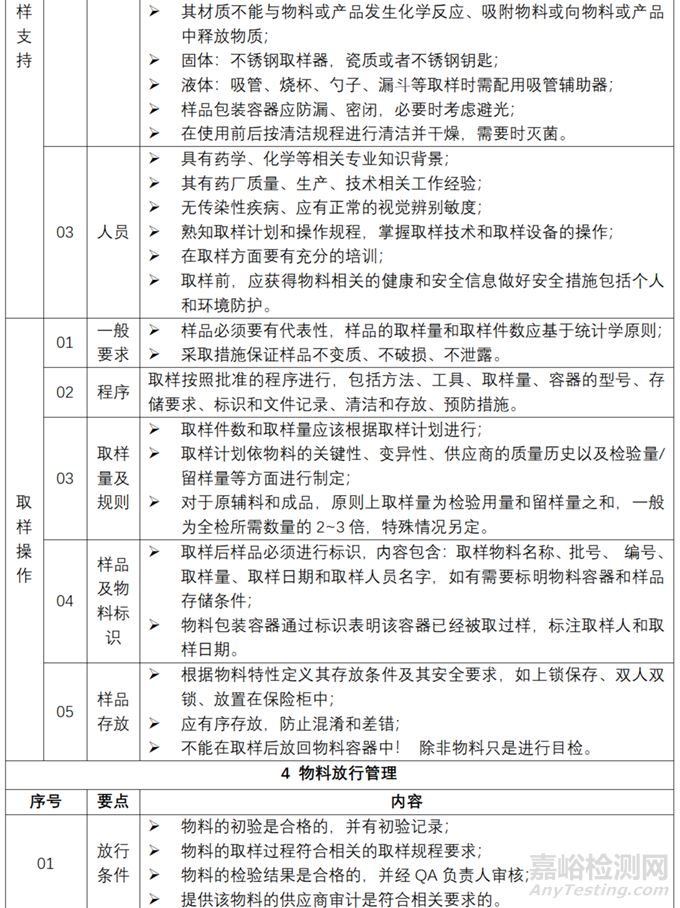
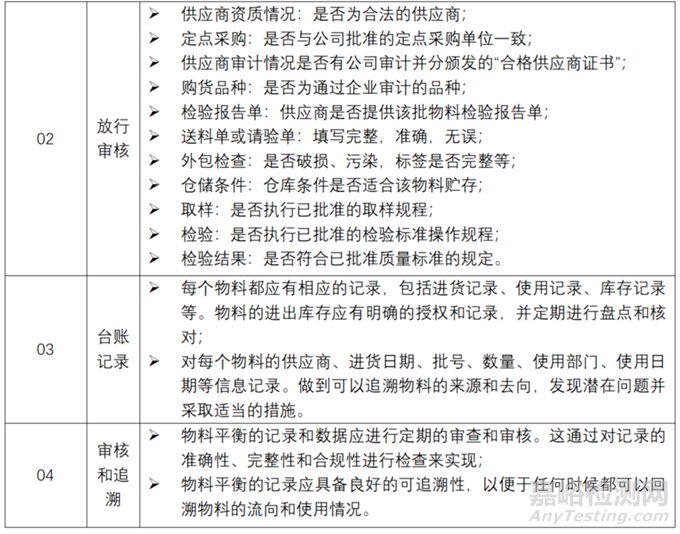
▲表2-物料從接收到放行管理的要點(diǎn)和內(nèi)容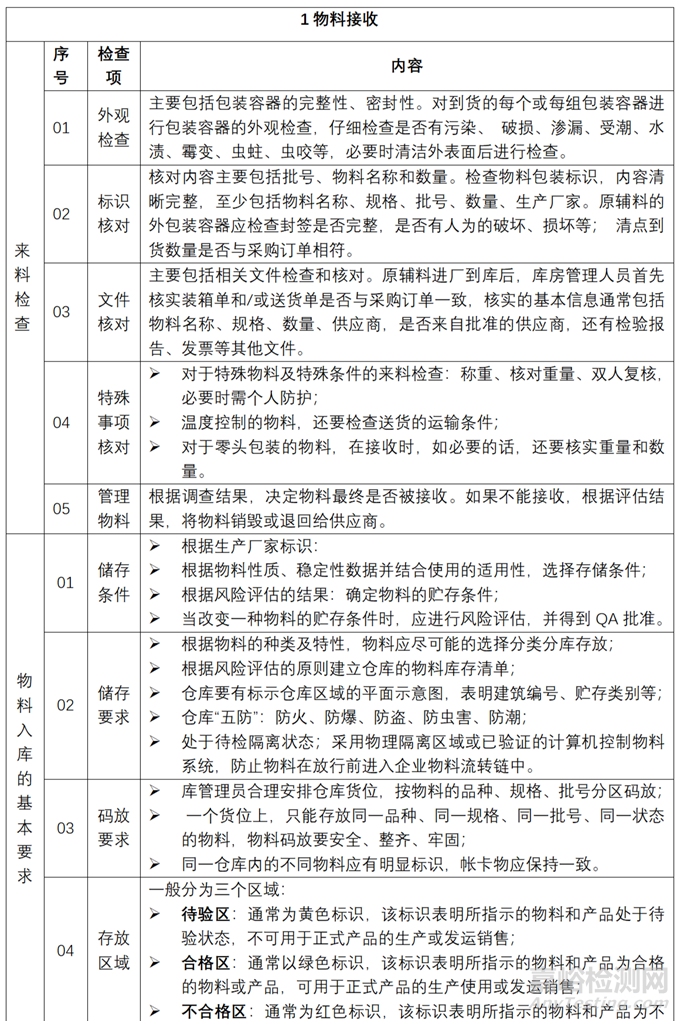
四�����、 結(jié)束語(yǔ)
物料管理是確保藥企產(chǎn)品質(zhì)量和合規(guī)性的基石���,藥企在GMP體系下物料從接收到放行的規(guī)范化流程管理�����,應(yīng)通過(guò)建立高效實(shí)用的SOP有序地執(zhí)行原材料采購(gòu)���、驗(yàn)收、存儲(chǔ)���、標(biāo)識(shí)�����、檢驗(yàn)���、放行、領(lǐng)用等程序���,并輔助施行風(fēng)險(xiǎn)評(píng)估���、糾正和預(yù)防措施體系(CAPA)���、變更�����、文件/臺(tái)賬記錄等SMP制度�。同時(shí),還應(yīng)定期進(jìn)行物料管理的內(nèi)部審核���,以確保物料管理過(guò)程的有效性和持續(xù)改進(jìn)���。
參考文獻(xiàn)
[1] 《藥品生產(chǎn)質(zhì)量管理規(guī)范》(2011版).
[2] 高潔,李海劍,宋麗麗.從我國(guó)藥品生產(chǎn)質(zhì)量管理規(guī)范的修訂看物料管理的動(dòng)向[J].中國(guó)藥業(yè), 2010, 19(012):4-5.
[3] 孔飛,徐世豪,田茂權(quán).制藥企業(yè)生產(chǎn)環(huán)節(jié)中的物料控制管理淺析[J].醫(yī)藥, 2022(11):4.
[4] 陶令峰.從藥品檢查角度探討原料藥生產(chǎn)現(xiàn)場(chǎng)檢查物料管理的常見問(wèn)題及對(duì)策[J].廣東化工, 2023, 50(16):77-79.