今日頭條
智翔金泰RSV預防藥物獲批臨床��。智翔金泰1類新藥GR2102注射液獲國家藥監(jiān)局臨床許可,擬開發(fā)用于預防呼吸道合胞病毒感染���。GR2102是一款重組全人源抗呼吸道合胞病毒(RSV)單抗�,可以特異性結合RSV表面的F蛋白�,阻斷RSV入侵宿主細胞,從而達到防止RSV感染的作用����。國內同類產品愛科百發(fā)的RSV融合蛋白小分子抑制劑齊瑞索韋(ziresovir,AK0529)已在中國申報上市���。
國內藥訊
1.強生GPRC5D/CD3雙抗擬納入優(yōu)先審評�。強生創(chuàng)新GPRC5D/CD3雙抗塔奎托單抗(Talquetamab)獲CDE擬納入優(yōu)先審評�,用于單藥治療既往接受過至少三種治療(包括一種蛋白酶體抑制劑、一種免疫調節(jié)劑和一種抗CD38抗體)的復發(fā)或難治性多發(fā)性骨髓瘤患者�。在Ⅰ/Ⅱ期MonumenTAL-1試驗中,talquetamab(405μg/kg���,800μg/kg)在至少4種前期治療的患者中達到73.0%和73.6%的總緩解率�。FDA已于去年8月加速批準Talquetamab上市���。
2.映恩Trop-2-ADC獲婦科腫瘤快速通道資格�。映恩生物自主研發(fā)新一代Trop2靶向ADC藥物DB-1305(BNT325)獲FDA授予快速通道資格,用于治療既往接受過1~3種全身治療方案的鉑類藥物耐藥上皮性卵巢癌����、輸卵管癌或原發(fā)性腹膜癌患者����。在I/IIa期臨床中,DB-1305治療晚期實體瘤的客觀反應率(ORR)達到30.4%�����,疾病控制率(DCR)為87.0%�。BioNTech公司擁有該新藥大中華區(qū)外的開發(fā)、生產和商業(yè)化權益����。
3.默沙東IL-2激動劑中國獲批SLE臨床。默沙東1類生物制品MK-6194注射液獲國家藥監(jiān)局臨床許可����,擬開發(fā)治療系統(tǒng)性紅斑狼瘡(SLE)。MK-6194是一款選擇性IL-2激動劑����,能夠選擇性與Tregs表面包含IL-2Ra亞基的IL-2受體三聚體結合���,從而特異性激活和擴增Tregs,對自身免疫性疾病有治療潛力��。目前���,該產品正在Ⅰ期臨床中用于治療中重度特應性皮炎患者�,以及在Ⅱ期臨床中評估治療非節(jié)段性白癜風��,和治療SLE的效果���。
4.恒瑞PARP1抑制劑獲批新臨床�。恒瑞自主研發(fā)的PARP1抑制劑HRS-1167的新適應癥臨床試驗申請獲國家藥監(jiān)局批準���,擬聯合ATR抑制劑HRS2398治療晚期實體瘤患者�����。目前���,該新藥正在國內開展兩項I期臨床,分別評估單藥以及與利福平聯用治療實體瘤患者的潛力��。值得一提的是,默克已與恒瑞達成合作許可協議�,獲得HRS-1167以及另一款Claudin-18.2 ADC產品SHR-A1904的中國大陸以外的全球權益。
5.安可康雙矛I型溶瘤病毒獲批臨床���。四川安可康生物開發(fā)的雙矛I型溶瘤病毒DS1-H2-1獲FDA批準開展I/II期臨床�����,擬評估用于治療神經母細胞瘤的安全性與有效性。DS1-H2-1由西尼羅河病毒(WNV)和人T細胞共刺激基因組成�。安可康計劃開發(fā)該產品用于治療復發(fā)和難治性神經母細胞瘤、膠質母細胞瘤和結腸癌�����。
6.智飛26價肺炎結合疫苗報IND����。智飛生物26價肺炎結合疫苗的臨床試驗申請獲NMPA受理。肺炎球菌有90多種血清型�,但造成侵襲性感染的血清型相對集中在部分型別。智飛綠竹自主研發(fā)的26價肺炎結合疫苗�����,擬開發(fā)用于2月齡以上人群,預防更廣泛肺炎球菌相關血清型引起的侵襲性疾病�。國內目前尚無同類產品進入臨床研究階段或獲批上市。
國際藥訊
1.強生FcRn抗體自免?、笃谂R床積極。強生靶向新生兒Fc受體(FcRn)抗體nipocalimab治療重癥肌無力(gMG)的Ⅲ期臨床VIVACITY達到主要終點��。與安慰劑比�����,nipocalimab治療患者的MG-ADL評分在22-24周時顯著降低����。詳細結果將公布于醫(yī)學大會上。此外����,nipocalimab在治療干燥綜合征(SjD)的Ⅱ期臨床DAHLIAS也達到主要終點,nipocalimab治療患者第24周時clinESSDAI評分較安慰劑顯著降低����。在兩項研究中,nipocalimab耐受性良好����。
2.葛蘭素史克BCMA ADC骨髓瘤頭對頭III期結果積極����。葛蘭素史克靶向BCMA的ADC藥物Blenrep(belantamab mafodotin)聯合硼替佐米加地塞米松(BorDex)治療復發(fā)或難治性多發(fā)性骨髓瘤的Ⅲ期臨床DREAMM-7達到主要終點和所有次要療效終點����。與daratumumab聯合BorDex相比,Blenrep聯合用藥顯著提高患者無進展生存期(中位PFS:36.6個月vs13.4個月)��,疾病進展或死亡風險降低59%(p<0.00001)���。目前,總生存期(OS)仍在繼續(xù)評估�����。
3.視網膜基因療法Ⅱ期臨床積極�。4D Molecular公司基因療法4D-150治療濕性年齡相關性黃斑變性(AMD)的Ⅱ期臨床PRISM結果積極。4D-150由表達阿柏西普和抗VEGF-C的RNAi有效載荷以及能夠在玻璃體內進行遞送的專有載體R100組成����,能夠抑制4種(VEGFA、B�����、C和PlGF)血管生成因子。48周隨訪結果顯示����,高劑量4D-150可將抗VEGF注射治療的年化注射率降低89%,63%的患者在接受治療后的24周內無需補充注射阿柏西普;4D-150耐受性良好���。
4.安進長效減重PDC早期臨床見刊���。安進GIPR/GLP-1R雙抗多肽偶聯(PDC)藥物AMG 133在《自然》子刊Nature Metabolism上發(fā)表用于減肥的臨床前研究和Ⅰ期臨床結果。數據顯示�,AMG 133(420mg,每月一針)治療患者在85天時體重較基線平均降低14.5%(約26斤)����;停藥150天后,仍可維持體重減輕超過10%���。最常見的不良事件為胃腸道相關不良事件��,包括惡心和嘔吐����,大多數為輕度。
5.諾華29億美元收購德國MorphoSys AG��。諾華擬以每股68歐元收購德國MorphoSys AG(總計27億歐元)��,并獲得該公司臨床后期擬開發(fā)用于治療骨髓纖維化的BET抑制劑pelabresib (CPI-0610)和用于實體瘤和淋巴瘤治療的EZH1/2蛋白雙重抑制劑tulmimetostat(CPI-0209)資產���。同日,Incyte也宣布與MorphoSys簽署一項資產購買協議����,獲得一款CD19靶向免疫療法tafasitamab的全球獨家開發(fā)和商業(yè)化權利。
6.諾和控股165億美元收購Catalent���。諾和諾德宣布�,公司大股東諾和控股(Novo Holdings)將以165億美元合并收購Catalent(康泰倫特)公司����。Catalent是一家總部位于美國新澤西州薩默塞特的全球合同開發(fā)和生產組織���,在全球五大洲擁有超過40家工廠設施�。作為交易的一部分�,諾和諾德將以110億美元的預付款從諾和控股手中收購屬于Catalent的三個灌裝工廠��,預計這將從2026年起逐步提高諾和諾德的灌裝能力�。
醫(yī)藥熱點
1.“四川省互聯網總醫(yī)院”正式上線����。近日,四川省互聯網總醫(yī)院正式上線���。這是原“天府醫(yī)健通”平臺改版升級的衛(wèi)生健康公益服務平臺�����,由省衛(wèi)生健康委監(jiān)管���、省衛(wèi)生健康信息中心主導建設,接入了四川大學華西醫(yī)院���、四川大學華西第二醫(yī)院�、四川省人民醫(yī)院���、四川省腫瘤醫(yī)院���、四川省婦幼保健院��、川北醫(yī)學院附屬醫(yī)院��、西南醫(yī)科大學附屬醫(yī)院等7家互聯網診療服務資源�,4000余名醫(yī)生在線接診����。
2.皖南醫(yī)學院二附院宮頸宮腔疾病診療中心揭牌。1月21日上午����,上海紅房子婦產科醫(yī)院與皖南醫(yī)學院第二附屬醫(yī)院合作共建宮頸宮腔疾病診療中心暨隋龍教授專家團隊工作室啟動儀式在安徽蕪湖隆重舉行。此次合作將促進雙方在醫(yī)療技術����、人才培養(yǎng)、科研創(chuàng)新等方面開展全方位的合作與交流�,共同推動宮頸宮腔疾病診療水平的提升和區(qū)域醫(yī)療健康事業(yè)的發(fā)展。
3.北京將開展慢病門診按人頭付費試點�。2月2日�,在2024年北京市“三醫(yī)聯動”工作會議上����,北京市醫(yī)保局黨組書記���、局長馬繼業(yè)介紹,今年����,北京市將開展糖尿病、高血壓等慢性病門診按人頭付費試點����。按人頭付費��,是指醫(yī)療保險機構根據醫(yī)院所服務的參保人數���,向醫(yī)院支付一筆固定費用。按人頭付費試點旨在激發(fā)醫(yī)院對患者進行長期健康管理��,使醫(yī)院整體把控醫(yī)?����;ㄙM���,有助于醫(yī)?��;鹂傮w控制。
評審動態(tài)
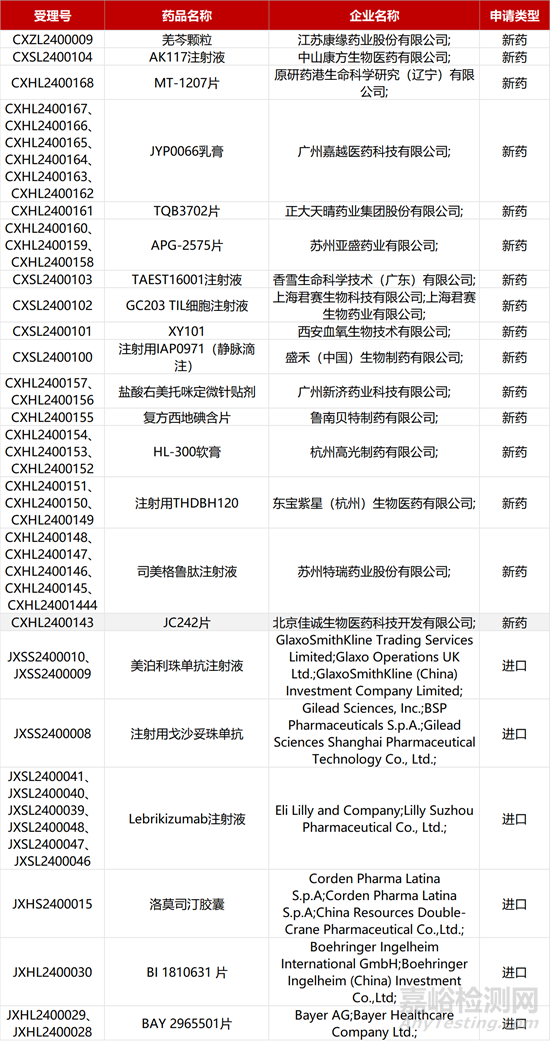
1. CDE新藥受理情況(02月06日)
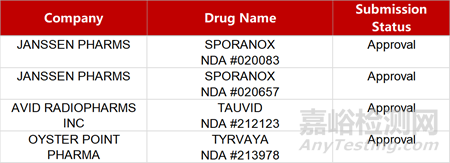
2. FDA新藥獲批情況(北美02月05日)