siRNA藥物通過調(diào)控mRNA增加或減少疾病相關(guān)蛋白的產(chǎn)生而發(fā)揮藥理學(xué)活性�。評價mRNA 和蛋白水平的變化�,需建立合適的體外和體內(nèi)模型?除了已被業(yè)界所熟知的基于LNP遞送系統(tǒng)和GalNac偶聯(lián)技術(shù)以外���,對于肝外靶向遞送����、新型作用機制的siRNA藥物,藥效學(xué)研究或藥代動力學(xué)/藥效學(xué)(PK/PD)具有更為重要的意義�����。
與小分子藥物和蛋白類藥物不同�����, siRNA藥物 PK/PD 關(guān)系獨特:
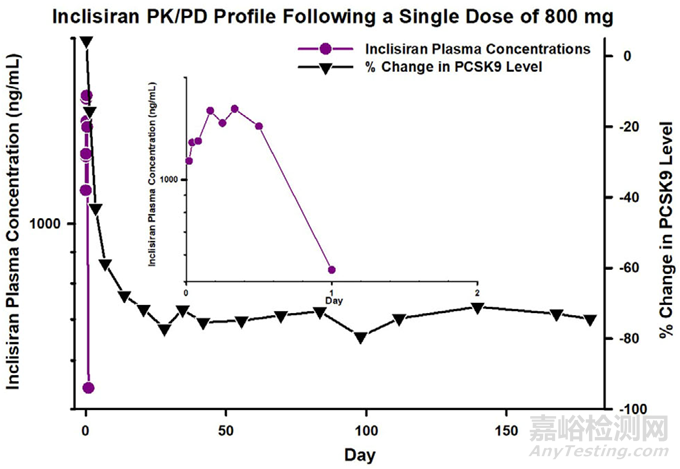
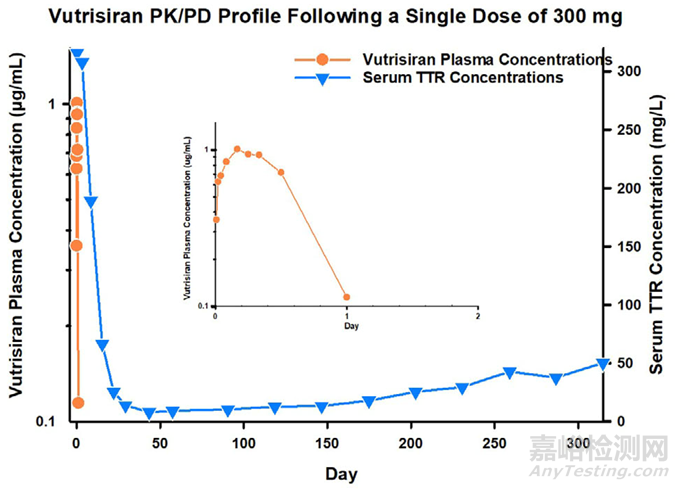
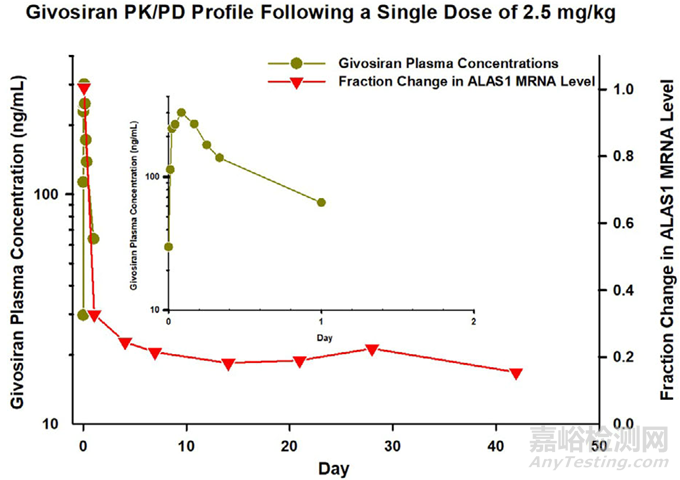
血漿中暴露時間短��、靶器官(如肝臟)中暴露時間長且藥效作用持久
圖1. Givosiran�����、Inclisiran 和 Vutrisiran:血漿中siRNA濃度和血清中PD標志物變化關(guān)系[1]
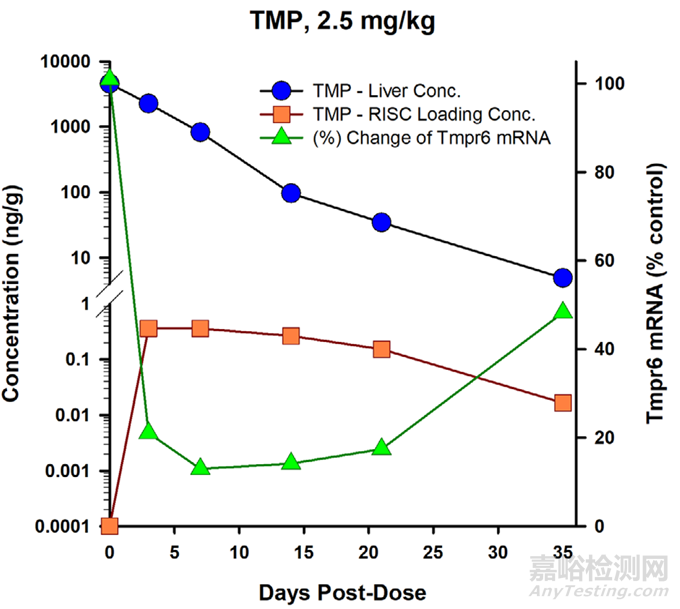
關(guān)鍵的藥效學(xué)物質(zhì)基礎(chǔ)是胞漿中siRNA和RISC復(fù)合物��,而非血漿或靶器官中總的siRNA濃度
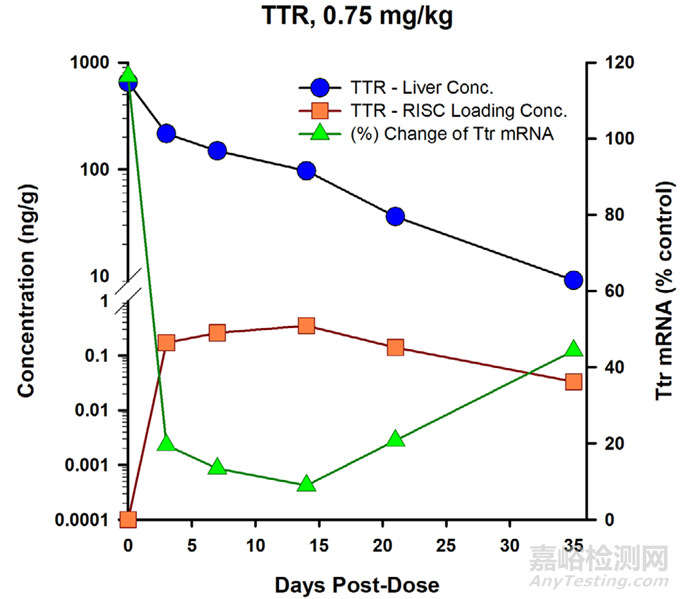
圖2. 肝臟中siRNA總濃度�、siRNA-RISC濃度和PD標志物變化關(guān)系[1]
siRNA的內(nèi)體逃逸效率����、siRNA與RISC的結(jié)合動力學(xué)也可能因平臺或遞送系統(tǒng)而異
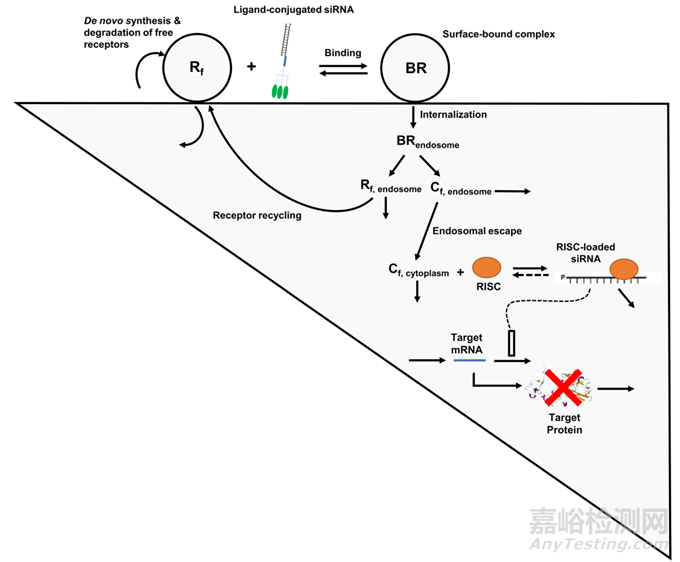
圖3. GalNac siRNA進入細胞��、細胞內(nèi)分布和發(fā)揮藥理學(xué)活性的過程和關(guān)鍵步驟[2]
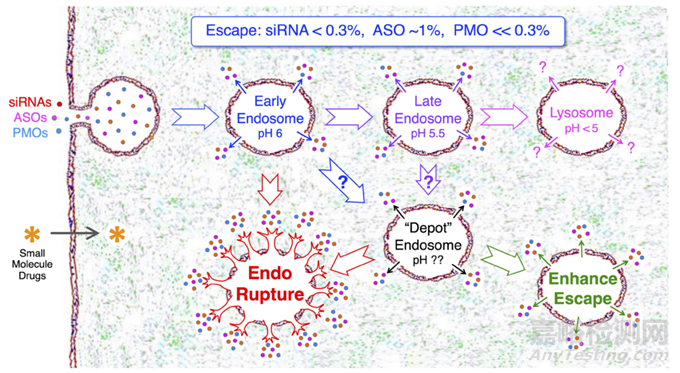
圖4. 兩種方案可提高 siRNA 內(nèi)體逃逸效率[3]
上述特點使得siRNA藥物的藥效學(xué)評價和臨床轉(zhuǎn)化面臨較大的挑戰(zhàn)���。未來需要開展更多關(guān)于siRNA藥物作用機制和PK過程(包括細胞內(nèi)PK)的定量研究�,以獲得更加精準的用于提示臨床有效性和指導(dǎo)臨床試驗設(shè)計的非臨床藥效學(xué)數(shù)據(jù)��。此外�,整合已有的非臨床和臨床數(shù)據(jù)對模型進行改進和優(yōu)化同樣重要。
1、體外活性和脫靶效應(yīng)評價
體外試驗是siRNA藥物研發(fā)的重要環(huán)節(jié)�,用于篩選靶向特異性強、活性高的siRNA序列��。通常,選擇人或動物的原代細胞?細胞系或轉(zhuǎn)染的細胞系作為試驗體系,考察siRNA對細胞活性?功能?相關(guān)蛋白和靶mRNA 水平的影響?借助體外試驗��,除了可考察對人體靶點的作用外����,還能評估對不同種屬mRNA的影響���,為毒理學(xué)試驗中相關(guān)種屬的選擇提供依據(jù)?根據(jù)FDA審評報告��,已上市的6款siRNA藥物均可濃度依賴性地調(diào)控靶mRNA并改變蛋白表達水平��,產(chǎn)生體外活性;均在猴體內(nèi)表現(xiàn)出藥理學(xué)活性?
表1. 已上市siRNA藥物相關(guān)種屬匯總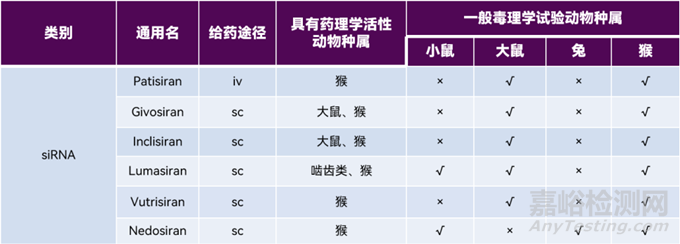
此外��,借助在線工具(in silico)對不同種屬間靶mRNA的同源性進行比對或預(yù)測其與候選siRNA藥物的配對情況����,為相關(guān)種屬的選擇提供參考;對人轉(zhuǎn)錄本中可能與候選siRNA藥物發(fā)生雜交的非目標序列(脫靶序列)進行初步篩選�,然后進行進一步的體外試驗和/或更全面的風(fēng)險評估(siRNA候選分子多層級脫靶效應(yīng)評估策略,發(fā)表中)��。
2�����、體內(nèi)藥效學(xué)
siRNA藥物與靶mRNA 的配對具有很高的特異性����,只有與靶mRNA同源性高的序列才能配對成功。通常����,通過1中所述手段進行相關(guān)種屬的選擇,然后在相關(guān)種屬動物中開展體內(nèi)藥效學(xué)研究����;非人靈長類動物是評價siRNA藥物體內(nèi)藥效學(xué)的重要模型,可以確定有效劑量范圍并評估給藥方案���。如沒有可產(chǎn)生藥理學(xué)活性的相關(guān)種屬,可選擇轉(zhuǎn)基因動物模型�����,或開展相應(yīng)的體外藥效學(xué)試驗?
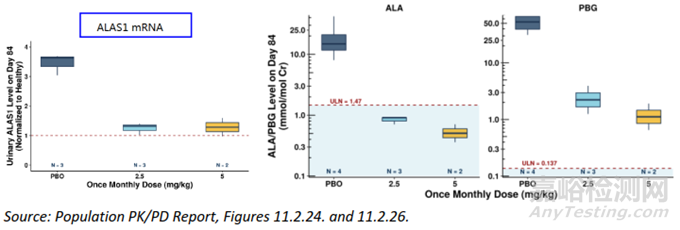
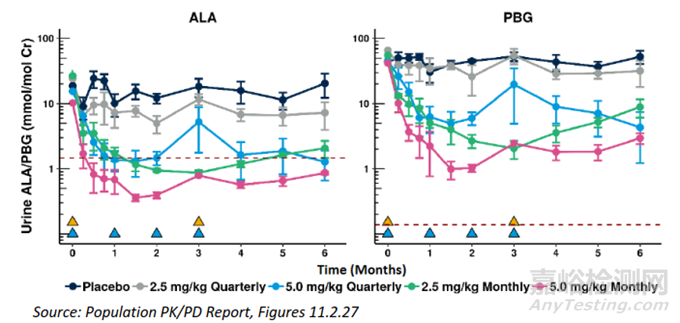
通過體內(nèi)藥效學(xué)試驗,可對劑量-效應(yīng)關(guān)系、時間-效應(yīng)關(guān)系��、療效相關(guān)生物標志物等進行探索����。此外,從定量藥理的角度����,PK/PD模型���、劑量-效應(yīng)-時間模型����、PK/PB模型等在siRNA藥物開發(fā)中發(fā)揮著重要作用,可用于將藥物研發(fā)從臨床前到臨床各階段的數(shù)據(jù)進行模擬���、外推和預(yù)測。對于研發(fā)者充分理解和利用siRNA藥物獨特的PK/PD關(guān)系��、指導(dǎo)siRNA藥物的開發(fā)至關(guān)重要���?�?茖W(xué)合理地設(shè)計臨床前藥效學(xué)試驗,結(jié)合轉(zhuǎn)化角度的研究,可以更好地支持siRNA產(chǎn)品的臨床試驗設(shè)計和人體療效預(yù)測����,有助于確定臨床首次人體試驗(FIH)及不同臨床階段的給藥方案,并用于NDA申請時作為支持臨床劑量選擇依據(jù)的描述��。已上市siRNA藥物�,如patisiran和givosiran的上市批準均采用了上述藥效學(xué)模型�����。
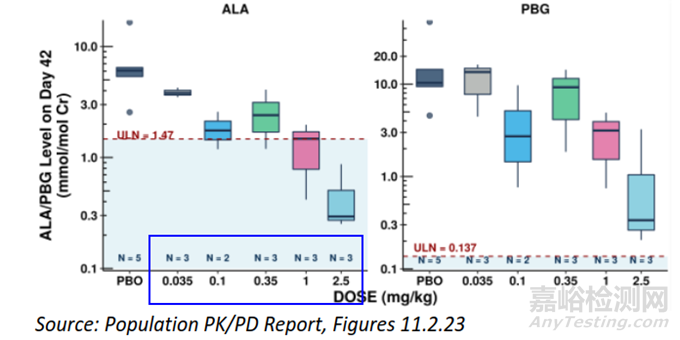
圖5. Givosiran劑量-尿ALA/PBG水平(上)�����、劑量-尿ALAS1 mRNA/ALA/RBG水平(中)、劑量-尿ALA/PBG水平(下)相關(guān)性分析[4]
參考資料:
[1] Guohua An. Pharmacokinetics and Pharmacodynamics of GalNAc-Conjugated siRNAs. The Journal of Clinical Pharmacology. 2024, 64(1) 45–57
[2] Jae Yoon Jeon, Vivaswath S. Ayyar. Amitava Mitra. Pharmacokinetic and Pharmacodynamic Modeling of siRNA Therapeutics – a Minireview. Pharmaceutical Research (2022) 39:1749–1759
[3] Steven F. Dowdy. Endosomal escape of RNA therapeutics: How do we solve this rate-limiting problem? RNA. 2023 Apr; 29(4): 396–401.
[4] MULTI-DISCIPLINE REVIEW of Givosiran.
https://www.accessdata.fda.gov/drugsatfda_docs/nda/2019/212194Orig1s000MultidisciplineR.pdf