老人和兒童是兩群最敏感且需要重點(diǎn)關(guān)注和保護(hù)的群體����。目前尚沒(méi)有針對(duì)老年人群的特定指導(dǎo)原則,但針對(duì)兒童和青少年藥物的非臨床評(píng)價(jià)指導(dǎo)原則���,F(xiàn)DA���、EMA和ICH等均有發(fā)布����。2009年,美國(guó)46%的藥物標(biāo)簽顯示可用于兒童����。然而,兒童并不是小號(hào)的成年人�,基于成年人數(shù)據(jù)上市的藥物給予兒童標(biāo)簽外用藥是有重大安全性風(fēng)險(xiǎn)的。兒童在解剖��、生理、發(fā)育方面的差異導(dǎo)致對(duì)于藥物代謝�、腎臟清除����、藥物-藥物相互作用及毒性敏感度等方面與成人可能是不同的。很多藥物在幼齡人群和成年人中的毒性表現(xiàn)也是有區(qū)別的�,比如氯霉素由于在幼齡人群中的半衰期和暴露量增加,會(huì)增加新生兒的死亡率���。又如吸入型糖皮質(zhì)激素會(huì)影響兒童的生長(zhǎng)速度�����。因此����,對(duì)于臨床擬用人群有未成年人的情況��,需要在幼齡動(dòng)物中開(kāi)展非臨床風(fēng)險(xiǎn)評(píng)估�。
幼齡動(dòng)物毒性評(píng)價(jià)最核心的關(guān)注點(diǎn)是出生后重要器官的發(fā)育毒性。比如大腦神經(jīng)發(fā)育會(huì)持續(xù)整個(gè)青春期(Adolescence)����,腎臟功能和胃腸道系統(tǒng)功能在1歲左右才達(dá)到成人水平,肺泡成熟通常在2歲左右��,免疫球蛋白IgG和IgA在5-12歲時(shí)達(dá)到成年人水平����,生殖系統(tǒng)在青春期才完全成熟,骨骼系統(tǒng)更是要到25-30歲發(fā)育結(jié)束�。因此,根據(jù)藥物的用藥人群年齡不同����,可能影響的器官發(fā)育、功能也會(huì)有所區(qū)別�。
而幼齡動(dòng)物研究結(jié)果在臨床兒童轉(zhuǎn)化方面是具有重要價(jià)值的。比如通過(guò)研究發(fā)育中的嚙齒動(dòng)物神經(jīng)系統(tǒng)����,發(fā)現(xiàn)了苯巴比妥對(duì)兒童認(rèn)知能力的影響。通過(guò)研究六氯苯酚對(duì)發(fā)育中大鼠和猴的神經(jīng)毒性����,成功提示了臨床新生兒的對(duì)應(yīng)風(fēng)險(xiǎn)。動(dòng)物試驗(yàn)發(fā)現(xiàn)未發(fā)育成熟心臟對(duì)鈣離子阻斷劑更為敏感����,這一結(jié)論對(duì)維拉帕米引起嬰兒心血管并發(fā)癥發(fā)生率增加有重要提示價(jià)值�。茶堿在幼齡動(dòng)物中發(fā)現(xiàn)的驚厥副作用�����,也在臨床幼年人群中得以驗(yàn)證�����。
幼齡動(dòng)物非臨床研究已經(jīng)有一系列指南和電子刊物發(fā)布�����,羅列如下:
1)FDA����,2006,Guidance for Industry: Nonclinical Safety Evaluation of Pediatric Drug Products.
2)EMA�����,2008�,Guideline on the Need for Nonclinical Testing in Juvenile Animals on Human Pharmaceuticals for Pediatric Indications.
3)JMHLW,2012�����,Guideline on Nonclinical Safety Studies in Juvenile Animals for Pediatric Drug Development.
4)ICH S11���,2020�,NONCLINICAL SAFETY TESTING IN SUPPORT OF DEVELOPMENT OF PAEDIATRIC PHARMACEUTICALS.
5)NMPA�����,2017���,兒科用藥非臨床安全性研究技術(shù)指導(dǎo)原則(征求意見(jiàn)稿)����。
6)黃芳華����,王慶利等,2017�����,《幼齡動(dòng)物毒理學(xué)研究: 試驗(yàn)設(shè)計(jì)��、實(shí)施和結(jié)果分析》。
7)單曉蕾�����,黃芳華等�����,2022����,《幼齡動(dòng)物毒理學(xué)試驗(yàn)的案例分析及考慮要點(diǎn)》。
當(dāng)然ICH M3����、ICH S6、ICH S9等指南對(duì)于符合特定產(chǎn)品分類����、適應(yīng)癥或通用要求的也是可以參照的。
那么什么情況下需要開(kāi)展幼齡動(dòng)物毒理研究呢��?
籠統(tǒng)的講���,當(dāng)現(xiàn)有的臨床數(shù)據(jù)�����、非臨床數(shù)據(jù)不能支持藥物在兒童患者中的安全性時(shí)��,幼齡動(dòng)物的非臨床研究就有了必要性���。比如:1)同類型產(chǎn)品(包括同靶點(diǎn)、同作用機(jī)制�、相似機(jī)制等)如果已經(jīng)有針對(duì)幼齡動(dòng)物毒性的擔(dān)憂;2)本品的臨床研究已有充分?jǐn)?shù)據(jù)提示潛在的風(fēng)險(xiǎn)��;3)非臨床成年動(dòng)物研究數(shù)據(jù)顯示出發(fā)育毒性風(fēng)險(xiǎn)���,或者提示有某些方面的特別擔(dān)憂����,需開(kāi)展進(jìn)一步研究����,如毒性的可逆性、充分的安全窗口探索等���;4)現(xiàn)有臨床����、非臨床安全性數(shù)據(jù)對(duì)于擬用于兒童的支持是不充分的。對(duì)于大部分藥物���,在用于兒童之前��,其實(shí)已經(jīng)有了成年人的安全性和有效性數(shù)據(jù)�����,甚至有些已經(jīng)有12歲以上未成年患者的數(shù)據(jù)��??梢越Y(jié)合已有的臨床前和臨床數(shù)據(jù)���,科學(xué)合理設(shè)計(jì)幼齡動(dòng)物的研究方案���。ICH S11對(duì)于是否需要額外開(kāi)展幼齡動(dòng)物非臨床安評(píng),建議進(jìn)行證據(jù)權(quán)重分析��,其中最重要的考量因素是臨床擬用患者的最小年齡以及對(duì)發(fā)育中器官系統(tǒng)是否有可疑影響�����,其它考量因素還包括前期資料完整度、藥物靶點(diǎn)對(duì)器官發(fā)育的作用�����、藥物的選擇性和特異性等��,如下圖所示�����。ICH S11附錄中關(guān)于證據(jù)權(quán)重分析決定幼齡動(dòng)物非臨床安評(píng)是否需要開(kāi)展給出了多個(gè)案例��,可以參考�����。

對(duì)于先用于兒科或兒科專用藥物�,如果可能����,建議先進(jìn)行成年健康志愿者試驗(yàn)。再根據(jù)成年動(dòng)物非臨床數(shù)據(jù)���、成年健康人體數(shù)據(jù)等進(jìn)行證據(jù)權(quán)重分析����。對(duì)于無(wú)法實(shí)現(xiàn)成年健康志愿者給藥,也無(wú)成年動(dòng)物數(shù)據(jù)支持的情況����,就需要開(kāi)展比較全面的幼齡動(dòng)物非臨床研究,包括幼齡嚙齒和幼齡非嚙齒類動(dòng)物一般毒理�����、安全藥理學(xué)���、遺傳毒性等�����。
研究設(shè)計(jì)和考量
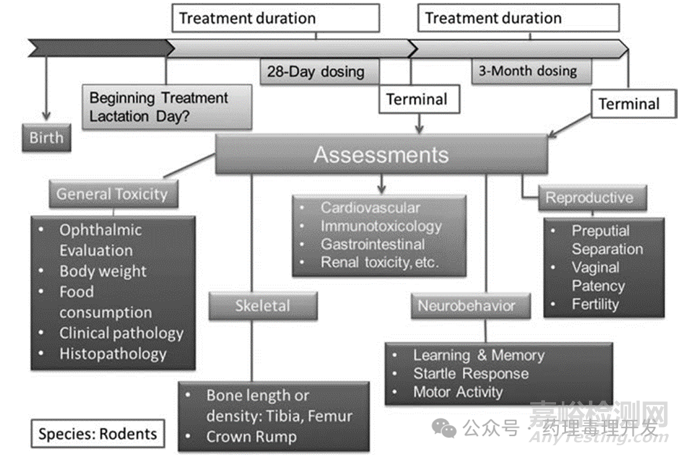
幼齡動(dòng)物毒理研究多以嚙齒類為主���,先從整體看下一項(xiàng)嚙齒類幼齡動(dòng)物毒理試驗(yàn),如下圖所示��。除了常規(guī)體重����、攝食量����、臨床病理�����、組織病理學(xué)檢查�����、眼科檢查外���,需要特別關(guān)注骨骼���、神經(jīng)系統(tǒng)����、生殖系統(tǒng)、心血管系統(tǒng)等發(fā)育情況�。另外,可以考慮將功能觀察組合測(cè)試(functional observation battery, FOB)嵌入一般毒性試驗(yàn)中�����。
種屬選擇方面,選擇依據(jù)與成年動(dòng)物類似����。如果前期已經(jīng)完成成年動(dòng)物毒理研究,且已經(jīng)有成年人體數(shù)據(jù)����,F(xiàn)DA、EMA����、ICH均認(rèn)為采用一種最相關(guān)種屬開(kāi)展幼齡動(dòng)物毒理研究即可。來(lái)自10家藥企的39個(gè)幼齡動(dòng)物毒理數(shù)據(jù)顯示����,大鼠是最常用種屬。但是���,如果擬開(kāi)發(fā)產(chǎn)品是兒科專用或先是兒科的適應(yīng)癥�����,這種情況下沒(méi)有前期成年動(dòng)物����、臨床數(shù)據(jù)支持,通常需要在兩個(gè)種屬(嚙齒+非嚙齒)幼齡動(dòng)物中開(kāi)展研究����,感興趣的可翻閱下脊髓性肌萎縮癥治療藥物諾西那生鈉(nusinersen,商品名Spinraza)的相關(guān)資料��。大鼠作為最常用種屬�,優(yōu)點(diǎn)是比較經(jīng)典,歷史對(duì)照資料豐富����,發(fā)育時(shí)間短,可進(jìn)行大量發(fā)育重點(diǎn)指標(biāo)的考察����,易于操作等。當(dāng)然��,大鼠也有其局限性��,具體優(yōu)�����、缺點(diǎn)如下表所示���。

對(duì)于生物制品�,如果大鼠不是相關(guān)種屬怎么辦��?用非人靈長(zhǎng)類(non-human primate���,NHP)開(kāi)展幼年動(dòng)物毒理研究嗎����?NHP開(kāi)展幼齡動(dòng)物毒理研究非常具有挑戰(zhàn)性�,離乳前用藥涉及繁殖、運(yùn)輸和母體/嬰仔對(duì)的處理�,離乳后(大約6個(gè)月齡)器官系統(tǒng)的成熟度通常已超過(guò)許多兒科相關(guān)年齡。如果有成年動(dòng)物發(fā)育和生殖毒理學(xué)試驗(yàn)數(shù)據(jù)�,主要是圍產(chǎn)期發(fā)育毒性試驗(yàn),可能足以支持兒科研究的非臨床風(fēng)險(xiǎn)����。如果沒(méi)有,可以考慮采用轉(zhuǎn)基因動(dòng)物���、替代分子或者其它體外試驗(yàn)系統(tǒng)等方案解決��。
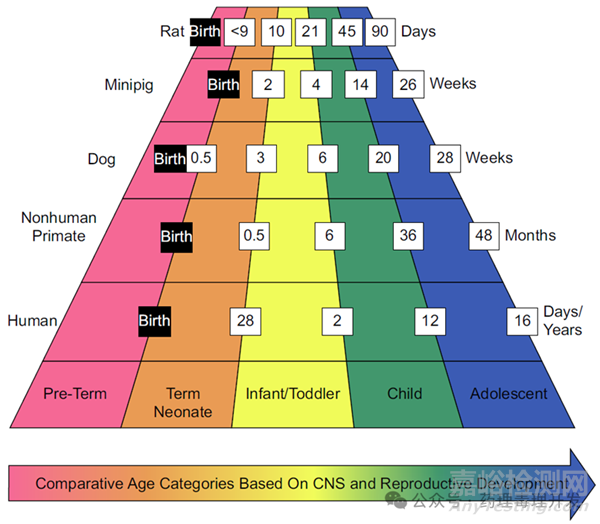
研究用動(dòng)物所屬年齡段與臨床擬暴露人群的年齡應(yīng)該具有可比性��,給藥起始年齡應(yīng)與臨床擬用最小年齡相當(dāng)�。下圖是不同種屬動(dòng)物和人體年齡對(duì)比示例圖。
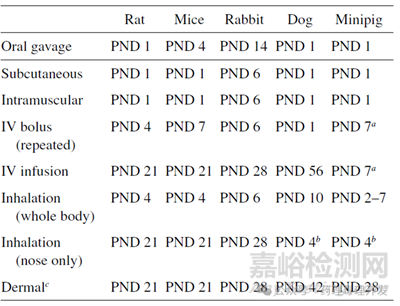
幼齡動(dòng)物一般不太建議從出生當(dāng)天就開(kāi)始給藥�,有可能會(huì)影響動(dòng)物的存活率。根據(jù)給藥途徑不同�,種屬不同,允許最早起始給藥時(shí)間如下表所示��。
對(duì)需離乳前給藥的��,一般持續(xù)1-3個(gè)月��。對(duì)于幼齡大鼠����,PND2-4,PND7和PND21開(kāi)始給藥���,可以分別支持新生兒��、1個(gè)月的嬰兒和2歲兒童的臨床試驗(yàn)��。給藥結(jié)束時(shí)動(dòng)物的年齡應(yīng)該是睪丸真正的成熟后(約PND59-63),或者至少覆蓋了發(fā)育的關(guān)鍵窗口期。這也是為什么大鼠使用最多的一個(gè)原因����,從開(kāi)始發(fā)育到性成熟的周期短。犬和小型豬的發(fā)育窗口期比大鼠長(zhǎng)很多��,非人靈長(zhǎng)類就更不實(shí)用了����。給藥起始年齡不合適是審評(píng)中的常見(jiàn)問(wèn)題,需要特別關(guān)注��。
劑量選擇方面���,F(xiàn)DA建議探索出清晰的劑量-效應(yīng)關(guān)系�。高劑量應(yīng)產(chǎn)生可識(shí)別的毒性����,如發(fā)育毒性或一般毒性。中劑量最好也產(chǎn)生一定程度的毒性反應(yīng)����。低劑量則產(chǎn)生輕微毒性或不產(chǎn)生毒性,如果可能�,最好是NOAEL劑量����。幼齡動(dòng)物毒性可能比成年動(dòng)物更為敏感����,也可能更不敏感,簡(jiǎn)單從成年動(dòng)物數(shù)據(jù)推導(dǎo)幼齡動(dòng)物并不合理�����,建議在開(kāi)展幼齡動(dòng)物正式毒理研究之前����,先開(kāi)展預(yù)試驗(yàn)進(jìn)行劑量探索。另外�,要避免毒性劑量水平過(guò)高導(dǎo)致生長(zhǎng)發(fā)育遲緩而引起器官系統(tǒng)的繼發(fā)性影響和/或母體忽略/拒絕哺乳幼仔。對(duì)體重產(chǎn)生明顯影響可能會(huì)混淆終點(diǎn)判斷����。
給藥途經(jīng)方面,給藥途經(jīng)要求與成年動(dòng)物研究類似���,與臨床擬用途徑保持一致����。如果無(wú)法實(shí)現(xiàn),需要說(shuō)明采用替代途徑給藥的原因及合理性�。兒童最常見(jiàn)的給藥途徑是口服,且因吞咽膠囊或片劑的難度��,液體制劑的設(shè)計(jì)更為合理��。嚙齒類動(dòng)物口服給藥�,通常最早開(kāi)始給藥的時(shí)間是出生后第4或7天(PND4或PND7)�。如果計(jì)劃出生后就開(kāi)始用藥,推薦腹腔或皮下注射����。年齡特別小的動(dòng)物,靜脈注射給藥難度很大�����,不是所有實(shí)驗(yàn)室均能熟練操作�����。另外����,給藥體積也需要特別注意�����,對(duì)于嚙齒類動(dòng)物�,不同的給藥途徑��,其給藥體積或適用年齡如下: 1)口服:5 mL/kg�����,超過(guò)此給藥容量會(huì)影響攝食�����;2)皮下給藥:3-5 mL/kg���,適合于PND 4 或更大年齡動(dòng)物�����。開(kāi)始時(shí)一般3個(gè)注射部位(肩胛�����、腰椎左右)給藥���,在成長(zhǎng)過(guò)程中���,最多可對(duì)5個(gè)部位給藥;3)靜脈注射:靜脈推注為5mL/kg����,小于PND18 不能重復(fù)靜脈注射給藥����;4)吸入給藥:離乳前采用全身暴露的方式,無(wú)法吸入給藥�;鼻腔給藥僅可在離乳后;5)經(jīng)皮給藥: 僅在離乳后可行�。
TK采血方面,細(xì)胞色素P450酶�����、藥物轉(zhuǎn)運(yùn)體和激素隨著發(fā)育而變化��,造成藥物在吸收�、分布、代謝和排泄方面的差異����,是導(dǎo)致兒童/青少年患者與成年人群毒性反應(yīng)敏感性不同的主要原因�。因此��,試驗(yàn)中包含TK 參數(shù)非常重要��。通常一般毒理試驗(yàn)中會(huì)設(shè)置衛(wèi)星組�����,采血時(shí)間點(diǎn)通常設(shè)置在首末次給藥��。另外�,由于幼齡動(dòng)物采血量有限,TK方法開(kāi)發(fā)時(shí)盡量減少分析所用樣本體積����,能實(shí)現(xiàn)微量檢測(cè)當(dāng)然最好,否則TK衛(wèi)星組可能要設(shè)置比較多的動(dòng)物用于采血����。還有一點(diǎn)需要注意,由于動(dòng)物在快速發(fā)育��,這其中就包括前述代謝酶、轉(zhuǎn)運(yùn)體��,所以幼齡動(dòng)物研究周期中的TK暴露量可能會(huì)出現(xiàn)較大的波動(dòng)�����。
分組設(shè)計(jì)方面��,由于幼齡動(dòng)物通常在離乳前即開(kāi)始給藥�,必須考慮同窩幼仔的分組問(wèn)題。常用的分組方法包括分窩設(shè)計(jì)(split-litter design)����、整窩設(shè)計(jì)(whole-litter design)�、交叉哺育(cross-fostering)。分窩設(shè)計(jì)指同一窩幼仔平均分配到各劑量組(in split-litter design, all dose levels should be equally represented within a litter)����,缺點(diǎn)是有交叉污染的風(fēng)險(xiǎn)。整窩設(shè)計(jì)指每窩幼仔接受同一劑量給藥(in whole-litter design, all pups from the same litter get the same dose)��,優(yōu)點(diǎn)是解決了交叉污染風(fēng)險(xiǎn)����,缺點(diǎn)是無(wú)法排除窩效應(yīng)和遺傳效應(yīng)的影響。交叉哺育可以最小化窩效應(yīng)和遺傳效應(yīng)影響,但又會(huì)存在非自然哺育引入的哺育效應(yīng)的問(wèn)題�。當(dāng)然,如果不涉及離乳前用藥���,分組需要考量的因素就會(huì)簡(jiǎn)化很多�����。
ICH S11推薦的分組方案是先構(gòu)建標(biāo)準(zhǔn)窩�,大多數(shù)幼仔與自然母親仍然在一起�����,每窩幼仔數(shù)標(biāo)準(zhǔn)化(比如5雌5雄)��,10窩為1個(gè)劑量組�����,下圖所示就是1個(gè)劑量組的動(dòng)物組成�����,A-J代表10窩��,每窩10只動(dòng)物,5雌和5雄代表了5個(gè)亞組�,分別用于不同的試驗(yàn)?zāi)康模械氖墙o藥結(jié)束剖檢用����,有的是TK用,有的是CNS行為學(xué)評(píng)估用��。這種設(shè)計(jì)有點(diǎn)類似整窩設(shè)計(jì)���,通過(guò)多窩組合減少窩效應(yīng)和遺傳效應(yīng)等混雜因素影響����。
檢測(cè)指標(biāo):通常���,幼齡動(dòng)物毒理研究需要關(guān)注出生后器官發(fā)育的影響比如骨骼、腎臟�����、肺����、神經(jīng)��、免疫系統(tǒng)和生殖系統(tǒng)��。終點(diǎn)指標(biāo)應(yīng)包括很多生長(zhǎng)相關(guān)指標(biāo)如冠臀長(zhǎng)度��、股骨和脛骨長(zhǎng)度����、性成熟的外部指征�����、體重��、體征�、臨床病理學(xué)、器官重量��、大體解剖和鏡檢����。下圖摘自黃芳華、王慶利等CDE老師發(fā)表的《幼齡動(dòng)物毒理學(xué)研究: 試驗(yàn)設(shè)計(jì)���、實(shí)施和結(jié)果分析》一文���,除了常規(guī)指標(biāo)����,還需要結(jié)合藥物的靶點(diǎn)生物學(xué)特征��、前期成年動(dòng)物毒理學(xué)數(shù)據(jù)��、臨床使用等case by case的設(shè)置針對(duì)性特殊評(píng)價(jià)指標(biāo)���。
最后
幼齡動(dòng)物的非臨床研究非常復(fù)雜����。首先�����,對(duì)于是否需要開(kāi)展附加的幼齡動(dòng)物非臨床研究進(jìn)行系統(tǒng)的證據(jù)權(quán)重分析�,不是所有兒科臨床研究均需要幼齡動(dòng)物數(shù)據(jù)支持。其次���,動(dòng)物給藥初始年齡選擇、給藥持續(xù)時(shí)間也需要結(jié)合臨床擬用人群���、動(dòng)物與人體器官發(fā)育的比較等進(jìn)行謹(jǐn)慎評(píng)估��。再就是劑量選擇����,并不是劑量越高越好,反而過(guò)猶不及�,會(huì)因?yàn)橄到y(tǒng)毒性影響對(duì)器官發(fā)育的評(píng)估。分組設(shè)計(jì)較成年動(dòng)物的考量因素復(fù)雜很多��,需要排除各種混雜因素的影響����。終點(diǎn)指標(biāo)的檢測(cè)除納入成年動(dòng)物毒理研究所選擇的常規(guī)指標(biāo),還需對(duì)器官系統(tǒng)的發(fā)育進(jìn)行重點(diǎn)研究�,某些靶點(diǎn)相關(guān)的特殊評(píng)價(jià)指標(biāo)也需要結(jié)合實(shí)際情況case by case分析。簡(jiǎn)簡(jiǎn)單單一篇文章很難全面���、系統(tǒng)的將幼齡動(dòng)物非臨床研究細(xì)節(jié)分析透徹��,好在ICH���、FDA、EMA等已經(jīng)有多個(gè)指導(dǎo)文件出臺(tái)�,也有大量已經(jīng)上市的藥物開(kāi)展過(guò)幼齡動(dòng)物非臨床研究��,公開(kāi)發(fā)表的文獻(xiàn)就更多了����,足以用來(lái)參考��。