摘 要 Abstract
伴隨著中藥工業(yè)化、現(xiàn)代化�、國際化進程,中藥監(jiān)管體系構建與能力提升正處在全球化監(jiān)管合作與監(jiān)管協(xié)調發(fā)展的戰(zhàn)略機遇期��。加快打造具有中國特色、符合中藥特點��、全球領先的中藥卓越監(jiān)管體系是我國構建“科學�、高效、權威”藥品監(jiān)管體系戰(zhàn)略的重要組成部分����,是中國式現(xiàn)代化藥品監(jiān)管實踐的新要求,是統(tǒng)籌高水平安全監(jiān)管和產(chǎn)業(yè)高質量發(fā)展的新舉措�。中藥卓越監(jiān)管體系作為新時代賦予藥監(jiān)人的新任務和新目標,其構建策略可概括為3 個層次�����、5 個維度和3 個機制:要聚焦中國特色����、中藥特點、全球領先3 個層次進行立體布局�����,要綜合法規(guī)制度�、組織機構、科技支撐�����、產(chǎn)業(yè)發(fā)展�����、國際影響5 個維度進行系統(tǒng)設計�,要圍繞中藥全鏈條監(jiān)管工作協(xié)調會商機制、中藥監(jiān)管科學研究者聯(lián)盟工作機制及中藥監(jiān)管全球化政策協(xié)調機制3 個工作進行方法創(chuàng)新�����,強化基礎學科向監(jiān)管應用轉化�����,支持中藥科學監(jiān)管決策�,推進高質量中藥傳承創(chuàng)新發(fā)展和高水平中藥監(jiān)管國際合作協(xié)調。
With the industrialization, modernization, and internationalization of traditional Chinese medicine (TCM), the regulatory system of TCM is currently experiencing a strategic opportunity to enhance global regulatory cooperation and coordination capabilities. Accelerating the development of a global leading TCM excellent regulatory system (TCM-ERS) with Chinese characteristics and in line with TCM's unique features is an important part of China's strategy to build a "scientific, efficient and authoritative" drug regulatory system. It represents a new requirement for drug regulatory practices in Chinesestyle modernization and a novel measure to coordinate high-level safety regulation with high-quality industrial development.The construction strategy of TCM-ERS, as a new task and goal assigned to drug regulatory authorities in the new era,can be summarized into three aspects: (1) a three-dimensional layout around three levels: Chinese characteristics, TCM characteristics, and global leadership. (2) a system from five dimensions: laws and regulations, organizational structure,technological support, industrial development, and international influence. (3) three working mechanisms: a TCM full chain coordination and consultation mechanism (TCM-FCCCM), a TCM regulatory science coalition mechanism (TCM-RSCM) and a TCM global policy coordination and regulation mechanism (TCM-GPCRM). Furthermore, it supports the transformation of basic disciplines into regulatory applications, assist scientific regulatory decision-making, and promote the inheritance and innovation of TCM.
關鍵詞 Key words
中藥����;中藥監(jiān)管科學;中藥卓越監(jiān)管體系�;構建策略;前景展望
traditional Chinese medicine (TCM); TCM regulatory science; TCM excellent regulatory system; building strategies; development prospects
中藥監(jiān)管從傳統(tǒng)的經(jīng)驗管理���、簡單的行政執(zhí)法���,到以科學為決策基礎的科學監(jiān)管�,再到信息化時代的智慧監(jiān)管�,科學技術的進步從來沒有像今天這樣深刻影響著中藥監(jiān)管事務、中藥產(chǎn)業(yè)發(fā)展及中藥傳承創(chuàng)新��。新時代新征程�����,要以習近平新時代中國特色社會主義思想為指導��,全面貫徹落實黨的二十大精神��,準確把握以中國式現(xiàn)代化全面推進中華民族偉大復興的新目標����,深刻領悟藥品監(jiān)管部門強化藥品安全監(jiān)管、促進中醫(yī)藥傳承創(chuàng)新��、“三醫(yī)”協(xié)同發(fā)展治理的新使命��,認真貫徹2024 年全國藥品監(jiān)督管理工作會議對中國式現(xiàn)代化藥品監(jiān)管實踐的新要求�,加快打造具有中國特色��、符合中藥特點����、全球領先的中藥卓越監(jiān)管體系的新任務����,建立中藥監(jiān)管科學研究轉化新機制[1]�,高位推進中醫(yī)藥傳承創(chuàng)新發(fā)展,不斷滿足人民群眾對中醫(yī)藥服務的需求����,為我國構建“科學、高效���、權威”藥品監(jiān)管體系發(fā)展戰(zhàn)略做出貢獻����。
1����、 高質量發(fā)展呼喚中藥卓越監(jiān)管體系
1.1 新興科技驅動中藥監(jiān)管主動變革
中藥作為在中醫(yī)藥理論指導下使用的藥用物質及其制劑,是中醫(yī)藥傳承創(chuàng)新發(fā)展的物質基礎���,具有悠久的臨床使用歷史��。隨著21 世紀科技飛速進步��,中藥新藥研發(fā)已經(jīng)采用系統(tǒng)生物學����、AI+、納米藥物等創(chuàng)新技術��,中藥生產(chǎn)創(chuàng)新也涉及連續(xù)制造��,先進的過程控制和自動化等先進工藝����。科學技術發(fā)展必然導致許多中藥新產(chǎn)品的出現(xiàn)和前所未有的監(jiān)管問題�,加之不同國家和地區(qū)藥品監(jiān)管部門的監(jiān)管要求和監(jiān)管環(huán)境存在較大差異,醫(yī)藥科技創(chuàng)新和藥品安全監(jiān)管也成為全球范圍內需要共同面對的監(jiān)管挑戰(zhàn)�。藥品創(chuàng)新和藥品監(jiān)管是針對同一個產(chǎn)品的不同視角的工作。從藥品監(jiān)管者的角度來看�,關注的是這些新技術新產(chǎn)品有效性、安全性證據(jù)是否充分����,有沒有受到嚴格的質量安全監(jiān)管��。從研發(fā)創(chuàng)新者的角度來看�,如果加強法規(guī)的監(jiān)管和過多的技術要求�,有可能阻礙創(chuàng)新的腳步和新產(chǎn)品的上市。
科技創(chuàng)新與嚴格監(jiān)管之間的矛盾和沖突直接推動了一門新興的監(jiān)管科學(Regulatory Science)誕生��。監(jiān)管科學從1970 年美國國家環(huán)境保護局(EPA)Alan Moghissi 提出概念�,到2010 年美國食品藥品監(jiān)督管理局(FDA)提出相對公認的科學定義,前后經(jīng)歷了邊界工作(boundary work����,1962 年)�����、超科學(trans-scientific���,1972 年)/跨科學(interdisciplinary��,1972 年)�、循證醫(yī)學(evidence based medicine�����,1990 年)、轉化醫(yī)學(translational medicine����,1996 年)、精準醫(yī)學(precision medicine�,2011 年)等多學科融合發(fā)展,現(xiàn)已成為21 世紀戰(zhàn)略性前沿學科[2]��。2019 年4 月����,國家藥監(jiān)局啟動中國藥品監(jiān)管科學行動計劃,通過中藥監(jiān)管科學研究基地�����、國家藥監(jiān)局中藥監(jiān)管重點實驗室���、中藥監(jiān)管科學重點項目“三位一體”整體推動��,中藥監(jiān)管科學研究及成果轉化應用步入快車道����。2020 年9 月,國家藥監(jiān)局對中藥注冊分類進行重大調整����,新分類包括中藥創(chuàng)新藥、中藥改良型新藥�����、古代經(jīng)典名方中藥復方制劑�����、同名同方藥[3]����。新的中藥注冊分類注重以臨床價值為導向�,鼓勵具有中醫(yī)藥特點的中藥復方制劑創(chuàng)新,不再僅以物質基礎劃分注冊類別和評價藥物研制水平及藥物療效的高低[4]��。國家藥監(jiān)局2023 年1 月發(fā)布《關于進一步加強中藥科學監(jiān)管促進中藥傳承創(chuàng)新發(fā)展的若干措施》���、2023 年2 月發(fā)布《中藥注冊管理專門規(guī)定》�,主動采取措施以適應日新月異科技進步的挑戰(zhàn)���。2023 年5 月��,國家藥監(jiān)局中藥監(jiān)管科學研究團隊及相關技術團隊��,首次對中藥監(jiān)管科學(TCM Regulatory Science�����,TCMRS)的科學內涵和定義進行詮釋���,即通過中西醫(yī)跨學科知識�、技術融合研究����,創(chuàng)新研發(fā)符合中藥特點的新工具、新標準和新方法��,用以評估受監(jiān)管中藥產(chǎn)品的安全性�����、有效性�、質量和風險獲益綜合性能的新興科學,進而發(fā)展中藥監(jiān)管科學創(chuàng)新體系���、轉化體系����、學科體系及國際協(xié)調體系,不斷強化我國中藥監(jiān)管體系建設和科學監(jiān)管能力提升���,強化對復雜多樣的中藥新技術新產(chǎn)品質量和安全進行有效監(jiān)管�,為建立具有中國特色�、符合中藥特點、全球領先的中藥卓越監(jiān)管體系提供科技支撐[5-6]�。中藥監(jiān)管科學作為我國新興的、亟待發(fā)展的中西醫(yī)交叉融合科學�����,不僅是監(jiān)管科學在中藥監(jiān)管領域的全新應用場景��,更是一種根植于傳統(tǒng)中醫(yī)藥學土壤的中西醫(yī)融合研究新模式和原創(chuàng)性科學思維方式[7]��。
1.2 產(chǎn)業(yè)發(fā)展挑戰(zhàn)中藥安全監(jiān)管
我國是全球最大的中藥研發(fā)���、生產(chǎn)及使用市場。我國中藥工業(yè)經(jīng)過近30 年的快速發(fā)展����,已經(jīng)建立了較為完備的全產(chǎn)業(yè)鏈質量安全監(jiān)管體系和中藥產(chǎn)業(yè)生態(tài)�。截至2022 年底���,中藥生產(chǎn)企業(yè)4569 家���,其中中成藥生產(chǎn)企業(yè)2319 家,中藥飲片生產(chǎn)企業(yè)2250 家����,專營中藥材、中藥飲片的藥品經(jīng)營企業(yè)486 家�����。中藥營業(yè)收入6919 億元(同比增長12.4%)����,利潤總額1005 億元(增長37.1%)。其中����,中成藥營業(yè)收入4862 億元(增長11.8%),利潤總額755 億元(增長23.2%)��;中藥飲片營業(yè)收入2057 億元(增長13.7%),利潤總額249 億元(增長102%)����。國家藥監(jiān)局監(jiān)管的中藥批準文號57 991 項,制劑品種8670 個���;2020 年版《中國藥典》一部收載中藥標準 2711 項���,局頒中藥標準13 091 項。現(xiàn)有中藥配方顆粒生產(chǎn)企業(yè)73 家�,上市備案15 718 件,品種880 個���。中藥醫(yī)療機構制劑批準文號總數(shù)16 548 個�,按傳統(tǒng)工藝備案13 434 個[8-9]����。
2023 年8 月,國務院常務會議審議通過《醫(yī)藥工業(yè)高質量發(fā)展行動計劃(2023 - 2025 年)》《醫(yī)療裝備產(chǎn)業(yè)高質量發(fā)展行動計劃(2023 -2025 年)》��,強調“要充分發(fā)揮我國中醫(yī)藥獨特優(yōu)勢����,加大保護力度,維護中醫(yī)藥發(fā)展安全”����。與國際上傳統(tǒng)藥、天然藥物�����、草藥或現(xiàn)代藥的定義不盡相同�,我國中藥產(chǎn)品既有采用傳統(tǒng)工藝、傳統(tǒng)給藥途徑�����、傳統(tǒng)劑型���,功能主治以中醫(yī)術語表述的古代經(jīng)典名方中藥復方制劑��,也有新發(fā)現(xiàn)的中藥材����、新的藥用部位及珍稀瀕危中藥替代品及其制劑�,還有化學成分明確的小分子藥物或組分相對明確的中藥提取物及其制劑。藥品監(jiān)管部門監(jiān)管的中藥產(chǎn)品涉及中藥材�����、提取物、中藥飲片���、配方顆粒�、醫(yī)院制劑��、中成藥等����,在產(chǎn)業(yè)、文化����、生態(tài)、衛(wèi)生等多個產(chǎn)業(yè)領域發(fā)揮重要而又獨特的作用���,不能簡單套用國際上的傳統(tǒng)藥�、草藥��、天然藥物或者現(xiàn)代藥規(guī)則對中藥進行監(jiān)管���。2023 年12 月中央經(jīng)濟工作會議強調���,“要以科技創(chuàng)新推動產(chǎn)業(yè)創(chuàng)新��,特別是以顛覆性技術和前沿技術催生新產(chǎn)業(yè)、新模式��、新動能�,發(fā)展新質生產(chǎn)力”。中藥產(chǎn)業(yè)需要開辟未來產(chǎn)業(yè)新賽道����,中藥監(jiān)管也要主動服務產(chǎn)業(yè)需求,統(tǒng)籌高水平安全監(jiān)管和產(chǎn)業(yè)高質量發(fā)展����,加快傳統(tǒng)產(chǎn)業(yè)轉型升級,推動我國從中藥制藥大國向中藥制藥強國跨越��。
1.3 中藥傳承創(chuàng)新呼喚卓越監(jiān)管
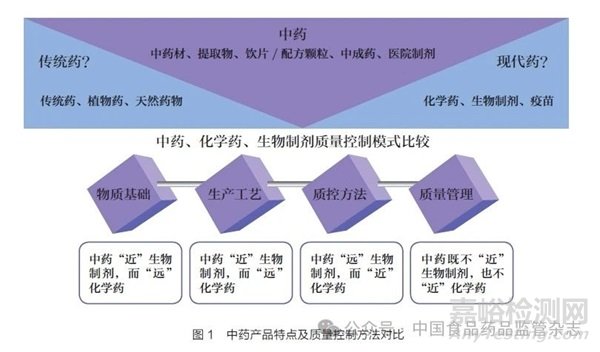
2019 年10 月《中共中央 國務院關于促進中醫(yī)藥傳承創(chuàng)新發(fā)展的意見》強調��,建立健全符合中醫(yī)藥特點的中藥安全�����、療效評價方法和技術標準。2021 年5 月��,習近平總書記在南陽醫(yī)圣祠考察時強調����,要做好守正創(chuàng)新、傳承發(fā)展工作�����,積極推進中醫(yī)藥科研和創(chuàng)新�����,為人民群眾提供更加優(yōu)質的健康服務����。2023 年5 月,習近平總書記在考察石家莊市國際生物醫(yī)藥園時強調�����,“要堅持人民至上�、生命至上,研發(fā)生產(chǎn)更多適合中國人生命基因傳承和身體素質特點的‘中國藥’��,特別是要加強中醫(yī)藥傳承創(chuàng)新發(fā)展”。中藥兼有中醫(yī)屬性和藥品屬性�,這類特殊而重要商品的監(jiān)管挑戰(zhàn)和困難也不言而喻。中藥傳承創(chuàng)新呼喚具有中國特色��、符合中藥特點的卓越監(jiān)管體系�。一方面,在中藥監(jiān)管立法的過程中�,由于傳統(tǒng)中醫(yī)屬性的個體用藥與現(xiàn)代藥品屬性的群體用藥的理論不同���,在中醫(yī)藥理論指導下的中藥復方組合用藥��,在面臨批準或者不批準��、撤市或者不撤市的監(jiān)管決策關頭��,如何避免“以西律中”�����,建立既符合中醫(yī)藥特點����,又符合群體用藥的有效性��、安全性、質量及獲益風險評估要求的中藥新藥審評標準評價體系和制度[10] ��;另一方面��,在中藥產(chǎn)品生產(chǎn)過程中�,中藥產(chǎn)品既不等同于國外的傳統(tǒng)藥、草藥或天然藥物���,也很難與現(xiàn)代藥畫等號��,從中藥�、化學藥�����、生物制劑特點及質量控制模式比較不難發(fā)現(xiàn)����,中藥的物質基礎、生產(chǎn)工藝“近”生物制劑而“遠”化學藥����,但中藥現(xiàn)行質量控制方法卻“遠”生物制劑而“近”化學藥,質量管理則既不“近”生物制劑�,也不“近”化學藥(圖1)[11]����。以上均反映出建立健全符合中醫(yī)藥特點的中藥安全����、療效評價方法和技術標準的重要性和緊迫性。
2 ����、中藥卓越監(jiān)管體系構建的設計策略
2.1 卓越藥品監(jiān)管體系的科學內涵
盡管我國的藥事管理最早可以追溯到3000 年前的西周時期,但現(xiàn)代意義的獨立的藥品監(jiān)管體系建設始于1998 年成立的國家藥品監(jiān)督管理局(直屬國務院)�����,2018 年機構改革設立國家藥品監(jiān)督管理局劃歸新成立的國家市場監(jiān)督管理總局管理���,至2023 年中國藥品監(jiān)管體制改革歷經(jīng)25 年[6,12]。2023 年7 月5 日國務院新聞辦舉行“強化藥品監(jiān)管 切實保障人民群眾用藥安全”發(fā)布會���,國家藥監(jiān)局堅決貫徹落實習近平總書記關于藥品監(jiān)管的重要指示批示精神��,持續(xù)深化藥品醫(yī)療器械審評審批制度改革����,持續(xù)強化藥品全生命周期質量監(jiān)管,有效維護了藥品安全形勢的總體穩(wěn)定���,推動我國從制藥大國向制藥強國跨越����,有力保護和促進了公眾健康[13]�。新時期中國式現(xiàn)代化藥品監(jiān)管實踐對中藥監(jiān)管提出新要求:加快打造具有中國特色、符合中藥特點��、全球領先的中藥卓越監(jiān)管體系[1]��。
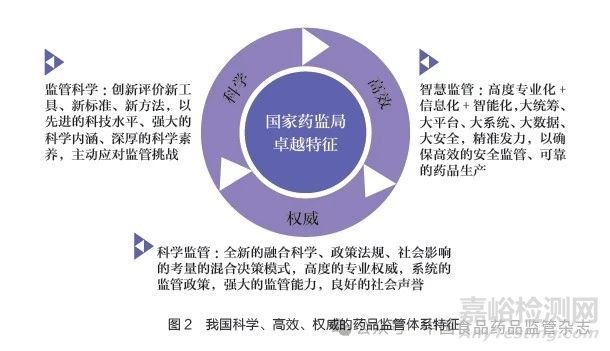
就全球范圍藥品監(jiān)管實踐來看��,F(xiàn)DA 自稱為國際上最強大�、最先進的監(jiān)管機構,無論是美國藥物監(jiān)管法律�����,還是美國制藥工業(yè)都已經(jīng)成為全球制藥工業(yè)的領跑者[14-15]�。FDA 藥品監(jiān)管體系的“卓越”特征,對內表現(xiàn)為強大的科學內涵和科學文化��,對外呈現(xiàn)高度專業(yè)性�,以及由此而來的權威性和社會聲譽[2]����。我國在2006 年8 月全國食品藥品監(jiān)督管理工作座談會就提出“科學監(jiān)管”概念[16]�。2019 年4 月,國家藥監(jiān)局實施中國藥品監(jiān)管科學行動計劃�。2021 年4 月,《國務院辦公廳關于全面加強藥品監(jiān)管能力建設的實施意見》正式提出“加快建立健全科學����、高效、權威的藥品監(jiān)管體系”����。2023 年7月,國家藥監(jiān)局印發(fā)《全面強化藥品監(jiān)管科學體系建設實施方案》�。2023 年11 月,國家藥監(jiān)局提出要全面貫徹黨的二十大精神�,認真落實習近平總書記關于藥品安全“四個最嚴”重要要求����,建立科學高效權威的藥品監(jiān)管體系,不斷強化高效能監(jiān)管�����,保障高水平安全,促進高質量發(fā)展[17]�。我國藥品監(jiān)管部門在推動我國從制藥大國向制藥強國跨越的進程中,監(jiān)管能力建設重點圍繞“創(chuàng)新���、質量����、效率����、體系、能力”五大主題����,聚焦“科學、高效�����、權威”三大核心內容�,開啟了我國藥品監(jiān)管體制機制創(chuàng)新的新階段?����?梢姡覈?ldquo;卓越”藥品監(jiān)管體系具有自身的科學內涵�����,其核心內容:一是“科學”���,基于監(jiān)管科學新工具����、新標準�����、新方法����,以先進的科技水平、強大的科學內涵�、深厚的科學素養(yǎng),主動迎接監(jiān)管挑戰(zhàn)��;二是“高效”�����,基于高度“專業(yè)化+信息化+ 智能化”的智慧監(jiān)管�,大統(tǒng)籌、大平臺��、大系統(tǒng)�、大數(shù)據(jù)、大安全�,以確保高效的安全監(jiān)管、可靠的藥品生產(chǎn)��;三是“權威”�����,完善的政策法規(guī)體系�,高素質的專業(yè)人才隊伍,創(chuàng)新性混合決策模式���,彰顯高度的專業(yè)權威����,具有良好的社會聲譽(圖2)����。
2.2 中藥卓越監(jiān)管體系構建的戰(zhàn)略目標
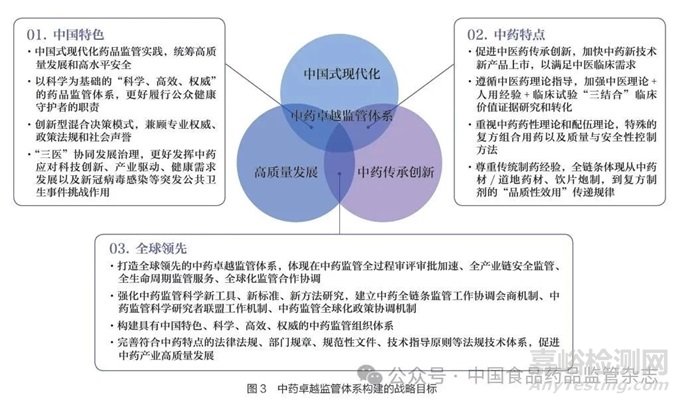
中藥卓越監(jiān)管體系作為我國“科學���、高效、權威”藥品監(jiān)管體系的重要組成部分�,其頂層設計具有更加豐富的戰(zhàn)略考量和科學內涵,要從具有中國特色��、符合中藥特點���、全球領先3 個層次進行設計(圖3)����。
(1)中國特色:核心是堅持中國式現(xiàn)代化的發(fā)展道路�。我國獨特的文化傳統(tǒng),獨特的歷史命運�����,獨特的基本國情��,注定了我們必然要走適合自己特點的發(fā)展道路����。中國式現(xiàn)代化藥品監(jiān)管實踐��,要建立以科學為基礎的“科學、高效���、權威”的藥品監(jiān)管體系����,要統(tǒng)籌高質量發(fā)展和高水平安全����。要創(chuàng)新科學監(jiān)管混合決策模式,兼顧專業(yè)權威�、政策法規(guī)和社會聲譽,更好履行公眾健康守護者的職責����。要堅持“三醫(yī)”協(xié)同發(fā)展治理,更好發(fā)揮中藥應對科技創(chuàng)新���、產(chǎn)業(yè)驅動�、健康需求發(fā)展以及新冠病毒感染等突發(fā)公共衛(wèi)生事件挑戰(zhàn)作用�。
(2)中藥特點:重點是建立具有中藥特點的審評審批體系。要遵循中醫(yī)藥理論指導����,促進中醫(yī)藥傳承創(chuàng)新�����。加強中醫(yī)理論+ 人用經(jīng)驗+ 臨床試驗“三結合”臨床價值證據(jù)研究和轉化�。要重視中藥特殊的藥性(毒性)理論和配伍理論��,特殊的復方組合用藥以及質量與安全性控制方法�����。要尊重傳統(tǒng)制藥經(jīng)驗和質量控制方法��,體現(xiàn)從中藥材/ 道地藥材����、飲片炮制,到復方制劑全鏈條的“品質性效用”傳遞規(guī)律��,加快中藥新技術新產(chǎn)品上市�,以滿足中醫(yī)臨床需求。
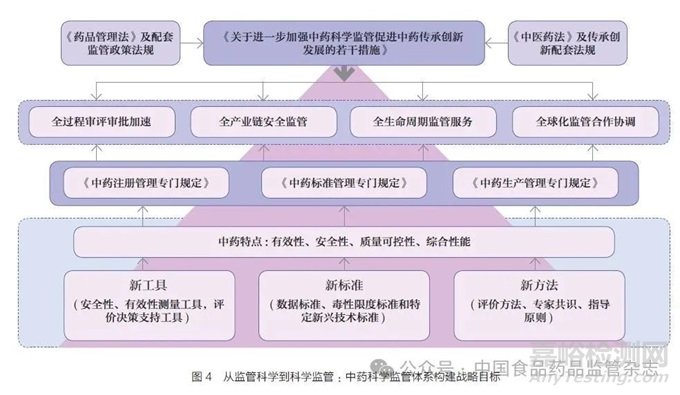
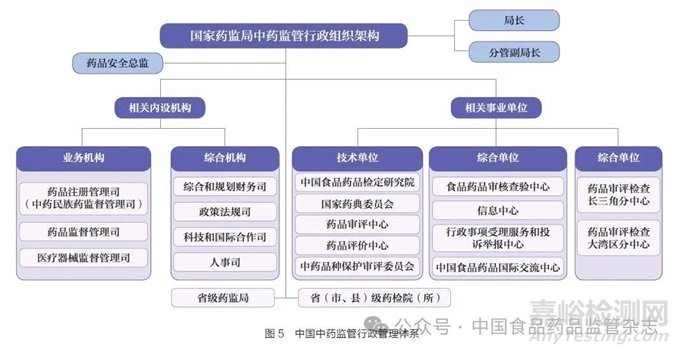
(3)全球領先:關鍵是高質量發(fā)展和高水平對外開放����。全球領先的基礎是高質量發(fā)展�,是創(chuàng)新成為第一動力���、協(xié)調成為內生特點��、綠色成為普遍形態(tài)、開放成為必由之路�、共享成為根本目的的發(fā)展,是國家推進高水平對外開放的必然要求�����。全球領先中藥卓越監(jiān)管體系要以全方位中藥監(jiān)管科學創(chuàng)新為支撐���,實現(xiàn)監(jiān)管全過程審評審批加速�、全產(chǎn)業(yè)鏈安全監(jiān)管��、全生命周期監(jiān)管服務����、全球化監(jiān)管合作協(xié)調(圖4)。強化中藥監(jiān)管科學新工具�、新標準、新方法研究�����,建立中藥全鏈條監(jiān)管工作協(xié)調會商機制、中藥監(jiān)管科學研究者聯(lián)盟工作機制����、中藥監(jiān)管全球化政策協(xié)調機制,完善符合中藥特點的法律法規(guī)�����、部門規(guī)章���、規(guī)范性文件�����、技術指導原則等法規(guī)技術體系[18]����,支持基礎學科向監(jiān)管應用轉化�,支持中藥科學監(jiān)管決策,構建具有中國特色�、高效運轉的中藥監(jiān)管行政管理體系(圖5)
3、 中藥卓越監(jiān)管體系實踐成效與發(fā)展前瞻
3.1 中藥卓越監(jiān)管體系的建設內容
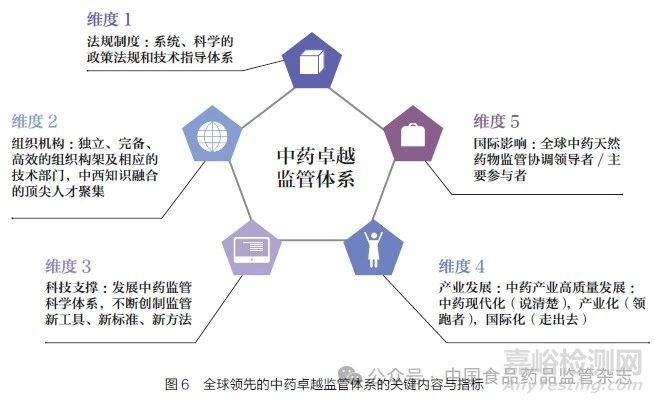
通過全球范圍內藥品監(jiān)管體系建設比較研究��,結合我國藥監(jiān)工作實踐和建立健全科學高效權威的藥品監(jiān)管體系戰(zhàn)略目標,我們提出構建“全球領先的中藥卓越監(jiān)管體系”重點內容�,在中國特色、中藥特點�����、全球領先3 個層次戰(zhàn)略布局基礎上�,要綜合法規(guī)制度、組織機構��、科技支撐�、產(chǎn)業(yè)發(fā)展����、國際影響5 個維度進行系統(tǒng)設計,完善工作內容和核心指標(圖6)����,確保全球領先戰(zhàn)略目標達成。
(1)法規(guī)制度:系統(tǒng)����、科學的政策法規(guī)和技術指導體系,涵蓋產(chǎn)品研發(fā)�����、審評審批、標準管理��、安全生產(chǎn)��、流通����、使用等全產(chǎn)業(yè)鏈和全生命周期的安全監(jiān)管。
(2)組織機構:獨立�、完備、高效的組織構架及中西知識融合的頂尖人才聚集����,確保管理運行的科學、高效�、權威。
(3)科技支撐:強化中藥監(jiān)管科學體系和轉化機制建設����,不斷創(chuàng)制符合中藥特點的監(jiān)管新工具、新標準�����、新方法。
(4)產(chǎn)業(yè)發(fā)展:通過中藥監(jiān)管創(chuàng)新和智慧監(jiān)管����,支持中藥產(chǎn)業(yè)化、現(xiàn)代化����、國際化,實現(xiàn)傳統(tǒng)中藥產(chǎn)業(yè)轉型升級和高質量發(fā)展�,成就我國中藥的“強大產(chǎn)業(yè)”。
(5)國際影響:建立中藥全鏈條監(jiān)管工作協(xié)調會商機制��,中藥監(jiān)管科學研究者聯(lián)盟工作機制���,中藥監(jiān)管全球化政策協(xié)調機制,全球中藥天然藥物監(jiān)管協(xié)調領導者/ 主要參與者�。
3.2 中藥卓越監(jiān)管體系的實踐與成效
(1)組建中藥監(jiān)管高端智庫。首次組建由中醫(yī)藥領域和其他相關學科領域的院士�����、國醫(yī)大師以及資深專家組成的中藥管理戰(zhàn)略決策專家咨詢委員會�。組建專門的中藥材生產(chǎn)質量管理規(guī)范(GAP)專家工作組、珍稀瀕危中藥材替代品監(jiān)管政策與技術要求研究專家工作組���、含馬兜鈴酸類成份中藥安全風險控制專家工作組��、已上市中藥注射劑上市后研究和評價專家工作組等�����。初步構建中藥監(jiān)管決策咨詢制度��,形成定位明晰�、特色鮮明、規(guī)模適度�����、布局合理的具有中國特色的中藥監(jiān)管智庫體系���。
(2)大力發(fā)展中藥監(jiān)管科學�����。實施中國藥品監(jiān)管科學行動計劃���、《全面強化藥品監(jiān)管科學體系建設實施方案》,組建中藥監(jiān)管科學研究基地2 家,國家藥監(jiān)局中藥監(jiān)管重點實驗室27 家�,開展中藥監(jiān)管科學重點項目研究并形成一批中藥監(jiān)管新工具、新標準�����、新方法����。成立中國藥品監(jiān)督管理研究會中藥監(jiān)管研究專業(yè)委員會、中國藥學會監(jiān)管科學與國際規(guī)范專業(yè)委員會等�����。召開首屆國家中藥科學監(jiān)管大會(2022 年7 月14 日��,北京)��、第二屆國家中藥科學監(jiān)管大會(2023 年7 月18 日�,上海)����、第六屆中國藥品監(jiān)管科學大會、中藥監(jiān)管科學研究——中藥新藥審評審批新工具新標準新方法研討會��、中國藥學會監(jiān)管科學與國際規(guī)范專業(yè)委員會成立大會暨第一屆監(jiān)管科學與國際規(guī)范大會、國家中藥科學監(jiān)管大會中藥監(jiān)管科學平行論壇等���,積極推動粵港澳三地藥品監(jiān)管部門協(xié)作會議機制���、西太區(qū)草藥監(jiān)管協(xié)調論壇(FHH)、中國- 東盟��、瀾湄國家�����、金磚國家傳統(tǒng)藥監(jiān)管研討等會議和監(jiān)管協(xié)調�。研究完成《中藥監(jiān)管科學戰(zhàn)略研究報告》,編輯出版《中國中藥監(jiān)管政策法規(guī)與技術指引》《2021 國家中藥監(jiān)管藍皮書》《2022 國家中藥監(jiān)管藍皮書》等����,為中藥科學監(jiān)管和智慧監(jiān)管提供技術支撐。
(3)強化中藥全產(chǎn)業(yè)鏈質量安全監(jiān)管���。深入推進藥品安全鞏固提升行動���,創(chuàng)新建立《中藥全鏈條監(jiān)管工作協(xié)調會商機制工作方案》。研究制定《中藥生產(chǎn)管理專門規(guī)定》以及制修訂《中藥材生產(chǎn)質量管理規(guī)范》《中藥品種保護條例》《實施審批管理的中藥材品種目錄》《實施審批管理的中藥飲片品種目錄》《地區(qū)性民間習用藥材管理辦法》等重要文件�����,印發(fā)《關于進一步加強中藥生產(chǎn)質量監(jiān)管工作的通知》,組建中藥材GAP 專家工作組�,開展中藥材GAP 監(jiān)督實施示范省(自治區(qū)����、直轄市)建設,加強中成藥上市后監(jiān)測和評價��。2023年抽檢中成藥43 個品種5584 批次�、中藥飲片9 個品種2185 批次,合格率分別達到99.5% 和97.1%�����,中藥質量整體情況持續(xù)穩(wěn)定向好�。
(4)深化中藥審評審批制度改革。研究制定《關于進一步加強中藥科學監(jiān)管促進中藥傳承創(chuàng)新發(fā)展的若干措施》《中藥注冊管理專門規(guī)定》《中藥標準管理專門規(guī)定》及系列中藥研究技術指導原則等���,不斷完善中藥全鏈條全生命周期監(jiān)管體系�,我國中藥監(jiān)管進入全方位科學監(jiān)管新階段�����。近年來����,中藥注冊審評新藥臨床試驗申請(IND)、新藥上市申請(NDA)和補充申請受理數(shù)量均大幅增長���,2021~2023 年分別有12���、10、11 個新藥獲批上市(以受理號計)����,并在2023 年首次實現(xiàn)了新的中藥(天然藥物)注冊分類調整后4 個類別的全覆蓋。
(5)全方位推進中藥監(jiān)管國際協(xié)調���。我國高度重視藥品監(jiān)管國際協(xié)調��,共同應對不斷出現(xiàn)的新問題和新挑戰(zhàn)��。充分發(fā)揮西太區(qū)草藥監(jiān)管協(xié)調論壇(FHH)��、第7 屆中國- 東盟藥品合作發(fā)展高峰論壇�、瀾湄國家����、金磚國家傳統(tǒng)藥監(jiān)管研討會議及亞洲合作資金項目����、中國- 東盟合作基金作用�,成功推選中國澳門成為FHH 正式會員,并推動設立FHH 永久秘書處落戶澳門大學��。完成22 個中藥技術文件翻譯工作���,為對外交流宣傳推廣提供基礎��。2023 年9 月���,筆者等出席第13 屆全球監(jiān)管科學峰會(GSRS),以“中國藥品監(jiān)管的科學化進程”為題進行了大會報告�,并與FDA 以及有關藥品企業(yè)、行業(yè)協(xié)會進行了交流��。近年來����,我國的監(jiān)管科學和新興技術研究取得了重要突破,尤其是中藥監(jiān)管體系建設和監(jiān)管成效引起了國際上高度重視�,顯著提升了我國在國際監(jiān)管科學領域的影響力�。
中藥監(jiān)管體系建設�、能力和成效得到業(yè)界高度評價:① 2023 年2 月25 日����,中華中醫(yī)藥學會發(fā)布2022 年度中醫(yī)藥十大學術進展——學術研究助力“三結合”中藥注冊審評證據(jù)體系構建[19]。② 2023 年12 月7 日�,中華中醫(yī)藥學會發(fā)布《新時代中醫(yī)藥標志性科技成果(2012-2022)》——中藥新藥審評理念革新推動一批代表性新藥獲批[20]。③ 2023 年12 月25 日����,《中國醫(yī)藥報》評出2023 年度中國醫(yī)藥十大新聞——中藥科學監(jiān)管開創(chuàng)新局面[21]。④ 2024 年1 月22 日��,《中國中醫(yī)藥報》評選2023 年中醫(yī)藥十大新聞——國家藥監(jiān)局發(fā)布《中藥注冊管理專門規(guī)定》�,加快推進完善中醫(yī)藥理論、人用經(jīng)驗和臨床試驗相結合(“三結合”)的中藥審評證據(jù)體系����,加速中藥新藥研發(fā)和產(chǎn)業(yè)發(fā)展[22] 等。
3.3 中藥卓越監(jiān)管體系發(fā)展前瞻
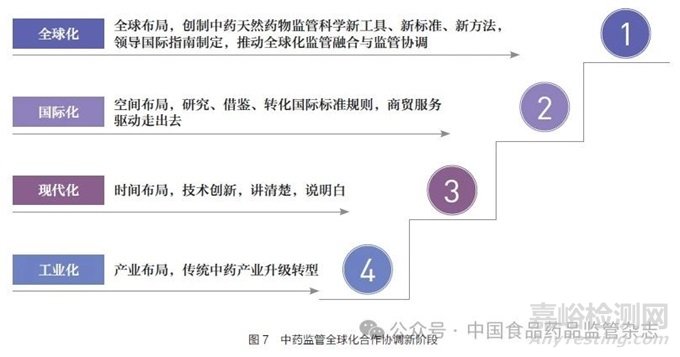
伴隨著中藥工業(yè)化����、現(xiàn)代化、國際化進程����,中藥監(jiān)管體系建設與能力提升正處在全球化中藥監(jiān)管融合與監(jiān)管協(xié)調發(fā)展的戰(zhàn)略機遇期(圖7)[23]�。國家藥監(jiān)局2024 年工作要點明確提出���,持續(xù)推進《關于進一步加強中藥科學監(jiān)管促進中藥傳承創(chuàng)新發(fā)展的若干措施》落實��,加快打造具有中國特色���、符合中藥特點、全球領先的中藥卓越監(jiān)管體系�,建立中藥監(jiān)管科學研究轉化機制。這是新時代賦予藥監(jiān)人的新任務�,是中國式現(xiàn)代化藥品監(jiān)管實踐的新要求,是統(tǒng)籌高質量發(fā)展和高水平安全�,是促進中藥傳承創(chuàng)新發(fā)展的根本保證。
中藥卓越監(jiān)管體系作為我國“科學��、高效��、權威”藥品監(jiān)管體系的重要組成部分���,是實現(xiàn)中藥高水平安全監(jiān)管和高質量產(chǎn)業(yè)發(fā)展的綜合��、高效�����、先進的管理系統(tǒng)�,是以中醫(yī)藥傳承創(chuàng)新為目標、以中藥監(jiān)管科學為基礎��、以高水平科學監(jiān)管為特征的新型監(jiān)管組織體系�����。其構建策略包括3 個方面內容:①要聚焦中國特色����、中藥特點��、全球領先3 個層次進行立體布局��。②要綜合法規(guī)制度����、組織機構、科技支撐���、產(chǎn)業(yè)發(fā)展��、國際影響5 個維度進行系統(tǒng)設計���。③要圍繞全鏈條中藥監(jiān)管工作協(xié)調會商���、全方位中藥監(jiān)管科學研究者聯(lián)盟及全球化中藥監(jiān)管政策協(xié)調3 個機制進行方法創(chuàng)新。中藥卓越監(jiān)管體系建設的基礎是科學技術進步�����,要充分發(fā)揮藥品監(jiān)管科學全國重點實驗室的高水平平臺作用����,創(chuàng)新中藥監(jiān)管科學中西醫(yī)融合研究新模式,建立中藥監(jiān)管科學轉化新機制[24]����。要按照國家藥監(jiān)局《全面強化藥品監(jiān)管科學體系建設實施方案》要求,探索建立符合中藥特點的先進臨床試驗方法����、中醫(yī)動物模型、生物標志物等中藥監(jiān)管新工具����、新標準�、新方法����,開展基于真實世界證據(jù)的具有人用經(jīng)驗中藥的風險獲益評價新方法、人工智能與中藥科學監(jiān)管����、中醫(yī)治未病的監(jiān)管科學與審評決策研究。進一步完善中醫(yī)藥理論�、人用經(jīng)驗和臨床試驗相結合的中藥注冊審評證據(jù)體系�,建立人用經(jīng)驗收集與整理的方法和工具,研究符合中醫(yī)藥特點的臨床療效評價新方法��。要持續(xù)推進中藥質量控制技術研究��,完善符合中藥特點的藥學評價技術體系��,突破中藥復雜體系質量的高級表征和系統(tǒng)控制技術瓶頸�����。2024 年1 月啟動新的一批藥品監(jiān)管科學體系建設重點項目�,中藥及監(jiān)管科學共性問題主要聚焦中藥監(jiān)管科學中西醫(yī)融合研究新模式,重點發(fā)展中藥監(jiān)管學科理論與方法,組織開展中藥監(jiān)管科學體系及學科體系�、新工具新方法轉化認定程序,中藥真實世界數(shù)據(jù)����、有效性、安全性�、質量及風險獲益評價方法等研究,為建立符合中醫(yī)藥特點的中藥審評審批體系提供技術支撐���。
總之��,2024 年全國藥品監(jiān)督管理工作會議提出“加快打造具有中國特色����、符合中藥特點�、全球領先的中藥卓越監(jiān)管體系”是我國構建“科學、高效��、權威”藥品監(jiān)管體系戰(zhàn)略的重要組成部分����,是中國式現(xiàn)代化藥品監(jiān)管實踐的新要求,是統(tǒng)籌高水平安全監(jiān)管和產(chǎn)業(yè)高質量發(fā)展的新舉措�����。這是沒有先例可循、沒有經(jīng)驗可借鑒的偉大奮斗目標����,需要我們立足時代方位,大膽探索���,創(chuàng)造先例��。我們要更加準確把握黨中央對藥品監(jiān)管的新要求�����,準確把握藥品安全面臨的新挑戰(zhàn)��,準確把握醫(yī)藥創(chuàng)新呈現(xiàn)的新態(tài)勢,系統(tǒng)研判中藥行業(yè)性特征�����、階段性特點和當前監(jiān)管難點���、痛點����、卡點,強化中藥卓越監(jiān)管體系戰(zhàn)略性�、前瞻性、系統(tǒng)性設計�����,統(tǒng)籌中藥高水平安全監(jiān)管和中藥產(chǎn)業(yè)高質量發(fā)展���,為推進中藥傳承創(chuàng)新發(fā)展貢獻藥監(jiān)力量�����。
參考文獻
[1] 國家藥品監(jiān)督管理局.2024 年全國藥品監(jiān)督管理工作會議召開[EB/OL].(2024-01-10).https://www.nmpa.gov.cn/yaowen/ypjgyw/hyxx/
zhhyxx/20240110172910106.html.
[2] 楊悅. 美國藥品監(jiān)管科學研究[M]. 北京:中國醫(yī)藥科技出版社�����,2020.
[3] 國家藥品監(jiān)督管理局.《中藥注冊分類及申報資料要求》政策解讀[EB/OL].(2020-09-30)[2021-02-03].https://www.nmpa.gov.cn/xxgk/zhcjd/
zhcjdyp/20200930164259184.html.
[4] 王停, 林紅梅, 于江泳, 等. 基于新法規(guī)下的中藥創(chuàng)新藥研發(fā)策略[J]. 中國中藥雜志,2021,46(12):3150-3155.
[5] 趙軍寧. 中藥監(jiān)管科學:助力更高水平的中藥科學監(jiān)管[J]. 中國藥學雜志,2023,58(9):749-761.
[6] 趙軍寧, 王軍志, 李波���,等. 中國藥品監(jiān)管的科學化進程與監(jiān)管科學發(fā)展[J/OL]. 中國科學: 生命科學,1-18[2024-02-21].http://kns.cnki.net/
kcms/detail/11.5840.Q.20240118.1430.002.html.
[7] 趙軍寧, 黃璐琦. 中藥監(jiān)管科學: 發(fā)展中的新興融合科學[J/OL]. 中國科學基金,1-10[2024-02-21].https://doi.org/10.16262/
j.cnki.1000-8217.20240209.003.
[8] 國家藥品監(jiān)督管理局.2022 中國藥品監(jiān)督管理統(tǒng)計年鑒[M]. 北京:《中國食品藥品監(jiān)管》雜志社,2022.
[9] 國家中藥監(jiān)管藍皮書編委會.2022 國家中藥監(jiān)管藍皮書[M]. 北京:中國醫(yī)藥科技出版社��,2023.
[10] 戴瑛, 張翼冠, 曾瑾��,等. 伊尹湯液之謎——中藥復方非典型藥理效應規(guī)律發(fā)現(xiàn)與評價策略[J]. 中國中藥雜志,2022,47(16):4261-4268.
[11] 肖小河, 張定堃, 王伽伯, 等. 中藥品質綜合量化評控體系——標準評控力金字塔[J]. 中國中藥雜志,2015,40(1):7-12.
[12] 胡穎廉. 中國藥品監(jiān)管體制改革25 年回顧[J]. 中國食品藥品監(jiān)管,2023(3):4-15.
[13] 國務院新聞辦網(wǎng)站. 國務院新聞辦就“強化藥品監(jiān)管 切實保障人民群眾用藥安全”舉行發(fā)布會[EB/OL].(2023-07-05).https://www.gov.cn/
govweb/lianbo/fabu/202307/content_6890069.htm.
[14] 孟八一. 嚴厲的監(jiān)管成就強大的產(chǎn)業(yè)——FDA 藥物監(jiān)管110 年剪影( 連載一)[J]. 中國食品藥品監(jiān)管,2018(6):47-55.
[15] 孟八一. 嚴厲的監(jiān)管成就強大的產(chǎn)業(yè)——FDA 藥物監(jiān)管110 年剪影( 連載二)[J]. 中國食品藥品監(jiān)管,2018(7):50-59.
[16] 謝志潔. 論科學發(fā)展觀指導下的科學監(jiān)管理念[J]. 中國醫(yī)藥技術經(jīng)濟與管理,2007(5):84-89.
[17] 李利. 建立健全科學高效權威的藥品監(jiān)管體系[N]. 學習時報,2023-11-10(1).
[18] 國家藥品監(jiān)督管理局. 中國中藥監(jiān)管政策法規(guī)與技術指引[M]. 北京:中國醫(yī)藥科技出版社���,2023.
[19] 中華中醫(yī)藥學會.2022 年度中醫(yī)藥十大學術進展發(fā)布[EB/OL].(2023-03-01). https://www.cacm.org.cn/2023/03/01/22021/.
[20] 中華中醫(yī)藥學會.《新時代中醫(yī)藥標志性科技成果(2012-2022)》發(fā)布[EB/OL].(2023-12-07).https://www.cacm.org.cn/2023/12/07/26494/.
[21] 中國醫(yī)藥報.“2023 年度中國醫(yī)藥十大新聞”揭曉[EB/OL].(2023-12-25).http://mtest.health-china.com/c/2023-12-25/1034890.shtml.
[22] 2023 年中醫(yī)藥十大新聞[N]. 中國中醫(yī)藥報, 2024-01-22(1).
[23] 張伯禮, 陳傳宏. 中藥現(xiàn)代化二十年(1996-2015)[M]. 上海:上?����?茖W技術出版社���,2016.
[24] 趙軍寧. 培育和強化藥品監(jiān)管領域國家戰(zhàn)略科技力量[J]. 中國食品藥品監(jiān)管,2023(4):4-13.