1.什么是逆向工程
自從我國從2015年開展仿制藥一致性評價以來,對仿制藥與參比制劑的處方一致性有一定要求���。為了達(dá)到藥學(xué)、臨床效果上的一致性,需要全面了解參比制劑的屬性���,以幫助仿制藥開發(fā)����。逆向工程是指對目標(biāo)原研制劑進(jìn)行逆向分析���,從而確定原研制劑原料藥晶型�、處方���、含量及制備工藝等關(guān)鍵質(zhì)量屬性���,從而指導(dǎo)仿制藥開發(fā)����,得到質(zhì)量和療效與原研制劑一致產(chǎn)品的方法���。逆向工程的應(yīng)用有助于降低制劑開發(fā)的難度����、減少處方開發(fā)的工作量���、縮短研發(fā)的時間�,提高仿制藥研發(fā)的成功率。
使用逆向工程技術(shù)�,可以方便地確定目標(biāo)制劑產(chǎn)品的關(guān)鍵質(zhì)量屬性,如處方中活性藥物成分(API)晶型���、輔料的定量組成�、處方的制備工藝等����。逆向工程可以從文獻(xiàn)調(diào)研和物理化學(xué)方法兩個方面來進(jìn)行�。
2.原研制劑文獻(xiàn)調(diào)研
文獻(xiàn)調(diào)研主要關(guān)注的是原研制劑的處方成分、單位重量�、外觀、原料藥晶型����、包衣材料����、包裝材料、以及其臨床和藥代動力學(xué)參數(shù)����。可以通過查詢相關(guān)的專利����、專業(yè)的數(shù)據(jù)庫����、藥監(jiān)局官網(wǎng)等調(diào)研以上相關(guān)參數(shù)。進(jìn)行調(diào)研需關(guān)注的主要文件有產(chǎn)品說明書����、公開的評審信息、專利等�。這些文件一般都可以在各上市國家的藥監(jiān)局網(wǎng)站查到����,如FDA、EMA、PMDA以及俄羅斯、阿根廷���、土耳其等國家的藥監(jiān)局網(wǎng)站;專利可以在FDA Orange Book�、歐洲專利局、Google專利搜索�、中國專利局、Soopat專利等搜索查詢���。
美國FDA公開的信息�,比如說明書label和評審綜述等�,可獲得信息包括處方輔料組成�、體內(nèi)藥動學(xué)參數(shù)、溶出方法����、藥物相互作用�、代謝途徑等。歐盟EMA評審報告�,可獲得處方輔料組成�、制備工藝、質(zhì)量標(biāo)準(zhǔn)���、穩(wěn)定性數(shù)據(jù)等���。日本PMDA公布的藥品說明書中一般會提供原料藥理化性質(zhì)����,如:溶解性、引濕性����、pKa、熔點����、穩(wěn)定性等相關(guān)信息����;同時對處方輔料組成,制劑形狀和重量、制劑穩(wěn)定性、溶出方法、體內(nèi)藥動學(xué)參數(shù)等一般也有比較詳細(xì)的描述����。
NMPA關(guān)于奧拉帕利原料性質(zhì)的描述
3.物理化學(xué)方法
從查得的文獻(xiàn)中可以獲得大量的原研制劑信息,但是也有很多具體的信息�,例如處方比例、工藝參數(shù)等描述并不準(zhǔn)確����,因此需要通過物理化學(xué)的方法對參比制劑進(jìn)行分析�,以獲得更加詳細(xì)的參數(shù)���。使用逆向工程技術(shù)���,可以方便地確定原研制劑中活性藥物成分信息、處方中輔料的定量組成以及處方的制備工藝���。
3.1原料藥信息
雖然目前的法規(guī)并未要求仿制藥需與參比制劑的晶型一致,但是為了保證溶出度與穩(wěn)定性的相似,仿制藥采用的原料藥應(yīng)盡量與原研制劑原料藥一致���。除了通過文獻(xiàn)專利獲得外,在實驗中可以利用多種方式確定晶型與粒徑���。
晶型確定:可以使用X-射線粉末衍射(XRPD)����、傅里葉變換紅外光譜(FTIR)、近紅外光譜(NIR)����、拉曼光譜、差示掃描量熱法(DSC)����、熱重分析(TGA)等分析技術(shù)對原料藥的固態(tài)性質(zhì)進(jìn)行表征�。XRPD是目前鑒別晶型的最主要的方法(原料藥含量在5%以上比較有效)����。在固體混合物中,每一種晶型都產(chǎn)生相互獨立的XRPD譜���,因此混合物的XRPD譜就是各粉末衍射圖譜的累加���。如果藥物與賦形劑的相互作用結(jié)果產(chǎn)生一種新的晶型或無定型����,也會在混合物的XRPD譜中產(chǎn)生新峰或者駝峰����。通過對比原料藥���、原研制劑和自制劑在相同條件下的XRD圖譜,幫助確定原研制劑原料藥的晶型結(jié)構(gòu)���。
粒徑分布:原料藥的粒徑分布直接影響生物利用度和溶出速率,了解原研制劑的原料藥粒度分布�,有助于保證制劑的生物等效性。但是由于制劑中存在的其余輔料����,所以基于光遮蔽和激光散射的常規(guī)化技術(shù)不適用測定原料藥粒度分布���,目前唯一可行的技術(shù)就是顯微鏡技術(shù)�。例如偏振光顯微鏡���,在偏振光下�,晶體藥物呈現(xiàn)雙折射模式,而許多輔料是非晶體的����,因此不呈現(xiàn)雙折射模式,因此根據(jù)顆粒形狀和雙折射等特征來區(qū)分原料藥和輔料����,從而大概了解原料藥的粒度范圍。
3.2輔料種類與用量
在大多數(shù)情況下����,輔料的用量無法通過文獻(xiàn)獲得����,采用逆向工程對原研制劑中的關(guān)鍵輔料進(jìn)行解析從而確定大概用量���。常用的輔料含量剖析方法有元素分析法�、色譜光譜法、質(zhì)量法等����。質(zhì)量法適于定量用量較大的不溶性輔料,如微晶纖維素�、丸芯。元素分析法適用與含金屬元素的輔料,如硬脂酸鎂、磷酸氫鈣����、纖維素鈉����、硬脂富馬酸鈉、羧甲淀粉鈉等�。光譜、色譜法包括HPLC���、GC-MS����、LC-MS和UV等手段�,可以測定多種輔料,如乳糖���、蔗糖�、羥丙纖維素等可采用HPLC法測定。
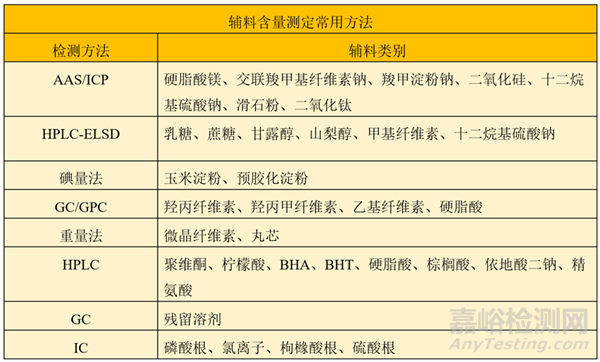
總結(jié)輔料含量測定常用方法如下:
3.3工藝
對與原研制劑的工藝�,我們可以通過多個方面進(jìn)行判斷����。①原料藥的理化特性:濕熱敏感的藥物一般不適用濕法制粒工藝,低劑量的藥物制劑一般會用使用混粉直壓�。②顯微鏡直接觀察片劑的切面,一般混粉直壓的切面要細(xì)一些���,而干法制?��;驖穹ㄖ屏5钠瑒┣忻嬉植谝恍?��,若顆粒較圓整,則采用濕法制粒的可能性較大����。③肉眼或顯微鏡觀察藥片在介質(zhì)中的崩解,混粉直壓一般產(chǎn)生單個顆粒而干法制?���;驖穹ㄖ屏9に囈话惝a(chǎn)生團(tuán)聚顆粒。④處方中輔料����,干法制粒以及濕法制粒一般需要加入粘合劑�,而一些混粉直壓處方中不含粘合劑,所以當(dāng)處方中不含粘合劑時�,很可能使用了混粉直壓工藝���。