俄羅斯對(duì)醫(yī)療器械的注冊(cè)管理實(shí)行強(qiáng)制性的監(jiān)管�,由俄羅斯衛(wèi)生部下屬俄羅斯衛(wèi)生監(jiān)督局(Roszdravnadzor,RZN)負(fù)責(zé)�。當(dāng)?shù)氐闹饕嚓P(guān)法規(guī)為Article 38 of the Health Law (Federal Law 323)等。(注:俄羅斯將于2026.1.1開(kāi)始轉(zhuǎn)換為EAEU(Eurasian Economic Union States)歐亞經(jīng)濟(jì)聯(lián)盟注冊(cè)路徑�。)
作為俄羅斯以外的生產(chǎn)廠家,您首先需要指定授權(quán)俄羅斯當(dāng)?shù)匾患夜咀鳛榇砣耍?進(jìn)而進(jìn)行醫(yī)療器械注冊(cè)申請(qǐng)�。在產(chǎn)品獲批后可以獲得當(dāng)局頒發(fā)的醫(yī)療注冊(cè)證書(shū)(長(zhǎng)期有效)和DOC(GOST R)符合性聲明證書(shū)(最長(zhǎng)3年)�。
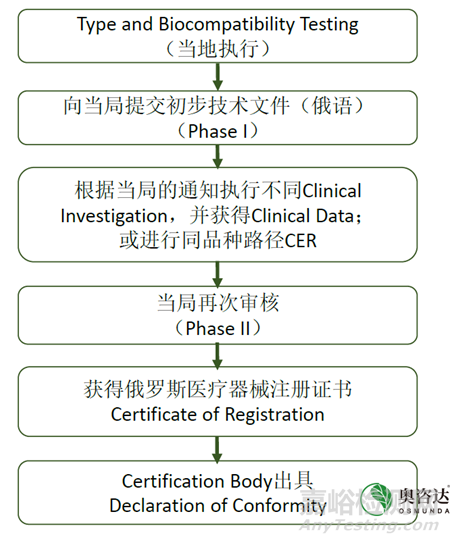
醫(yī)療器械(包括IVD產(chǎn)品)的風(fēng)險(xiǎn)等級(jí)分類(lèi)主要取決于器械的性質(zhì)和預(yù)期用途�。俄羅斯的風(fēng)險(xiǎn)等級(jí)分類(lèi)與歐盟基本類(lèi)似,由低到高依次為I, IIa, IIb和III類(lèi)�。但不論何種分類(lèi)的產(chǎn)品,俄羅斯當(dāng)局均要求在當(dāng)?shù)貓?zhí)行檢測(cè)�。在檢測(cè)之后申辦方需要向當(dāng)局提交初步的技術(shù)文件。根據(jù)當(dāng)局的初步反饋�,申辦方有可能需要執(zhí)行臨床實(shí)驗(yàn),并再次提交當(dāng)局審核�。審核通過(guò)后可以獲得注冊(cè)證書(shū)。
羅斯的醫(yī)療器械注冊(cè)大約需要半年到一年半左右�,不同風(fēng)險(xiǎn)等級(jí)的產(chǎn)品有所差異。官方注冊(cè)和當(dāng)?shù)氐谌降馁M(fèi)用總計(jì)大概是1-2萬(wàn)美元�。