美國(guó) FDA 醫(yī)療器械與放射健康中心(CDRH)主任 Jeff Shuren 于 3 月 19 日發(fā)布聲明通告有關(guān) FDA 對(duì)中國(guó)產(chǎn)塑料注射器相關(guān)質(zhì)量和性能問(wèn)題的最新評(píng)估進(jìn)展�,警告公眾除非沒(méi)有其它選擇�,否則不要使用此類注射器�。
FDA 最初于去年 11 月發(fā)布安全通訊���,內(nèi)容涉及 FDA 對(duì)某些中國(guó)產(chǎn)塑料注射器潛在器械故障的評(píng)估。FDA 此前收到了有關(guān)這些注射器的性能和安全性擔(dān)憂的信息����,包括它們單獨(dú)使用或與輸液泵等其它醫(yī)療器械一起使用時(shí)輸送正確劑量藥物的能力。
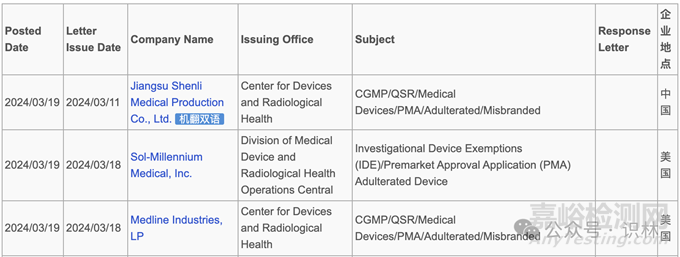
FDA 在最新的聲明中表示����,F(xiàn)DA 廣泛評(píng)估了中國(guó)產(chǎn)塑料注射器的問(wèn)題���,包括對(duì) Medline Industries 公司和 Sol-Millennium Medical 公司的設(shè)施進(jìn)行檢查,在邊境檢查和扣留產(chǎn)品���,對(duì)注射器進(jìn)行實(shí)驗(yàn)室測(cè)試,并與相關(guān)生產(chǎn)商合作確保采取適當(dāng)?shù)募m正措施���。FDA 表示,“我們正在進(jìn)行的評(píng)估已證實(shí)����,中國(guó)產(chǎn)塑料注射器的質(zhì)量問(wèn)題及其在美國(guó)的銷售比最初所知的更為普遍���。”
同時(shí),F(xiàn)DA 還公布了分別發(fā)送給中國(guó)塑料注射器生產(chǎn)商江蘇神力醫(yī)用制品有限公司���,以及在美國(guó)分銷中國(guó)產(chǎn)塑料注射器的兩家公司 Medline Industries 公司和 Sol-Millennium Medical 公司的警告信。所有三封警告信均描述了與銷售和分銷未經(jīng) FDA 批準(zhǔn)或許可在美國(guó)使用的未經(jīng)授權(quán)的中國(guó)產(chǎn)塑料注射器相關(guān)的違規(guī)行為����。FDA 在給兩家銷售商的警告信中還注意到其設(shè)施存在質(zhì)量體系違規(guī)行為����。
閱讀 FDA 發(fā)給江蘇神力的警告信發(fā)現(xiàn)�,江蘇神力通過(guò)了申請(qǐng)?zhí)枮?K103830 的 510(k) 申請(qǐng)�,獲得了 FDA 對(duì)其生產(chǎn)的 5cc 魯爾鎖活塞式注射器的許可����。但神力在美國(guó)分銷的產(chǎn)品具有顯著不同的技術(shù)特征,包括:尺寸不是 5cc 的注射器���,用魯爾接頭代替魯爾鎖頭,用于特殊藥品的注射器���,不同顏色(著色劑)和對(duì)照的注射器���。FDA 在警告信中指出���,這每一種都構(gòu)成設(shè)計(jì)的重大變更或修改���,可能會(huì)顯著改變器械的安全性或有效性���。關(guān)于對(duì)影響安全性和有效性的預(yù)期用途或設(shè)計(jì)的變更需要進(jìn)行新的上市前通知或“510(k)”的進(jìn)一步解釋。神力未能為這些注射器提交 510(k)�,從而這些產(chǎn)品被 FDA 認(rèn)定為摻雜和錯(cuò)標(biāo)。
另外���,F(xiàn)DA 在給 Medline Industries 公司的警告信中還提到了江蘇采納醫(yī)療科技公司生產(chǎn)的塑料注射器的質(zhì)量問(wèn)題和性能測(cè)試失敗的問(wèn)題�。FDA 了解到江蘇采納的幾款塑料注射器的性能測(cè)試顯示出現(xiàn)意外且無(wú)法解釋的故障。FDA 的評(píng)估正在進(jìn)行中���,F(xiàn)DA 表示將酌情采取額外措施����。
FDA 建議美國(guó)供應(yīng)商�、消費(fèi)者和醫(yī)療機(jī)構(gòu)�,在過(guò)渡到替代品之前����,除非絕對(duì)必要�,應(yīng)立即停止使用江蘇采納生產(chǎn)的塑料注射器和江蘇神力生產(chǎn)的未經(jīng)許可的塑料注射器(包括除 5mL 魯爾鎖注射器以外的所有型號(hào))。
對(duì)于中國(guó)產(chǎn)的所有其它塑料注射器����,F(xiàn)DA 建議僅根據(jù)需要繼續(xù)使用����,直至能夠過(guò)渡到替代品����,并且應(yīng)密切監(jiān)測(cè)泄漏���、破損和其它問(wèn)題�,并向 FDA 報(bào)告����。FDA 表示,警告不涉及玻璃注射器���、預(yù)充式注射器或用于口服或局部用途的注射器。FDA 補(bǔ)充指出���,可通過(guò)檢查標(biāo)簽、外包裝或聯(lián)系供應(yīng)商或集團(tuán)采購(gòu)組織來(lái)確認(rèn)注射器的生產(chǎn)地點(diǎn)�。
FDA 表示���,并不擔(dān)心該問(wèn)題會(huì)導(dǎo)致供應(yīng)鏈問(wèn)題,因?yàn)橛凶銐虻膰?guó)內(nèi)和其它國(guó)際生產(chǎn)商可以供應(yīng)塑料注射器���。