有小伙伴提出了一個很有意思的問題����,毒理試驗能進行非對稱設(shè)計嗎?恢復(fù)期組別是否可以不在所有劑量組體現(xiàn)�����?恰逢最近在整理類似主題的文章����,一并發(fā)出,供大家討論����。
非臨床研究中關(guān)于毒性反應(yīng)的可逆性評估對于指導(dǎo)臨床設(shè)計至關(guān)重要?����?赡嫘缘目疾焱ǔMㄟ^設(shè)置恢復(fù)期組動物實現(xiàn)?���;謴?fù)期組動物與主研究組同樣方案給藥,不同的是在末次給藥后動物不處死��,繼續(xù)觀察一段時間����,評估毒性反應(yīng)的可逆性,可以是部分可逆�����,也可是完全可逆�����。關(guān)于恢復(fù)期�����,ICH S6重復(fù)給藥毒性試驗部分有相關(guān)描述“試驗設(shè)計一般應(yīng)包括恢復(fù)期����,以確定藥理學(xué)/毒理學(xué)作用的可逆性或潛在惡化和/或潛在的延遲毒性效應(yīng)”。同時�����,ICH S6還指出“Recovery from pharmacological and toxicological effects with potential adverse clinical impact should be understood when they occur at clinically relevant exposures”����。這里面有個關(guān)鍵詞——臨床相關(guān)暴露量。什么叫臨床相關(guān)暴露量�����?ICH M3提示≤10倍臨床擬用劑量的暴露量��。那么如果在臨床相關(guān)暴露量下��,動物無毒性發(fā)現(xiàn)�����,或者動物毒性發(fā)現(xiàn)高于臨床相關(guān)暴露量����,是不是就不需要設(shè)置恢復(fù)期動物?或者說�����,如果需要設(shè)置恢復(fù)期,可以僅在其中1個劑量水平設(shè)置嗎����?
ICH M3 Q&A關(guān)于不需要設(shè)置恢復(fù)期的情況也列舉了幾個例子,比如已發(fā)現(xiàn)的毒性明確不可逆�����;已發(fā)現(xiàn)的毒性僅在高于臨床相關(guān)暴露量組發(fā)現(xiàn)����;已發(fā)現(xiàn)的毒性已在同類產(chǎn)品中觀察到,且明確毒性可控�����;已發(fā)現(xiàn)的毒性在短期重復(fù)給藥毒性中已經(jīng)觀察到����,且更長周期毒性試驗中未見更嚴重趨勢。ICH S9 Q&A也有類似理念描述“一般毒理學(xué)研究應(yīng)提供恢復(fù)潛力的科學(xué)評估����,至少在一個研究或一個劑量水平設(shè)置恢復(fù)期來獲得”。不難看出��,ICH對于恢復(fù)期的設(shè)置是有一定靈活性的��,允許結(jié)合具體項目進行合理設(shè)計��。
以單克隆抗體為例����,單抗因其特異性好,大部分毒性發(fā)現(xiàn)以其靶點的藥理學(xué)作用放大為主����。恢復(fù)期設(shè)置方面是否有更多的設(shè)計空間�����?但是�����,從Sewell等人統(tǒng)計的2010-2013年間53個單抗��,84項毒理學(xué)研究(有的抗體是兩個相關(guān)動物種屬)發(fā)現(xiàn)��,69項試驗設(shè)置了恢復(fù)期動物,設(shè)置的原因有兩點��,一是公司的標準實踐指南要求�����,二是預(yù)期的監(jiān)管要求����。毫無疑問,每項試驗�����,每個劑量組均設(shè)置恢復(fù)期�����,最起碼內(nèi)部無責����,外部監(jiān)管也無風險。
隨著ICH S6等指南的頒布����,以及動物“3R”原則的呼聲愈發(fā)強烈��,疊加抗體類項目的大量增加,關(guān)于恢復(fù)期的科學(xué)��、合理設(shè)計的話題值得進一步深入討論��。尤其是單抗大多需要采用非人靈長類動物進行安評����,從倫理角度和資源可及性,均應(yīng)盡可能減少動物的使用�����。Sewell等人的調(diào)研比較早期�����,不能代表工業(yè)界和監(jiān)管機構(gòu)的最新認識�����。
由NC3Rs�����、AbbVie、Bristol Myers Squibb����、GlaxoSmithKline、Genentech��、Janssen����、Merck & Co、AstraZeneca��、Sanofi-Aventis��、Roche����、Pfizer、Novartis等十幾家藥企和組織對2015-2019年啟動研究的51個單抗毒理試驗恢復(fù)期設(shè)置情況進行了統(tǒng)計分析����。共計94項研究(83項非嚙齒、11項嚙齒)在2015-2019年啟動��,24項研究(19項非嚙齒、5項嚙齒)于2015年之前啟動��。這里稍微解釋下��,有的單抗支持首次臨床試驗的毒理試驗是在2015年前完成的�����,2015-2019年開展的支持Ⅲ期臨床或BLA的更長周期毒理研究�����。51個抗體毒理研究所用種屬�����、研究周期及有無設(shè)置恢復(fù)期如下表所示����,×代表未設(shè)置恢復(fù)期����,√則相反。
51個抗體中�����,43個采用的單一種屬,且42/43采用的非嚙齒類開展的研究��,主要是食蟹猴����,有一個抗體采用的轉(zhuǎn)基因動物作為單一種屬。8個抗體采用的雙種屬開展的毒理研究����,其中4個在更長周期毒性試驗中縮減為單種屬,另外4個則依然采用的雙種屬����。
從表格中不難看出,有4個項目在IND enabling和后續(xù)更長周期毒理研究中��,均未設(shè)置恢復(fù)期(3����、18、35和40號抗體)�����。其中,3個產(chǎn)品的適應(yīng)癥為炎癥�����,1個是腫瘤�����。具體原因沒有披露��。25個抗體在短期和長期毒理研究中均設(shè)置了恢復(fù)期��。12個抗體僅在短期毒理研究中設(shè)置了恢復(fù)期��,7個抗體僅在更長周期毒理研究中設(shè)置了恢復(fù)期����。
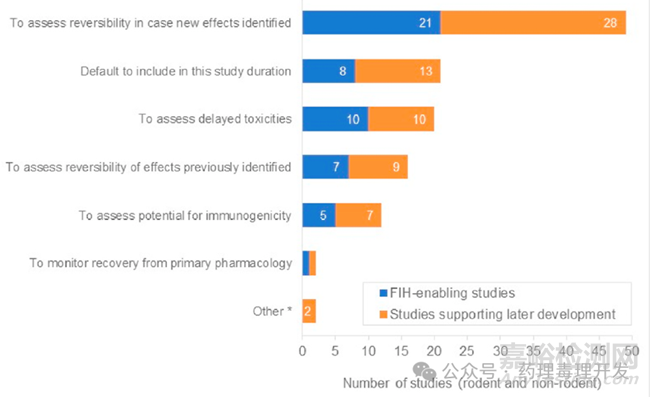
設(shè)置恢復(fù)期的主要原因如下圖所示��,反饋最多的原因是可能鑒定出的新的毒性作用的可逆性��,公司的一些默認做法以及潛在的延遲毒性評估��。但實際上ICH S6(R1)里面有明確描述��,The purpose of the non-dosing period is to examine reversibility of these effects, not to assess delayed toxicity. 評估延遲毒性并不是設(shè)置恢復(fù)期的目的。企業(yè)反饋的關(guān)于恢復(fù)期設(shè)置的原因中����,還有一條是檢測可能的免疫原性。關(guān)于這點����,ICH S6(R1)里面同樣有過描述,the addition of a recovery period just to assess potential for immunogenicity is not required. 設(shè)置恢復(fù)期對于ADA的評估并無額外價值�����。這也說明ICH的指南即使在一些大的藥企中�����,也未完全的嚴格落于實踐�����。大多還是基于避險心理�����,無論是來自公司層面的��,還是注冊層面,亦或是純粹對未發(fā)生事件的擔心等原因����,默認了恢復(fù)期的存在。
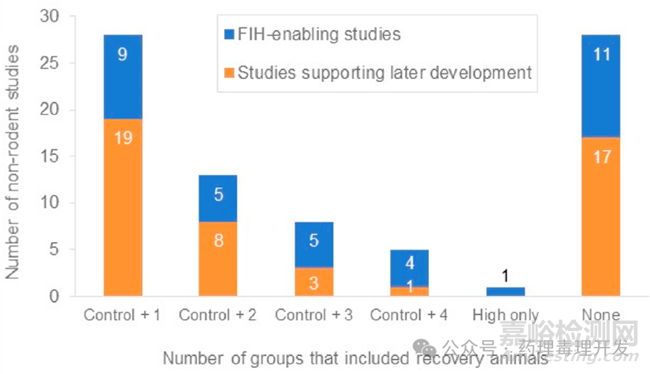
在55項非嚙齒類含恢復(fù)期的毒理研究中��,28/55個僅在對照組+1個供試品給藥組設(shè)置恢復(fù)期�����。這其中����,23/28項試驗僅設(shè)置在高劑量組。22/55項研究在所有劑量組均設(shè)置了恢復(fù)期��。4/55項研究在>1個劑量組設(shè)置了恢復(fù)期����,但并不是所有劑量組��。1/55項研究僅在高劑量組包含恢復(fù)期�����,其它給藥組及對照組均未設(shè)置。另外提一句��,9項嚙齒類動物毒理研究中�����,大部分(7/9)在所有劑量組均設(shè)置了恢復(fù)期����。
以上是國外MNC企業(yè)就2015-2019年間幾十個抗體進行的問卷式調(diào)查,未披露具體產(chǎn)品名稱�����。已上市的單抗很多����,再舉幾個有名有姓的例子。2018年8月8日����,F(xiàn)DA批準上市的CCR4抗體Poteligeo,開展了28天和26周食蟹猴單種屬重復(fù)給藥毒理研究����,在28天短期重復(fù)給藥毒理試驗中設(shè)置了3個月恢復(fù)期�����,26周試驗中未見設(shè)置�����。2020年FDA批準上市的IL-6R抗體Enspryng��,開展了4周和26周食蟹猴重復(fù)給藥毒性研究��,短期研究未設(shè)置恢復(fù)期����,長期26周的研究設(shè)置了13周的恢復(fù)期�����。2023年10月26日�����,F(xiàn)DA批準了Eli Lilly的IL23p19單抗Omvoh上市����,用于治療潰瘍性結(jié)腸炎。Omvoh非臨床研究采用食蟹猴作為相關(guān)種屬�����,開展了4周和6個月兩個給藥周期的重復(fù)給藥毒理研究����。4周重復(fù)給藥毒性試驗中設(shè)置了8周的恢復(fù)期,而6個月毒理研究中未見恢復(fù)期設(shè)置�����。不只抗體類產(chǎn)品����,CRESEMBA是FDA于2015年批準上市的艾沙康唑膠囊,用于治療侵襲性曲霉菌病和侵襲性毛霉菌病成人患者�����,在其食蟹猴13周重復(fù)給藥毒理試驗中��,設(shè)置了4周恢復(fù)期�����,但僅在陰性對照和高劑量組包含恢復(fù)期動物,且每個性別僅設(shè)置了1只動物��。在其食蟹猴39周重復(fù)給藥毒理試驗中�����,同樣設(shè)置了4周恢復(fù)期��,同樣僅在陰性對照和高劑量組包含了恢復(fù)期動物�����,每個性別設(shè)置了2只動物�����。案例很多��,不再進一步展開�����。
相較于早期的一些回顧性數(shù)據(jù)�����,恢復(fù)期的設(shè)置近些年呈減少的趨勢����。恢復(fù)期的設(shè)置與否以及怎么設(shè)置還是要回歸到科學(xué)層面進行思考�����。既不能默認所有試驗�����,所有劑量組均設(shè)置恢復(fù)期��,也不可走向另外一個極端��,否定恢復(fù)期的作用��。有很多問題值得去進一步討論�����,比如如果有兩個相關(guān)種屬��,且毒性表現(xiàn)類似,是否可以僅在其中1個種屬中設(shè)置恢復(fù)期組����?比如如果設(shè)置恢復(fù)期,能否僅在其中1組或非全部供試品給藥組設(shè)置��?比如如果可以在部分組別設(shè)置恢復(fù)期��,是在高劑量還是更接近臨床相關(guān)暴露量劑量組����?比如恢復(fù)期的時間應(yīng)該多久,預(yù)設(shè)的恢復(fù)期是否可以在試驗過程中根據(jù)供試品毒性表現(xiàn)進行動態(tài)調(diào)整?比如陰性對照組動物設(shè)置恢復(fù)期的意義是什么��,如果有充分的歷史對照數(shù)據(jù)��,是否還有必要繼續(xù)設(shè)置�����?
以上都是些很有意思的話題����。ICH S6和M3或多或少都有相關(guān)描述。也可以翻一翻已經(jīng)批準上市的單抗或者其他同類別藥物的藥理毒理研究數(shù)據(jù)����,對恢復(fù)期設(shè)置的了解也能更多一些?���;謴?fù)期的科學(xué)設(shè)置是建立在充分的預(yù)試驗及對產(chǎn)品的充分了解基礎(chǔ)之上,是一個開放的話題����,絕不是默認設(shè)置那么簡單?���;謴?fù)期設(shè)置也是一個前瞻性又稍顯“敏感”的話題,工業(yè)界的調(diào)研畢竟代表不了監(jiān)管機構(gòu)的態(tài)度��。還是秉承ICH M3和S9 Q&A中給出的一些原則����,結(jié)合充分的文獻調(diào)研和前期試驗數(shù)據(jù)�����,企業(yè)可以嘗試與監(jiān)管機構(gòu)就毒理研究方案或策略進行溝通��,以求最優(yōu)化試驗設(shè)計����。