今日頭條
普方18億美金被Genmab收購(gòu)��。Genmab公司與普方生物達(dá)成最終協(xié)議���,將以18億美元現(xiàn)金收購(gòu)后者���,獲得該公司下一代ADC產(chǎn)品組合資產(chǎn)���。2024年1月�����,普方生物開(kāi)發(fā)的靶向FRα的ADC藥物rinatabart sesutecan (Rina-S�����,PRO1184)已獲FDA授予快速通道資格���,用于治療表達(dá)葉酸受體α(FRα)的高級(jí)別漿液性或子宮內(nèi)膜樣鉑耐藥的卵巢癌患者�����。該新藥目前正處于治療卵巢癌和其他FRα表達(dá)實(shí)體瘤I/II期臨床階段��。
國(guó)內(nèi)藥訊
1.益普生「蘭瑞肽」獲批新適應(yīng)癥。益普生醋酸蘭瑞肽緩釋注射液(預(yù)充式)獲國(guó)家藥監(jiān)局批準(zhǔn)新適應(yīng)癥�����,用于治療不可切除�����、高分化或中分化���、局部晚期或轉(zhuǎn)移性胃腸胰神經(jīng)內(nèi)分泌瘤(GEP-NETs)成人患者���;以及用于類癌綜合征成人患者。在臨床研究中���,該產(chǎn)品可顯著延長(zhǎng)患者的無(wú)進(jìn)展生存期(PFS)達(dá)38.5個(gè)月�����,疾病復(fù)發(fā)風(fēng)險(xiǎn)降低53%。
2.九源基因「司美格魯肽」報(bào)產(chǎn)���。九源基因的生物類似藥司美格魯肽注射液上市申請(qǐng)獲CDE受理���,用于成人2型糖尿病患者的血糖控制。司美格魯肽是一款長(zhǎng)效GLP-1(胰高血糖素樣肽-1)受體激動(dòng)劑�����,原研產(chǎn)品由諾和諾德開(kāi)發(fā)���,商品名為諾和泰®���,已獲批用于輔助飲食和運(yùn)動(dòng)以改善2型糖尿?��。═2DM)患者的血糖控制�����。今年初,司美格魯肽片(Rybelsus�����,諾和忻)也在華獲批上市��,用于治療2型糖尿病�����。
3.君實(shí)降脂新藥新適應(yīng)癥報(bào)產(chǎn)���。君實(shí)生物PCSK9抑制劑昂戈瑞西單抗的新適應(yīng)癥上市申請(qǐng)獲CDE受理,推測(cè)申報(bào)的適應(yīng)癥為“單藥治療原發(fā)性高膽固醇血癥和混合型高脂血癥患者”��。公布在AHA2023年會(huì)上的Ⅲ期數(shù)據(jù)顯示�����,治療24周時(shí),昂戈瑞西單抗(150mg Q2W和300mg Q4W)兩隊(duì)列LDL-C較基線變化百分比與安慰劑組差異的最小二乘均值分別為-67.74%和-61.2%��;且療效維持長(zhǎng)達(dá)52周���。
4.泰它西普獲干燥綜合征快速通道資格。榮昌生物BLyS/APRIL雙靶點(diǎn)融合蛋白泰它西普獲FDA授予快速通道資格���,用于治療干燥綜合征���。該新藥通過(guò)同時(shí)抑制BLyS和APRIL兩個(gè)細(xì)胞因子的過(guò)度表達(dá)���,“雙管齊下”阻止B細(xì)胞的異常分化和成熟��,從而治療自身免疫性疾病��。此前�����,該新藥已獲批用于治療系統(tǒng)性紅斑狼瘡���;泰它西普類風(fēng)濕性關(guān)節(jié)炎適應(yīng)癥的補(bǔ)充上市申請(qǐng)也已獲得CDE受理��。
5.馴鹿CAR-T美國(guó)獲批自免病IND��。馴鹿生物自主研發(fā)的靶向BCMA的CAR-T產(chǎn)品伊基奧侖賽注射液(CT103A)獲FDA批準(zhǔn)IND申請(qǐng)��,擬開(kāi)發(fā)用于治療難治性全身型重癥肌無(wú)力(gMG)患者��。在一項(xiàng)針對(duì)復(fù)發(fā)/難治性抗體介導(dǎo)的神經(jīng)系統(tǒng)特發(fā)性炎癥性疾病的探索性研究(NCT04561557)中��,2例難治性重癥肌無(wú)力(MG)患者接受單次CT103A回輸3個(gè)月-18個(gè)月期間�����,患者M(jìn)G-ADL評(píng)分��、QMG評(píng)分、MG-QOL評(píng)分和改良Rankin評(píng)分(mRS)持續(xù)改善��。
6.恩華抑郁癥新藥獲批IND��。恩華藥業(yè)1類化藥NH103草酸鹽片獲國(guó)家藥監(jiān)局臨床試驗(yàn)?zāi)驹S可,擬開(kāi)發(fā)用于治療抑郁癥���。NH103對(duì)常用抗抑郁靶點(diǎn)5-羥色胺轉(zhuǎn)運(yùn)蛋白(SERT)和抗抑郁活性增效靶點(diǎn)5-HT2A/5-HT2C受體均有較強(qiáng)且均衡的抑制活性,可阻斷SERT將5-羥色胺(5-HT)回收至突觸前的過(guò)程�����,從而特異性地提升5-HT的濃度��。目前暫無(wú)相同機(jī)制的抗抑郁藥上市�����。
國(guó)際藥訊
1.第一三共ADC獲批不限癌種sBLA���。FDA加速批準(zhǔn)阿斯利康與第一三共開(kāi)發(fā)的HER2靶向抗體偶聯(lián)藥物(ADC)Enhertu(trastuzumab deruxtecan)的補(bǔ)充上市申請(qǐng),用于治療不可切除或轉(zhuǎn)移性HER2陽(yáng)性(免疫組化[IHC] 3+)實(shí)體瘤成年患者�����。這是首款獲批的不限癌種HER2 ADC療法�����。在DESTINY-PanTumor02中�����,Enhertu確認(rèn)客觀緩解率(ORR)達(dá)到51.4%��,中位緩解持續(xù)時(shí)間(DOR)為19.4個(gè)月�����。
2.BMS骨髓瘤CAR-T獲批擴(kuò)展使用范圍�����。百時(shí)美施貴寶與2seventy bio開(kāi)發(fā)的BCMA CAR-T療法Abecma(idecabtagene vicleucel)獲FDA批準(zhǔn)擴(kuò)大適用范圍,用于治療接受包括免疫調(diào)節(jié)劑(IMiD)��、蛋白酶體抑制劑(PI)和CD38單抗三類藥物治療后進(jìn)展的復(fù)發(fā)或難治性多發(fā)性骨髓瘤(MM)患者���。在III期KarMMa-3臨床中��,Abecma較標(biāo)準(zhǔn)治療使疾病進(jìn)展或死亡風(fēng)險(xiǎn)降低51%(mPFS:13.3個(gè)月vs4.4個(gè)月)��。此前,Abecma已獲批用于治療已接受過(guò)四線及以上治療的R/R MM患者。
3.諾華核藥Ⅲ期臨床積極���。諾華靶向放射性配體療法Pluvicto(177Lu-PSMA-617)治療去勢(shì)抵抗性前列腺癌(mCRPC)患者的Ⅲ期PSMAfore臨床達(dá)到主要終點(diǎn)和關(guān)鍵次要終點(diǎn)��。與使用改變種類的雄激素受體通路抑制劑(ARPI)治療相比���,Pluvicto治療改善患者無(wú)進(jìn)展生存期(rPFS),使疾病進(jìn)展或死亡風(fēng)險(xiǎn)降低59%(p<0.0001)��;在未經(jīng)調(diào)整的意向治療(ITT)患者中���,患者的OS風(fēng)險(xiǎn)比小于1.0�����。Pluvicto的安全性與之前研究一致。
4.默沙東肺癌聯(lián)合療法啟動(dòng)III期臨床���。默沙東宣布啟動(dòng)口服KRAS G12C抑制劑MK-1084聯(lián)合PD-1抑制劑Keytruda一線治療KRAS G12C突變且腫瘤表達(dá)PD-L1(TPS≥50%)轉(zhuǎn)移性非小細(xì)胞肺癌(NSCLC)的III期臨床試驗(yàn)。I期臨床初步結(jié)果顯示�����,MK-1084單藥治療實(shí)體瘤患者時(shí)ORR達(dá)到22%;在與Keytruda聯(lián)合治療NSCLC患者時(shí)ORR達(dá)71%�����,而在PD-L1表達(dá)(TPS≥50%)患者中ORR達(dá)到75%���。
5.Candel公司胰腺癌療法II期臨床積極�����。Candel公司溶瘤病毒療法CAN-2409聯(lián)合伐昔洛韋和化療用于交界性可切除胰腺癌的II期研究結(jié)果積極。與對(duì)照組相比�����,CAN-2409聯(lián)合治療顯著延長(zhǎng)患者中位總生存期(mOS:28.8個(gè)月vs12.5個(gè)月)���;患者兩年期生存率分別為71.4%和16.7%�����;36個(gè)月時(shí)���,接受CAN-2409并在手術(shù)前進(jìn)行放化療的患者存活率預(yù)估為47.6%,而對(duì)照組為16.7%���。此外�����,CAN-2409耐受性良好�����。
6.Macrogenics公司ADC早期臨床積極�����。Macrogenics公司靶向B7H3的抗體偶聯(lián)藥物vobramitamab duocarmazine(MGC-018)治療去勢(shì)抵抗前列腺癌的Ⅱ期臨床TAMARACK結(jié)果積極。數(shù)據(jù)顯示���,患者接受MGC-018(2.0mg/kg和2.7mg/kg)治療�����,患者前列腺特異性抗原(PSA)水平下降超過(guò)50%��;因副作用停止治療的比例分別為4.4%和2.3%��,沒(méi)有副作用致死案例出現(xiàn)��。詳細(xì)結(jié)果將在今年ASCO會(huì)議上報(bào)告���。
7.強(qiáng)生131億美元收購(gòu)Shockwave Medical。強(qiáng)生宣布與Shockwave Medical達(dá)成最終協(xié)議��,將以131億美元總交易金額收購(gòu)后者��,并獲得該公司創(chuàng)新血管內(nèi)碎石術(shù)(IVL)技術(shù)平臺(tái)以及用于緩解難治性心絞痛癥狀的Reducer System��,以擴(kuò)大強(qiáng)生醫(yī)療技術(shù)部門(mén)(Johnson & Johnson MedTech)在心血管介入治療的應(yīng)用范圍��。該交易預(yù)計(jì)將于2024年年中完成。此前���,強(qiáng)生醫(yī)療技術(shù)部門(mén)已成功收購(gòu)了心血管醫(yī)療技術(shù)巨頭Abiomed以及左心耳閉合裝置公司Laminar�����。
醫(yī)藥熱點(diǎn)
1.三部委發(fā)文支持建設(shè)三級(jí)養(yǎng)老服務(wù)網(wǎng)絡(luò)。4月2日�����,國(guó)家發(fā)改委等三部門(mén)修訂印發(fā)《“十四五”積極應(yīng)對(duì)人口老齡化工程和托育建設(shè)實(shí)施方案》,中央預(yù)算內(nèi)投資支持三級(jí)養(yǎng)老服務(wù)網(wǎng)絡(luò)中的縣級(jí)養(yǎng)老服務(wù)中心建設(shè)和縣城公辦托育服務(wù)能力建設(shè)項(xiàng)目���,并提出���,引導(dǎo)金融機(jī)構(gòu)對(duì)普惠養(yǎng)老、普惠托育企業(yè)和機(jī)構(gòu)提供金融支持���。中央預(yù)算內(nèi)投資原則上按照東、中��、西�����、東北地區(qū)分別不超過(guò)平均總投資的40%�����、60%���、80%�����、80%的比例進(jìn)行支持�����。
2.山東省首家罕見(jiàn)病?�?撇》砍闪?����。4月3日��,山東省濟(jì)寧市第一人民醫(yī)院成立濟(jì)寧市罕見(jiàn)病診療中心,并率先在全省設(shè)立成建制的罕見(jiàn)病?�?撇》?�。罕見(jiàn)病?��?撇》坑蓾?jì)寧市第一人民醫(yī)院神經(jīng)內(nèi)科主任閆中瑞牽頭,專職醫(yī)生負(fù)責(zé)常規(guī)運(yùn)行���,秉承罕見(jiàn)病多學(xué)科診療模式��,除專職醫(yī)師外���,多個(gè)臨床科室派出醫(yī)師兼職管理病房,同時(shí)還有罕見(jiàn)病多學(xué)科專家(MDT)團(tuán)隊(duì)參與MDT查房���,為罕見(jiàn)病和未診斷疾病患者提供優(yōu)質(zhì)的醫(yī)療服務(wù)���。
3.中國(guó)科大附一院離子醫(yī)學(xué)中心開(kāi)診。4月3日上午��,中國(guó)科大附一院離子醫(yī)學(xué)中心(合肥離子醫(yī)學(xué)中心)正式開(kāi)診�����,這是安徽省首家全面開(kāi)診的質(zhì)子治療中心�����,旨在為廣大腫瘤患者提供高質(zhì)量的醫(yī)療服務(wù)��。中國(guó)科大附一院離子醫(yī)學(xué)中心位于合肥市高新區(qū)長(zhǎng)寧大道與燕子河路交叉口東南角���,是安徽省���、合肥市超前布局,與中國(guó)科學(xué)院合肥物質(zhì)科學(xué)研究院合作共建的創(chuàng)新平臺(tái)項(xiàng)目��。
評(píng)審動(dòng)態(tài)
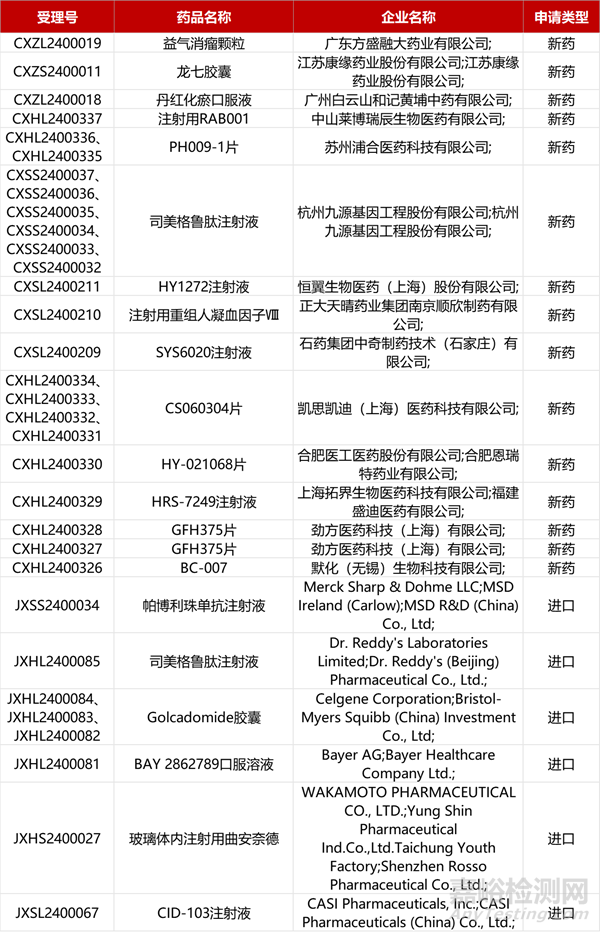
1. CDE新藥受理情況(04月07日)
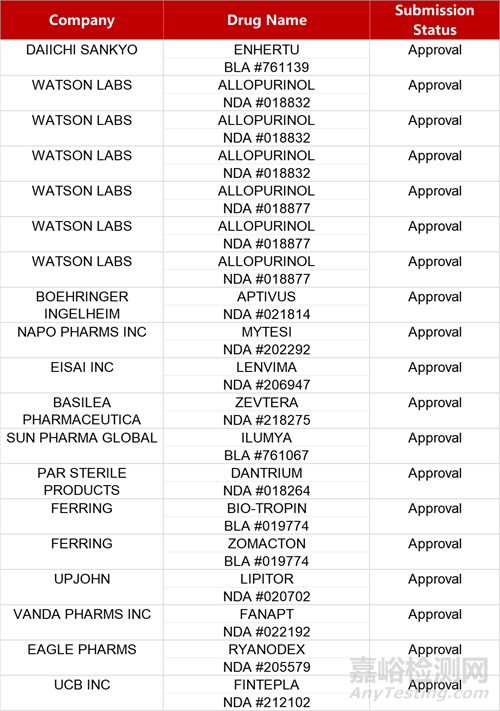
2. FDA新藥獲批情況(北美04月05日)