今日頭條
傳奇/強生CAR-T獲批新適應(yīng)癥���。傳奇生物與強生開發(fā)的BMCA CAR-T療法Carvykti(ciltacabtagene autoleucel���,cilta-cel)獲FDA批準(zhǔn)新適應(yīng)癥,用于治療既往接受過包括蛋白酶體抑制劑(PI)和免疫調(diào)節(jié)劑(IMiD)治療���、并對來那度胺耐藥的復(fù)發(fā)或難治性多發(fā)性骨髓瘤(RRMM)成人患者���。在III期CARTITUDE-4研究中,Carvyktii二線治療較標(biāo)準(zhǔn)治療顯著性改善了患者無進展生存期(HR=0.41���,p<0.0001)���。此前���,該新藥已獲批用于治療至少4種系統(tǒng)治療的RRMM患者。
國內(nèi)藥訊
1.華東醫(yī)藥引進婦科ADC獲批Ⅲ期臨床。華東醫(yī)藥旗下與ImmunoGen公司(已被艾伯維收購)開發(fā)的FRα-ADC新藥索米妥昔單抗(IMGN853���、HDM2002)獲CDE批準(zhǔn)開展國際Ⅲ期臨床���,擬聯(lián)合貝伐珠單抗用于維持治療二線含鉑化療后未出現(xiàn)疾病進展的FRα陽性復(fù)發(fā)性鉑敏感上皮性卵巢癌、輸卵管癌或原發(fā)性腹膜癌患者���。去年10月���,該新藥已在國內(nèi)報產(chǎn)���,用于治療既往接受過1-3線系統(tǒng)治療的FRα陽性的鉑類耐藥的卵巢癌患者���。
2.索元FIC抑郁癥新藥國際臨床積極���。索元生物潛在“first-in-class”三重再攝取抑制劑DB104(liafensine)治療DGM4陽性的難治性抑郁癥(TRD)的國際IIb期臨床(ENLIGHTEN)到達了主要和所有次要終點���。與安慰劑相比���,liafensine組患者蒙哥馬利-阿斯伯格抑郁量表 (MADRS)總分較基線的變化改善了4.4分(p=0.0056)���;臨床總體印象量表嚴(yán)重程度(CGI-S)和希恩殘疾量表(SDS)相對于基線的變化改善36%。此外���,liafensine耐受性良好���。
3.迪哲肺癌新藥再獲FDA突破性療法。迪哲醫(yī)藥EGFR-TKI創(chuàng)新藥舒沃哲®(舒沃替尼)獲FDA突破性療法認(rèn)定���,用于一線治療EGFR exon20ins突變���、晚期非小細(xì)胞肺癌(NSCLC)患者。Ⅰ/Ⅱ期臨床(WU-KONG1)匯總數(shù)據(jù)顯示���,研究者評估舒沃替尼一線單藥治療確認(rèn)的客觀緩解率達到78.6%���,其中300mg劑量組患者中位無進展生存期為12.4個月���。此前���,該新藥已獲FDA授予用于經(jīng)治EGFR exon20ins突變型晚期NSCLC的突破性療法認(rèn)定���。
4.恒瑞實體瘤ADC啟動Ⅰb/Ⅲ期臨床���。恒瑞醫(yī)藥Claudin-18.2抗體偶聯(lián)藥物(ADC)SHR-A1904登記啟動一項Ib/III期臨床,擬評估SHR-A1904聯(lián)合用藥治療CLDN18.2陽性晚期實體瘤的耐受性和安全性���,并確定III期研究推薦劑量���;以及在III期階段比較SHR-A1904聯(lián)合化療和免疫一線治療CLDN18.2陽性晚期實體瘤是否優(yōu)于化療聯(lián)合免疫。該項試驗由中山大學(xué)腫瘤防治中心徐瑞華博士牽頭開展���。此前���,恒瑞已將該新藥的中國大陸以外的全球權(quán)益授予默克。
5.領(lǐng)諾補體藥物澳洲獲批臨床���。領(lǐng)諾醫(yī)藥新一代補體靶向藥物SLN12140獲澳大利亞人類研究倫理委員會(HREC)批準(zhǔn)開展Ⅰ期臨床���,擬評估用于健康受試者中的安全性、耐受性及藥代動力學(xué)特性���。SLN12140是一款基于VHH-Fc的結(jié)構(gòu)形式的補體旁路路徑選擇性抑制劑���,可有效避免C5靶向分子的療效不足問題���。領(lǐng)諾醫(yī)藥也于3月底向FDA提交了SLN12140的IND申請���,并計劃在2024年二季度提交中國的IND申請。
國際藥訊
1.新型頭孢抗生素獲FDA批準(zhǔn)上市。Basilea公司新一代頭孢抗生素頭孢比羅酯Zevtera(ceftobiprole)獲FDA批準(zhǔn)上市���,用于治療金黃色葡萄球菌菌血癥(SAB)成人患者(包括右側(cè)感染性心內(nèi)膜炎患者)���;急性細(xì)菌性皮膚和皮膚結(jié)構(gòu)感染(ABSSSI)成人患者���;以及社區(qū)獲得性細(xì)菌性肺炎(CABP)的成人和兒童(3個月-18歲)患者。Zevtera可快速殺死多種革蘭氏陽性菌和革蘭氏陰性菌���。華潤三九擁有該新藥的中國權(quán)益���。
2.膽道癌雙抗向FDA滾動提交BLA。Jazz公司與Zymeworks聯(lián)合開發(fā)的HER2靶向雙抗zanidatamab已完成向FDA滾動提交生物制品許可申請(BLA)���,用于治療不可切除���、局部晚期或轉(zhuǎn)移性HER2陽性膽道癌(BTC)經(jīng)治患者。在IIb期HERIZON-BTC-01研究中���,zanidatamab二線治療的客觀緩解率(ORR)達到41.3%(95% CI:30.4���,52.8),DOR為12.9個月(95% CI:5.95, NE)���。百濟神州擁有zanidatamab在亞洲(日本除外)���、澳大利亞和新西蘭的獨家授權(quán)���。
3.優(yōu)時比抗炎抑制劑報sBLA。優(yōu)時比IL-17A/F抑制劑Bimzelx(bimekizumab)的補充生物制品許可申請(sBLA)獲FDA受理���,用于治療中重度化膿性汗腺炎(HS)成人患者。在Ⅲ期臨床(BE HEARD I和BE HEARD II)中���,Bimzelx治療16周時有56%-58%患者的膿腫和炎性結(jié)節(jié)減少至少50%���,與安慰劑相比具有臨床意義上的改善。2023年10月���,該新藥已獲得FDA批準(zhǔn)上市���,用于治療需要全身治療或光療的中重度斑塊狀銀屑病成人患者。
4.AZ奧希替尼啟動肺癌Ⅲ期臨床���。阿斯利康EGFR-TKI抑制劑Tagrisso(奧希替尼)在Clinicaltrials.gov網(wǎng)站上注冊一項Ⅲ期臨床(TROPION-Lung14)���,擬評估奧希替尼聯(lián)合或不聯(lián)合Trop2 ADC新藥Dato-DXd一線治療EGFR突變陽性非小細(xì)胞肺癌(NSCLC)的有效性與安全性。該項研究預(yù)計于2028年3月完成���。今年2月���,奧希替尼已獲FDA批準(zhǔn)新適應(yīng)癥,聯(lián)合化療一線治療攜帶EGFR突變的NSCLC患者���。
5.創(chuàng)新自免病CAR-T獲批新IND���。Caribou公司同種異體CD19靶向CAR-T療法CB-010獲FDA批準(zhǔn)開展Ⅰ期臨床(GALLOP),擬評估用于治療狼瘡性腎炎(LN)和腎外狼瘡(ERL)的安全性與初步療效���。CB-010針對B細(xì)胞表面的蛋白CD19���,并敲除了PD-1的表達,有望減少CAR-T細(xì)胞的耗竭���。在治療復(fù)發(fā)或難治性B細(xì)胞非霍奇金淋巴瘤(r/r B-NHL)的Ⅰ期ANTLER臨床中���,CB-010達到94%的總緩解率���。
6.益普生9億美元引入一款A(yù)DC。益普生與Sutro Biopharma就后者臨床前期ROR1靶向抗體偶聯(lián)藥物(ADC)STRO-003達成了全球獨家許可協(xié)議���。STRO-003已在實體瘤和血液惡性腫瘤的臨床前研究中顯示出了單藥療效和差異化安全性,有望成為“best-in-class”藥物���。根據(jù)協(xié)議���,Sutro將獲得預(yù)付款和約9000萬美元的近期付款、開發(fā)���、監(jiān)管和商業(yè)里程碑后期付款���,交易總金額高達9億美元。
醫(yī)藥熱點
1.安徽將新建一家醫(yī)院���。安徽省馬鞍山市人民政府近日發(fā)布���,馬鞍山市公共資源交易中心已發(fā)布馬鞍山十七冶醫(yī)院陽湖新院區(qū)(一期)工程設(shè)計服務(wù)項目招標(biāo)計劃���。該項目位于馬鞍山市雨山區(qū)陽湖片區(qū)東側(cè),按照三級甲等綜合醫(yī)院標(biāo)準(zhǔn)進行建設(shè)���,總建筑面積46000㎡���,其中門診住院綜合樓38500㎡(配建300床)。計劃招標(biāo)時間為2024年5月���。
2.北大醫(yī)院住院收費電子票據(jù)上線���。為全面落實財政部、國家衛(wèi)健委���、國家醫(yī)保局聯(lián)合下發(fā)的《關(guān)于全面推行醫(yī)療收費電子票據(jù)管理改革的通知》文件要求���,推進醫(yī)療收費電子票據(jù)改革���,近日北京大學(xué)第一醫(yī)院住院收費電子票據(jù)正式上線?��;颊呖梢酝ㄟ^北大醫(yī)院微信服務(wù)號���、支付寶生活號或掃描醫(yī)院取票專用二維碼,自助獲取電子票據(jù)���。醫(yī)療收費電子票據(jù)由財政部門統(tǒng)一監(jiān)督���,與紙質(zhì)票據(jù)具有同等法律效力,可作為報銷原始憑證���。
3.美國CDC對感染高致病性禽流感發(fā)布警報。美國疾控中心當(dāng)?shù)貢r間4月5日在其“健康警報網(wǎng)絡(luò)”發(fā)布消息���,介紹其本月1日報告的一例人感染高致病性禽流感病毒病例的最新情況���。這名感染者是得克薩斯州一家商業(yè)奶牛場的一名農(nóng)場工人,此人在與疑似感染病毒的奶牛接觸后被感染。這名感染者除結(jié)膜炎外無其他癥狀���,已被建議隔離并接受抗病毒藥物治療���。目前尚未發(fā)現(xiàn)H5N1病毒從奶牛或禽類傳播給人的其他病例���,也沒有發(fā)現(xiàn)H5N1病毒的人際傳播���。
評審動態(tài)
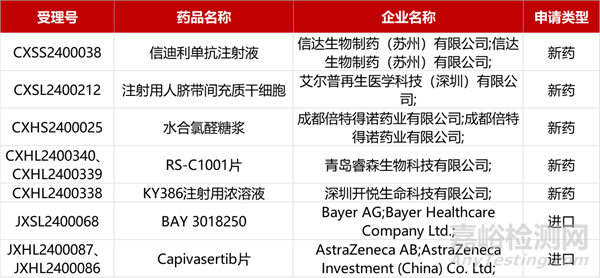
1. CDE新藥受理情況(04月08日)
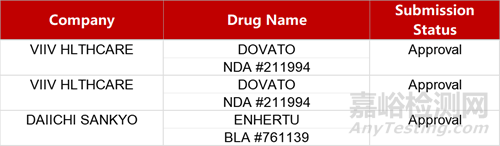
2. FDA新藥獲批情況(北美04月05日)