中藥在兒科領(lǐng)域臨床中應(yīng)用廣泛�����,但兒童群體可用的中成藥相對較少�����。2019年頒布的《中華人民共和國藥品管理法》明確�����,國家鼓勵運用現(xiàn)代科學(xué)技術(shù)和傳統(tǒng)中藥研究方法進(jìn)行中藥開發(fā)��,同時鼓勵兒童用藥品的研制和創(chuàng)新��。
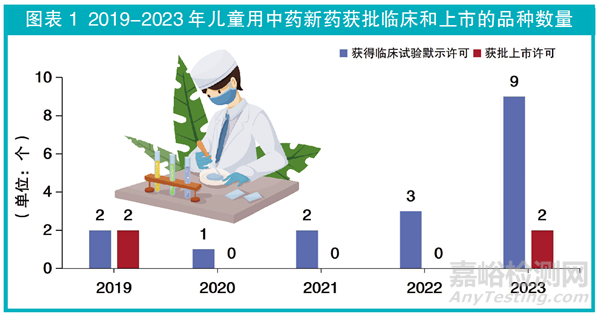
近5年來,我國兒童用中藥新藥研發(fā)取得了一定進(jìn)展����,雖然兒童用中藥新藥獲批上市許可和獲得臨床試驗?zāi)驹S可的數(shù)量總體較少(詳見圖表1),但獲得臨床試驗?zāi)驹S可的數(shù)量逐年增加��。
1����、新藥研發(fā)周期較長
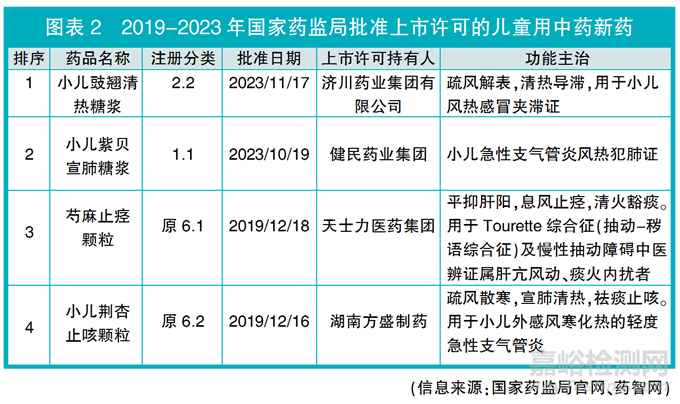
2019-2023年,國家藥監(jiān)局批準(zhǔn)上市許可的33個中藥新藥(含中藥1-3類�����,原中藥1-8類)品種中��,僅4個品種明確可用于兒童群體(詳見圖表2)�����,占總數(shù)的12.1%(4個/33個)����,包括中藥創(chuàng)新藥3個����,中藥改良型新藥1個����。
獲批上市許可的4個兒童用中藥新藥適應(yīng)癥領(lǐng)域����,除芍麻止痙顆粒為精神神經(jīng)藥品外,其他3個適應(yīng)癥領(lǐng)域為呼吸類��,其中小兒紫貝宣肺糖漿�����、小兒荊杏止咳顆粒2個品種的功能主治中��,均明確用于小兒急性支氣管炎����。急性氣管炎/支氣管炎屬于中醫(yī)學(xué)“咳嗽”范疇,當(dāng)前指南推薦的藥物治療以對癥治療為主��,是中醫(yī)藥治療的優(yōu)勢病種����。
獲批上市許可的4個兒童用中藥新藥中有3個中藥創(chuàng)新藥��,據(jù)國家藥品監(jiān)督管理局藥品審評中心(CDE)公開的申請上市技術(shù)審評報告����,這3個中藥創(chuàng)新藥均為中藥復(fù)方制劑�����,來源于臨床經(jīng)驗方�����,研發(fā)周期長�����,獲批進(jìn)行臨床試驗至獲批上市許可時間逾十年����,且在申請新藥上市許可前均完成了隨機(jī)、雙盲��、平行對照��、多中心的Ⅱ期和Ⅲ期臨床試驗��。
2����、適應(yīng)癥領(lǐng)域集中
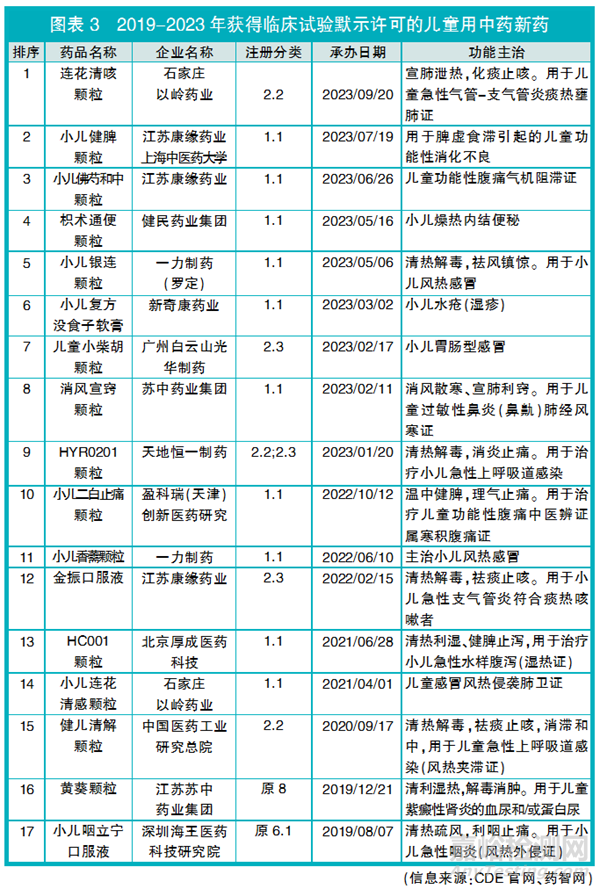
據(jù)CDE公開信息,按照“兒童”“小兒”等關(guān)鍵詞檢索藥品名稱以及獲得臨床試驗?zāi)驹S可時公開的功能主治����,2019-2023年共有17個兒童用中藥新藥品種獲得臨床試驗?zāi)驹S可(詳見圖表3),含11個中藥創(chuàng)新藥和6個中藥改良型新藥(改變劑型3個��、增加功能主治2個�����、既改變劑型又增加功能主治1個)����。
筆者查詢相關(guān)公司新聞報道發(fā)現(xiàn),7個兒童用中藥創(chuàng)新藥品種(小兒健脾顆粒����、小兒佛芍和中顆粒、枳術(shù)通便顆粒�����、消風(fēng)宣竅顆粒、小兒二白止痛顆粒��、HC001顆粒��、小兒咽立寧口服液)來自臨床經(jīng)驗方�����。
在獲得臨床試驗?zāi)驹S可的17個兒童用中藥新藥品種中����,8個品種(小兒連花清感顆粒、HC001顆粒��、小兒香薷顆粒��、消風(fēng)宣竅顆粒����、HYR0201顆粒、金振口服液��、健兒清解顆粒����、黃葵顆粒)已在CDE藥物臨床試驗登記與信息公示平臺進(jìn)行了臨床試驗登記��,其中進(jìn)展最快的是石家莊以嶺藥業(yè)的小兒連花清感顆粒��,正在進(jìn)行Ⅲ期臨床試驗。
獲得臨床試驗?zāi)驹S可的兒童用中藥新藥劑型以顆粒劑為主�����,占82.4%(14個/17個)����;適應(yīng)癥領(lǐng)域分布集中,呼吸和消化2個領(lǐng)域的藥物占主流����,占比為88.2%(15個/17個)。
3�����、研發(fā)指導(dǎo)原則發(fā)布
兒童可用的中藥品種數(shù)量占比較少��,天津中醫(yī)藥大學(xué)附屬第一醫(yī)院的研究人員以“寶”“歲”“兒”等為檢索詞�����,在“藥品名稱”“功能主治”“用法與用量”“限定”字段進(jìn)行檢索后發(fā)現(xiàn),《中國藥典》(2020年版及第一增補本)中收載的兒童用中藥成方制劑和單味制劑僅占總量的15.4%(248種/1615種)����、《國家基本藥物目錄》(2018年版)中兒童用中成藥僅占總量的12.6%(59種/268種)。
總體來看����,2019-2023年獲批上市許可和獲得臨床試驗?zāi)驹S可的兒童用中藥新藥品種數(shù)同樣較少,分別占中藥新藥總數(shù)的12.1%(4個/33個)和9.7%(17個/174個)�����。
兒童用中藥新藥的研發(fā)多源于臨床經(jīng)驗方��,劑型的選擇以兒童生理特征����、方便調(diào)整用量為原則,顆粒劑為主����,也有口服溶液劑、糖漿劑和軟膏劑��。且這類藥品的注冊申請易于納入優(yōu)先審評審批程序(符合兒童生理特征的兒童用藥品新品種、劑型和規(guī)格)��。
為進(jìn)一步完善“中醫(yī)藥理論����、人用經(jīng)驗和臨床試驗相結(jié)合的中藥注冊審評證據(jù)體系”,充分發(fā)揮中醫(yī)藥在兒童疾病方面的優(yōu)勢作用��,鼓勵兒童用中藥研發(fā)����,2月29日�����,CDE發(fā)布了第一個針對兒童群體的中藥新藥研發(fā)指導(dǎo)原則《小兒便秘中藥新藥臨床研發(fā)技術(shù)指導(dǎo)原則(試行)》�����。相信隨著CDE針對兒童群體的中藥新藥研發(fā)指導(dǎo)原則陸續(xù)發(fā)布��,企業(yè)將更積極�����、科學(xué)、規(guī)范地開展兒童用中藥新藥的研發(fā)�����。
“三結(jié)合”降低研發(fā)成本
3月1日��,在征求意見稿發(fā)布時隔4個多月后��,國家藥監(jiān)局藥審中心正式發(fā)布《小兒便秘中藥新藥臨床研發(fā)技術(shù)指導(dǎo)原則(試行)》(以下簡稱《指導(dǎo)原則》試行稿)����。
《指導(dǎo)原則》試行稿系統(tǒng)闡述了小兒便秘的中醫(yī)藥理論特點,提出了人用經(jīng)驗收集整理需重點關(guān)注的內(nèi)容����,明確了中藥新藥可能的臨床定位,強(qiáng)調(diào)了中醫(yī)藥理論和人用經(jīng)驗對小兒便秘中藥新藥研發(fā)的支持作用�����,并對臨床研發(fā)總體考慮����、臨床試驗設(shè)計和評價需關(guān)注的問題等提出了相關(guān)建議。
可操作性增強(qiáng)
《指導(dǎo)原則》試行稿與征求意見稿的內(nèi)容基本一致��,僅對征求意見稿的部分內(nèi)容描述進(jìn)行刪除、新增或順序調(diào)整����,使全文用詞更精準(zhǔn)、更簡潔��、更通順����,可操作性更強(qiáng)。如《指導(dǎo)原則》試行稿新增了兩處臨床評價新工具��,概述部分新增“觀察者/監(jiān)護(hù)者報告結(jié)局”作為臨床報告結(jié)局指標(biāo)����;次要療效指標(biāo)對于疼痛的評價部分新增“視覺模擬量表(VAS)評分�����、數(shù)字評定量表(NRS)評分”��。對于目標(biāo)人群描述部分則刪除了“原則上��,應(yīng)當(dāng)先在較大年齡段兒童中獲得初步的有效性和安全性信息后��,再開展較小年齡段人群的臨床研究。”
驅(qū)動研發(fā)創(chuàng)新
長期以來����,我國兒科中藥研發(fā)較為滯后,適宜品種����、劑型、規(guī)格開發(fā)相對不足��。隨著國家陸續(xù)出臺多項利好政策�����,合力驅(qū)動兒科藥創(chuàng)新研發(fā)成為趨勢�����。
2020-2023年����,我國兒童用中藥新藥分別有2個藥獲批上市及15個藥獲批臨床試驗?zāi)驹S可,上市創(chuàng)新藥涉及健民集團(tuán)1.1類中藥創(chuàng)新藥小兒紫貝宣肺糖漿及濟(jì)川藥業(yè)2類中藥改良型新藥小兒豉翹清熱糖漿�����。從兒科用藥劑型來看,目前在研的兒科中藥新藥以顆粒劑����、口服液、合劑等適宜兒童的劑型為主�����,適應(yīng)癥以感冒��、支氣管炎�����、腹瀉等兒科常見病居多����,缺乏兒童罕見病�����、危重癥��、早產(chǎn)兒或新生兒疾病治療的專用中藥�����。
機(jī)遇挑戰(zhàn)并存
近10年,為了鼓勵國內(nèi)藥企加大對兒科中藥的研發(fā)和生產(chǎn)�����,相關(guān)部門陸續(xù)出臺系列指導(dǎo)原則��、鼓勵研發(fā)藥品清單�����、優(yōu)先評審等相關(guān)政策�����,為中藥企業(yè)帶來了新的研發(fā)機(jī)遇��。特別是“三結(jié)合”審評證據(jù)體系的構(gòu)建����,對于傳統(tǒng)中藥給藥途徑和工藝的新藥,符合中醫(yī)藥理論��、具有人用經(jīng)驗支持的中藥復(fù)方制劑��,可鼓勵使用人用經(jīng)驗數(shù)據(jù)、真實世界研究用于兒童藥研發(fā)��,并作為支持注冊的證據(jù)之一����,以減少不必要的兒童人群臨床試驗,有效降低兒童藥品的研發(fā)成本�����,提高研發(fā)效率����,提高藥品生產(chǎn)企業(yè)或相應(yīng)機(jī)構(gòu)的研發(fā)積極性。
然而����,與化藥相比,從事中藥新藥研發(fā)的團(tuán)隊比較少�����,限制了中藥在兒童用藥領(lǐng)域的創(chuàng)新與發(fā)展��。同時����,受兒童體質(zhì)和疾病與成人差異較大、倫理和臨床試驗有難度��、研發(fā)周期長��、投入成本多�����、上市風(fēng)險高����、收益不成正比等因素影響,企業(yè)在兒科用藥研發(fā)方面的動力稍嫌不足����。
研發(fā)有的放矢
米內(nèi)網(wǎng)數(shù)據(jù)顯示,2023年上半年����,在中國城市公立醫(yī)院、縣級公立醫(yī)院����、城市社區(qū)中心及鄉(xiāng)鎮(zhèn)衛(wèi)生院終端��,中藥兒科用藥銷售額超過52億元�����,增長率達(dá)10.36%����,中國城市實體藥店終端兒科中成藥銷售額同比漲幅15.12%�����,市場潛力持續(xù)爆發(fā)����。企業(yè)研發(fā)兒科中藥不妨從以下三個方向著手:
一是,篩選中醫(yī)藥優(yōu)勢病種����,開發(fā)適合兒科用中藥。
可考慮以古代經(jīng)典名方����、名老中醫(yī)經(jīng)驗方為基礎(chǔ),將中醫(yī)辨證與現(xiàn)代中醫(yī)辨病相結(jié)合,以期研發(fā)出療效好��、不良反應(yīng)少��、服用方便����、價格經(jīng)濟(jì)的兒科治療用藥��。
二是�����,開展兒童用藥臨床試驗�����,完善兒童用藥劑量����。
可通過注冊申請等方式開展規(guī)范的兒童用藥臨床試驗,獲取兒童的人用經(jīng)驗或探索真實世界研究數(shù)據(jù)�����,明確具體的兒童用法用量和療程,通過變更劑型����、規(guī)格等方式,研發(fā)適宜不同年齡段兒童使用的劑型��、規(guī)格�����,尤其是適合低齡兒童的劑型�����,如口服液����、滴劑等,將成人��、兒童共用藥擴(kuò)展至兒童用藥��。
三是��,重視市場需求調(diào)研����,專研兒科專用中藥�����。
基于兒科疾病用藥的需求迫切性����,在充分考慮兒科人群病癥的流行率����、待治療疾?�。ɑ蜃C候)的嚴(yán)重性�����、替代藥物是否缺乏����、臨床是否急需等情況的基礎(chǔ)上,精準(zhǔn)對標(biāo)具體的治療需求�����,優(yōu)選合理的方藥、劑型開展兒童罕見病等研究��,使兒科專用中藥的研發(fā)有的放矢�����。(作者:劉炳新)