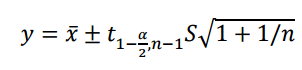一����、前言
分析方法學(xué)驗(yàn)證是一個(gè)常被提及的話題��,每一個(gè)做質(zhì)量研究的小伙伴都不陌生�。分析方法學(xué)驗(yàn)證的難點(diǎn)不在做驗(yàn)證的過(guò)程�,因?yàn)槠浔举|(zhì)也就是做實(shí)驗(yàn)�,亦不在制定“模式化”的可接受標(biāo)準(zhǔn)����,畢竟法規(guī)中有些指標(biāo)是明明白白寫在那的,會(huì)看各國(guó)藥典、ICH Q2和GMP��,就會(huì)制定“模式化”的可接受標(biāo)準(zhǔn),其難點(diǎn)之一在于基于法規(guī)層面上的“變化”,如何做到“萬(wàn)變不離其宗”����,制定科學(xué)合理的“個(gè)性化”可接受標(biāo)準(zhǔn)且又不違背法規(guī)的底層邏輯�。其難點(diǎn)之二在于如何攻克法規(guī)中描述的“不知其所以然”的條例,充分發(fā)揮法規(guī)的指導(dǎo)價(jià)值��。
分析方法學(xué)驗(yàn)證常見��,但完全參透也是路漫漫其修遠(yuǎn)兮�,筆者也在求索的路上����。此文僅圍繞“準(zhǔn)確度如何推導(dǎo)”這一主題展開�,旨在與大家分享一些見解��,也歡迎大家一同探討。
二、“準(zhǔn)確度可推導(dǎo)”的法規(guī)背景
中國(guó)藥典2020版和ICH Q2(R1)中指出:準(zhǔn)確度可以在精密度��、線性和專屬性建立后推論而得��。
上述條例表明:準(zhǔn)確度可以通過(guò)推導(dǎo)而非僅能通過(guò)準(zhǔn)確度實(shí)驗(yàn)獲得����,且這一措施符合國(guó)際和國(guó)內(nèi)的監(jiān)管要求。因此��,如若能夠正確運(yùn)用這一法規(guī)�,方法學(xué)驗(yàn)證階段可以少做一組實(shí)驗(yàn),減少實(shí)驗(yàn)量��;方法開發(fā)階段可以通過(guò)部分實(shí)驗(yàn)數(shù)據(jù)提前預(yù)估方法的準(zhǔn)確度,屬實(shí)為質(zhì)量研究工作者的福音�。
三�、“準(zhǔn)確度可推導(dǎo)”的數(shù)學(xué)背景
中國(guó)藥典9101中這樣指出:分析方法驗(yàn)證的目的是證明建立的方法適合相應(yīng)檢測(cè)要求����。那么����,為何一次驗(yàn)證通過(guò)�,就能夠表明此分析方法是適用的?不考慮意外因素時(shí)(如斷電����、色譜柱柱效下降�、儀器漏液等)是否一定不會(huì)出現(xiàn)結(jié)果超預(yù)期?
實(shí)質(zhì)上,分析方法學(xué)驗(yàn)證就是在做“統(tǒng)計(jì)推斷”��,也就是說(shuō)��,分析方法學(xué)驗(yàn)證的數(shù)據(jù)是一組統(tǒng)計(jì)樣本,而“建立的方法適合相應(yīng)檢測(cè)要求”是通過(guò)這組樣本推斷而得的結(jié)論��。有統(tǒng)計(jì)推斷的地方就有誤差����,有誤差的地方就有風(fēng)險(xiǎn)�,這也是為什么在中國(guó)藥典9101和ICH Q2(R1)中要求數(shù)據(jù)報(bào)告時(shí)應(yīng)報(bào)告置信區(qū)間,畢竟方法學(xué)驗(yàn)證的測(cè)量結(jié)果僅僅為本次實(shí)驗(yàn)的測(cè)得值��,而測(cè)得值的置信區(qū)間為一定置信水平下的推斷值,可預(yù)估分析方法的整體風(fēng)險(xiǎn)����。
綜上:分析方法學(xué)驗(yàn)證就是通過(guò)小樣本(方法驗(yàn)證數(shù)據(jù))推斷整體(分析檢測(cè))的統(tǒng)計(jì)科學(xué)。因此����,準(zhǔn)確度作為分析方法學(xué)驗(yàn)證的關(guān)鍵指標(biāo)之一����,可通過(guò)其他驗(yàn)證指標(biāo)統(tǒng)計(jì)推導(dǎo)亦不足為奇��。
四��、“推導(dǎo)準(zhǔn)確度”的適用場(chǎng)景
準(zhǔn)確度推導(dǎo)的前提是分析方法的專屬性、線性和精密度得到論證����。其結(jié)果可通過(guò)精密度推導(dǎo)而得��,需要關(guān)注的是����,并非所有的準(zhǔn)確度推算均被視為可接受的�。將準(zhǔn)確度分為含量測(cè)定準(zhǔn)確度和有關(guān)物質(zhì)測(cè)定準(zhǔn)確度2類分別考慮:
當(dāng)分析人員評(píng)估含量準(zhǔn)確度時(shí)����,隨機(jī)誤差的相對(duì)貢獻(xiàn)程度遠(yuǎn)低于由干擾引起的誤差��,此時(shí)誤差通??梢酝ㄟ^(guò)“良好的專屬性”得到控制【4】��。
與含量測(cè)定準(zhǔn)確度有顯著區(qū)別的是����,有關(guān)物質(zhì)測(cè)定的雜質(zhì)通常含量較低�,因此雜質(zhì)濃度大概率較低�,隨機(jī)誤差的相對(duì)貢獻(xiàn)變得更大��,導(dǎo)致其變異性水平比含量測(cè)定高得多,風(fēng)險(xiǎn)控制相對(duì)困難【4】。
綜上:含量測(cè)定測(cè)定的準(zhǔn)確度可以通過(guò)推導(dǎo)而得,但有關(guān)物質(zhì)測(cè)定的準(zhǔn)確度應(yīng)采用實(shí)際的加標(biāo)回收試驗(yàn)或與成熟的方法測(cè)定結(jié)果比較來(lái)證實(shí),并不能用推算結(jié)果替代����。
感興趣的小伙伴也可以仔細(xì)研讀ICH Q2(R1)準(zhǔn)確度的相關(guān)內(nèi)容,僅含量測(cè)定項(xiàng)下的準(zhǔn)確度描述了“可推導(dǎo)”的相關(guān)語(yǔ)句����,但有關(guān)物質(zhì)測(cè)定項(xiàng)下的準(zhǔn)確度并未說(shuō)明 “可推導(dǎo)”����。
五��、“推導(dǎo)含量準(zhǔn)確度”的步驟:
● Step1(獲取精密度結(jié)果):取同一濃度(分析方法擬定的樣品測(cè)定濃度��,相當(dāng)于100%濃度水平)的供試品,用至少6份的測(cè)定結(jié)果進(jìn)行評(píng)價(jià)�,結(jié)果采用相對(duì)標(biāo)準(zhǔn)偏差RSD表示【4】。
● Step2(推算準(zhǔn)確度):具體公式參見如下【3,4】:

上式中:
t(q,df):返回q處的累積分布函數(shù)�;
df:自由度��,n-1;
Upper和Lower:分別表示準(zhǔn)確度可接受標(biāo)準(zhǔn)的上限和下限值;
Mean:重復(fù)測(cè)定的樣本的均值�;
SD:標(biāo)準(zhǔn)差,可由RSD* Mean得到�;
n:樣本數(shù)量��;
筆者解析:上述公式通過(guò)精密度結(jié)果推算準(zhǔn)確度在一定可接受標(biāo)準(zhǔn)下的置信度,以確定置信度是否在可接受的標(biāo)準(zhǔn)內(nèi)����,通常以0.95為可接受標(biāo)準(zhǔn),即95%的置信水平����。這個(gè)公式也可以做變形轉(zhuǎn)化��,反過(guò)來(lái)計(jì)算95%置信水平下的準(zhǔn)確度的置信區(qū)間����,這時(shí)的可接受標(biāo)準(zhǔn)就是通常所見的 Lower~Upper。變換后公式如下:
筆者在這里特別說(shuō)明,以上變換公式來(lái)源于國(guó)家藥典委員會(huì)2024年03月最新公示的《分析數(shù)據(jù)的解釋與處理指導(dǎo)原則公示稿(第一次)》��,這也是中國(guó)藥典首次將分析數(shù)據(jù)的處理納入指導(dǎo)原則��,旨在用可靠的檢測(cè)數(shù)據(jù)及統(tǒng)計(jì)學(xué)分析方法對(duì)分析數(shù)據(jù)進(jìn)行處理�、解釋和科學(xué)呈現(xiàn)。感興趣的小伙伴可以去官網(wǎng)上下載閱讀��,內(nèi)容頗豐��。
六�、“推導(dǎo)準(zhǔn)確度”的現(xiàn)實(shí)應(yīng)用情況:
雖然“準(zhǔn)確度可推導(dǎo)”的概念早在20多年前就已經(jīng)提出,但至今并未在國(guó)內(nèi)大規(guī)模流行����,其原因之一是制藥行業(yè)內(nèi)大部分工作者的統(tǒng)計(jì)學(xué)知識(shí)略有欠缺�,原因之二是存在“推導(dǎo)準(zhǔn)確度”會(huì)不會(huì)被發(fā)補(bǔ)的疑惑�。
此次藥典委員會(huì)公示的《分析數(shù)據(jù)的解釋與處理指導(dǎo)原則公示稿(第一次)》�,讓筆者充分感受到了國(guó)內(nèi)數(shù)據(jù)分析水平的突越����,以及國(guó)家對(duì)統(tǒng)計(jì)學(xué)數(shù)據(jù)分析的重視��,相信未來(lái)會(huì)有更多的企業(yè)能夠真正的將“推導(dǎo)準(zhǔn)確度”實(shí)行����。
參考文獻(xiàn):
【1】中國(guó)藥典2020年版
【2】ICH Q2(R1)
【3】Method Validation in Pharmaceutical Analysis
【4】USP <1200>: Requirements for Compendial Validation