今日頭條
康泰脊髓灰質(zhì)炎疫苗報產(chǎn)。康泰生物旗下民海生物研發(fā)的Sabin株脊髓灰質(zhì)炎滅活疫苗(Vero細(xì)胞)上市申請獲NMPA受理,用于預(yù)防由脊髓灰質(zhì)炎1型���、2型和3型病毒感染導(dǎo)致的脊髓灰質(zhì)炎���。與傳統(tǒng)的脊髓灰質(zhì)炎滅活疫苗和脊髓灰質(zhì)炎減毒活疫苗相比�,Sabin株脊髓灰質(zhì)炎滅活疫苗(Vero細(xì)胞)結(jié)合了這兩種傳統(tǒng)疫苗安全的優(yōu)勢�,可用于預(yù)防脊髓灰質(zhì)炎病毒所引起的急性傳染病�。
國內(nèi)藥訊
1.BMS促紅劑中國報sNDA���。百時美施貴寶血紅細(xì)胞成熟劑羅特西普(Reblozyl)新適應(yīng)癥上市申請獲CDE受理�,推測適應(yīng)癥為“骨髓增生異常綜合征(MDS)”���。公布在ASCO2023年會上的III期COMMANDS研究數(shù)據(jù)顯示�,與重組人促紅素組相比�����,Reblozyl治療組24周時患者實(shí)現(xiàn)擺脫紅細(xì)胞輸注12周(RBC-TI)且平均血紅蛋白(Hb)水平增加≥1.5g/dL的比例更高(58.5%vs31.2%���,p<0.0001)�。此前�,該新藥已獲CDE批準(zhǔn)用于治療β-地中海貧血患者�����。
2.石藥EGFR單抗啟動III期臨床。石藥集團(tuán)EGFR單抗becotatug(JMT101)登記啟動一項(xiàng)III期臨床,擬評估JMT101聯(lián)合奧希替尼對比順鉑聯(lián)合培美曲塞一線治療攜帶EGFR 20號外顯子插入突變晚期非小細(xì)胞肺癌(NSCLC)的療效和安全性。該項(xiàng)研究由中山大學(xué)腫瘤防治中心張力博士牽頭開展�����。在II期BECOME研究中,在ITT人群中�����,IRC評估的JMT101聯(lián)合奧希替尼確認(rèn)的客觀緩解率(cORR)為50.0%�,疾病控制率(DCR)為79.5%。
3.康方濕疹單抗啟動Ⅲ期臨床�����。康方生物IL4-Rα單抗AK120注射液登記啟動一項(xiàng)Ⅲ期臨床���,擬評估治療中重度特應(yīng)性皮炎(AD)患者的有效性與安全性。AK120可通過與IL-4Rα特異性結(jié)合以阻斷IL-4與IL-13介導(dǎo)的信號通路,抑制相關(guān)免疫炎癥反應(yīng)的發(fā)生與發(fā)展�。在Ⅰ期臨床中,AK120治療后濕疹面積和嚴(yán)重程度指數(shù)(EASI)評分明顯改善,患者整體評分(IGA)0或1和降低≥2的比例增加���。
4.諾誠健華BTK抑制劑啟動III期臨床���。諾誠健華BTK抑制劑奧布替尼在ClinicalTrials.gov上登記注冊一項(xiàng)III期臨床(NCT06363994)�,擬評估奧布替尼聯(lián)合苯達(dá)莫司汀+利妥昔單抗對比苯達(dá)莫司汀+利妥昔單抗用于未經(jīng)治療的套細(xì)胞淋巴瘤(MCL)患者的療效與安全性。去年5月�����,該新藥在Blood子刊上發(fā)表了治療R/R MCL的長期療效數(shù)據(jù):中位隨訪為23.8個月時���,奧布替尼經(jīng)IRC評估的總緩解率(ORR)達(dá)到81.1%,其中完全緩解(CR)率為27.4%�。
5.同源康抗耐藥腫瘤藥獲批臨床。同源康醫(yī)藥新型小分子YAP/TEAD抑制劑TYK-01054獲FDA批準(zhǔn)開展新藥研究���。YAP�、TAZ和TEAD是Hippo通路的下游效應(yīng)子;YAP/TAZ/TEAD信號傳導(dǎo)的失調(diào),可能是患者對各種靶向療法和化療產(chǎn)生內(nèi)在和獲得性耐藥的主要機(jī)制。TYK-01054能結(jié)合TEAD并抑制了TEAD下游基因的表達(dá),有望為耐藥性腫瘤患者提供新的治療選擇。在國內(nèi)�����,同源康已與NMPA進(jìn)行了Pre-IND溝通交流���,預(yù)計近期將提交TYK-01054的IND申請�����。
國際藥訊
1.AZ哮喘單抗獲批用于低齡兒童�。阿斯利康IL-5Rα單抗Fasenra(benralizumab)獲FDA批準(zhǔn)擴(kuò)大適用人群,用于6至11歲嗜酸性粒細(xì)胞表型嚴(yán)重哮喘患者的附加維持治療�。Benralizumab可直接與嗜酸性粒細(xì)胞上的IL-5受體α結(jié)合���,并吸引自然殺傷細(xì)胞通過細(xì)胞凋亡(程序性細(xì)胞死亡)誘導(dǎo)嗜酸性粒細(xì)胞快速且?guī)缀跬耆谋M���。2017年11月�����,benralizumab首次在美國獲批上市,用于12歲及以上的重癥嗜酸性粒細(xì)胞性哮喘患者的附加維持治療���。
2.艾伯維偏頭痛新藥Ⅲ期臨床積極���。艾伯維CGRP拮抗劑Qulipta(atogepant)用于預(yù)防慢性或發(fā)作性偏頭痛患者疾病發(fā)作的Ⅲ期擴(kuò)展研究結(jié)果積極���。數(shù)據(jù)顯示���,atogepant治療使患者每月偏頭痛天數(shù)平均減少8.5天,且療效維持長達(dá)48周�;患者每月偏頭痛天數(shù)減少≥50%的患者比例達(dá)到70%;atogepant總體安全性良好�����。去年4月,Qulipta用于上市適應(yīng)癥的sNDA申請已獲FDA批準(zhǔn)���。
3.Lipocine公司減脂增肌新藥Ⅱ期臨床積極�����。Lipocine公司減脂增肌口服療法LPCN 2401在治療肥胖或超重并患有體重相關(guān)合并癥患者的Ⅱ期臨床獲積極結(jié)果�。在36周時���,與安慰劑相比,LPCN 2401治療患者的肌肉量(LM)增加4.4%�����,脂肪量(FM)減少6.7%���;同時,患者的腹部脂肪(AF)降低4.1%�,骨礦物質(zhì)含量(BMC)增加2.8%。此外���,藥物治療對患者的體重沒有影響�����,患者的脂肪減少被其無脂體重增加所抵消���。
4.Eliem公司購進(jìn)自免病抗體。Eliem公司宣布完成1.2億美元的融資�����,以用于支持收購Tenet Medicines公司�����,并推動Tenet Medicines主打候選抗體藥物TNT119的開發(fā)�,用于治療多種自身免疫疾病。TNT119旨在靶向和消耗產(chǎn)生自身抗體的CD19陽性B細(xì)胞�,為系統(tǒng)性紅斑狼瘡的潛在治療提供一種新方法。完成收購后�,Eliem公司預(yù)計下半年將啟動TNT119用于治療系統(tǒng)性紅斑狼瘡和免疫性血小板減少癥的Ⅱ期臨床�����。
5.諾華引進(jìn)一款前列腺腫瘤PROTAC���。諾華與Arvinas公司達(dá)成了合作許可協(xié)議�,獲得后者第二代雄激素受體(AR)降解劑ARV-766的全球臨床開發(fā)和商業(yè)化權(quán)益,應(yīng)用于前列腺癌的治療�。諾華還擁有Arvinas公司臨床前AR-V7項(xiàng)目相關(guān)的所有研究、開發(fā)�、制造和商業(yè)化授權(quán)。根據(jù)協(xié)議�����,Arvinas將獲得1.5億美元的預(yù)付款、高達(dá)10.1億美元的開發(fā)���、監(jiān)管和商業(yè)里程碑后期付款�,以及ARV-766的分層版稅���。
6.基因泰克終止超30億美元合作�。Adaptimmune公司宣布,已終止與基因泰克于2021年達(dá)成的超過30億美元的戰(zhàn)略合作�。2021年9月,基因泰克與Adaptimmune公司達(dá)成了研發(fā)和許可協(xié)議:Adaptimmune公司將利用誘導(dǎo)多能干細(xì)胞(iPSC)衍生同種異體細(xì)胞技術(shù)平臺來生成T細(xì)胞�,基因泰克公司將負(fù)責(zé)設(shè)計T細(xì)胞受體(TCR)�,兩家公司將聯(lián)合開發(fā)靶向5種癌癥相關(guān)靶點(diǎn)的同種異體T細(xì)胞療法,以及個體化同種異體T細(xì)胞療法���。
醫(yī)藥熱點(diǎn)
1.香港特區(qū)查獲日本福島等受管地食品���。4月11日�����,香港特區(qū)政府發(fā)布新聞公報�����,香港特區(qū)食物環(huán)境衛(wèi)生署食物安全中心在檢查日本進(jìn)口食品時,發(fā)現(xiàn)其中有來自日本受管制縣份的蔬菜和水產(chǎn)品�����,產(chǎn)品沒有附上輻射證明書及出口商證明書���。有關(guān)進(jìn)口商涉嫌違反相關(guān)《食物安全命令》,涉事產(chǎn)品已被封存�,沒有流出市面���。食安中心正跟進(jìn)該事件���。
2.北京兒童醫(yī)院開出首張“先行先試”罕見病藥品處方�。4月11日,北京兒童醫(yī)院為軟骨發(fā)育不全患兒開出了由北京市罕見病藥品保障先行區(qū)引進(jìn)的“先行先試”罕見病藥品的首張?zhí)幏健T撎幏剿幤访麨?span style="color:#ff0000;">伏索利肽�����,是全球首款治療兒童軟骨發(fā)育不全的罕見病藥品,也是北京罕見病藥品保障先行區(qū)中首款“先行先試”的罕見病藥品�����。
3.成都明確醫(yī)院要配置“醫(yī)保員”。4月8日���,《成都市醫(yī)保員體系建設(shè)管理暫行辦法》公布并實(shí)施�。辦法明確,定點(diǎn)醫(yī)療機(jī)構(gòu)應(yīng)獨(dú)立設(shè)置醫(yī)?��??/span>�,三級醫(yī)院醫(yī)?��?圃瓌t上應(yīng)作為一級科室設(shè)置。床位數(shù)1000以下的醫(yī)療機(jī)構(gòu)���,建議醫(yī)保員配置不少于3人���;床位數(shù)1000以上的醫(yī)療機(jī)構(gòu)�����,建議配置不少于10名醫(yī)保員�����。醫(yī)保員負(fù)責(zé)督導(dǎo)開展本科室(部門)醫(yī)保費(fèi)用審核和自查���,發(fā)現(xiàn)其他工作人員或病人的違法違規(guī)行為報告科室(部門)負(fù)責(zé)人并及時提醒制止�,涉嫌欺詐騙保的�,同步報告醫(yī)院醫(yī)保管理機(jī)構(gòu)。
評審動態(tài)
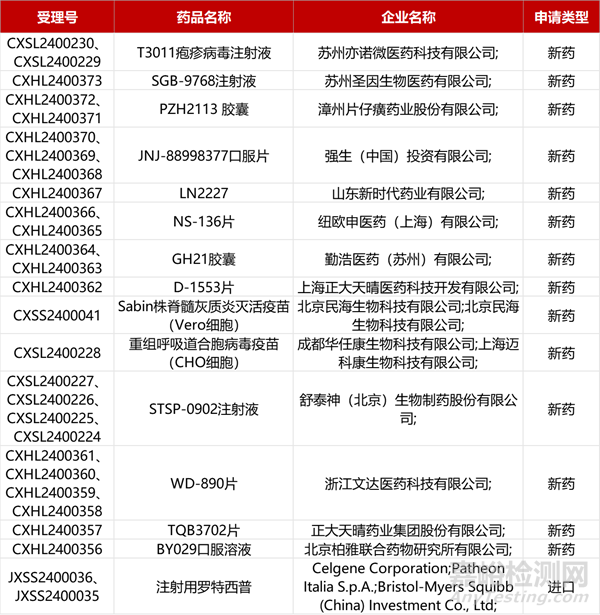
1. CDE新藥受理情況(04月13日)
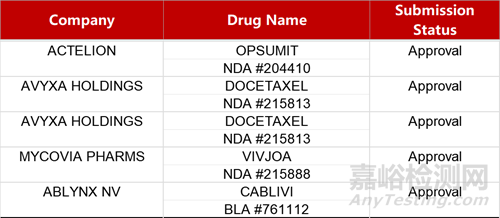
2. FDA新藥獲批情況(北美04月11日)