MDR監(jiān)管要求
眾所周知的是���,無(wú)論處于哪種風(fēng)險(xiǎn)等級(jí),所有醫(yī)療器械都需要將臨床評(píng)價(jià)作為其技術(shù)文檔的組成部分���。
以眼鏡產(chǎn)品為例�����,根據(jù)MDR的監(jiān)管框架��,處方眼鏡與非處方眼鏡均被作為醫(yī)療器械管理�����。而太陽(yáng)眼鏡則被視作個(gè)人裝備��,意味著制造商應(yīng)根據(jù)MDR第 61條和附件XIV的part A策劃�����、實(shí)施和記錄臨床評(píng)價(jià)�����。
眼鏡醫(yī)療器械的共性特征
眼鏡通常被認(rèn)作一項(xiàng)成熟的技術(shù)WET ���,此類醫(yī)療器械共同特點(diǎn)有↓
· 相對(duì)簡(jiǎn)單��、常見(jiàn)且穩(wěn)定的設(shè)計(jì)��,基本無(wú)演變���;
· 其通用器械組具有眾所周知的安全性,并且在過(guò)往與安全問(wèn)題無(wú)關(guān)聯(lián)���;
· 臨床性能特征及其通用器械組采用護(hù)理器械的標(biāo)準(zhǔn),在適應(yīng)癥和最新技術(shù)方面基本無(wú)變化��;
· 在市場(chǎng)上具有悠久的歷史���。
眼鏡醫(yī)療器械的臨床評(píng)價(jià)過(guò)程
■ 常規(guī)而言�����,眼鏡不需要臨床試驗(yàn)或PMCF研究���,因?yàn)榇祟惍a(chǎn)品基于成熟的技術(shù),基本無(wú)創(chuàng)新���,并且有著悠久的市場(chǎng)歷史�����?��?墒褂门R床前和主動(dòng)收集的上市后監(jiān)督(PMS)數(shù)據(jù)以證明眼鏡符合通用安全和性能要求(GSPR)。
■ 此外���,制造商必須進(jìn)行文獻(xiàn)檢索��,包括類似器械的SOTA�����。SOTA的文獻(xiàn)綜述是關(guān)于器械的最新技術(shù)���、臨床背景��、可替代和目前的技術(shù)�����,包括相關(guān)的安全和性能問(wèn)題�����。
對(duì)類似器械開展?jié)撛诘陌踩托阅軉?wèn)題調(diào)查��,并確認(rèn)參數(shù)��,此類參數(shù)用于確定所評(píng)價(jià)器械預(yù)期目的下收益風(fēng)險(xiǎn)比的可接受性�����。
■ 臨床評(píng)價(jià)的第一步是策劃行動(dòng)���,必須確定相關(guān)數(shù)據(jù)并隨后進(jìn)行評(píng)估。
■下一步為分析臨床數(shù)據(jù)并撰寫臨床評(píng)估報(bào)告CER��。
臨床評(píng)價(jià)過(guò)程 如下圖所示↓
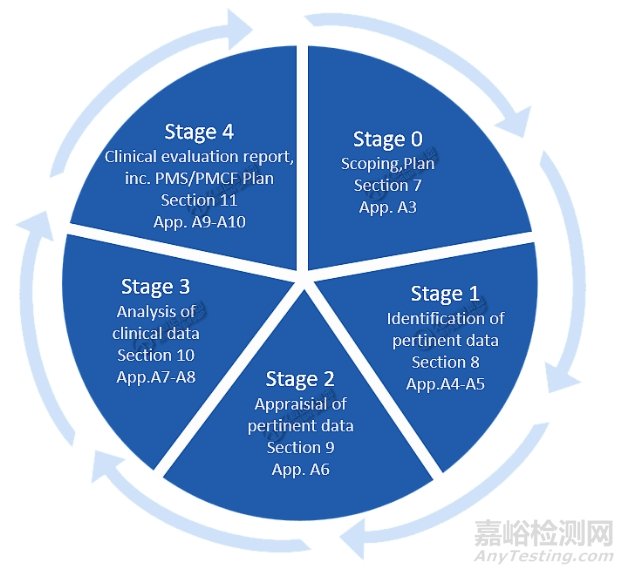
以上圖片解讀如下↓
階段0:范圍���、計(jì)劃
階段1:相關(guān)數(shù)據(jù)的識(shí)別
階段2:相關(guān)數(shù)據(jù)的評(píng)估
階段3:臨床資料的分析
階段4:臨床評(píng)價(jià)報(bào)告�����、PMS/PMCF計(jì)劃
臨床前數(shù)據(jù)包括各領(lǐng)域的測(cè)試結(jié)果��,如:生物相容性�����、生物力學(xué)�����、動(dòng)物試驗(yàn)等���。醫(yī)療器械的風(fēng)險(xiǎn)等級(jí)越低,應(yīng)顯示的臨床前證據(jù)量就越大���。
臨床數(shù)據(jù)可能包括科學(xué)文獻(xiàn)數(shù)據(jù)��、PMS數(shù)據(jù)��。
眼鏡醫(yī)療器械臨床評(píng)價(jià)的挑戰(zhàn)與應(yīng)對(duì)
最常見(jiàn)挑戰(zhàn)是臨床評(píng)價(jià)的及時(shí)規(guī)劃���。由于CER是技術(shù)文檔的最后一份文件��,這意味著應(yīng)事先提供其他文件�����。因此���,編寫 CER 前,應(yīng)完成所有臨床前測(cè)試和 PMS 數(shù)據(jù)的主動(dòng)收集�����。
制造商應(yīng)詳盡測(cè)試其器械�����,以證明其符合標(biāo)準(zhǔn)(協(xié)調(diào))和通用規(guī)范(如適用)�����。此外��,應(yīng)及時(shí)實(shí)施PMS數(shù)據(jù)的主動(dòng)收集�����,并編制技術(shù)文檔。
自身缺乏眼鏡臨床數(shù)據(jù)通常是制造商向MDR過(guò)渡的主要問(wèn)題�����。然而�����,由于這類的許多器械在長(zhǎng)時(shí)間內(nèi)基本保持不變�����,因此來(lái)自市場(chǎng)經(jīng)驗(yàn)的數(shù)據(jù)可支持成熟的技術(shù)(WET)方法��。
充分記錄的臨床評(píng)估計(jì)劃��,是支持法規(guī)提交和CE標(biāo)記過(guò)程的關(guān)鍵因素���。


