隨著目前醫(yī)療器械行業(yè)日新月異的高速發(fā)展�,國內(nèi)外的相關(guān)法規(guī)標(biāo)準(zhǔn)也對醫(yī)療器械生產(chǎn)環(huán)境也提出了更高的要求��。關(guān)于醫(yī)療器械生產(chǎn)潔凈室(區(qū))的國內(nèi)外法規(guī)一系列更新��,特別是24年8月發(fā)布的新版YY/T 0033《無菌醫(yī)療器械生產(chǎn)潔凈室 (區(qū)) 確認(rèn)及監(jiān)測要求》(征求意見稿)中��,對無菌醫(yī)療器械生產(chǎn)潔凈室(區(qū))確認(rèn)及監(jiān)測提出了明確的要求�����。
今天我們來聊聊潔凈室 (區(qū)) 的確認(rèn)及監(jiān)測有哪些最新的核心要點(diǎn)����。
核心術(shù)語須知
潔凈室(區(qū))clean room(zone)
需要對空氣懸浮粒子及微生物含量進(jìn)行控制的房間(區(qū)域)。其建筑結(jié)構(gòu)��、裝備及作用均具有減少該房間(區(qū)域)內(nèi)污染源的介入����、產(chǎn)生和滯留的功能。
潔凈度 cleanliness
潔凈環(huán)境內(nèi)單位體積空氣中含大于或等于某一粒徑的空氣懸浮粒子和微生物的允許統(tǒng)計數(shù)。
潔凈室(區(qū))確認(rèn) clean room(zone)qualification
證實(shí)無菌醫(yī)療器械生產(chǎn)潔凈室(區(qū))是否能夠滿足規(guī)定要求的過程�。
風(fēng)險評估 risk assessment
識別出危險并對與暴露危險相關(guān)的風(fēng)險進(jìn)行分析和評價的系統(tǒng)性過程。
為無菌醫(yī)療器械生產(chǎn)潔凈室(區(qū))設(shè)定的某一參數(shù)(如微生物)的量值��,超過該值��,預(yù)示可能偏離正常狀況���,宜加強(qiáng)關(guān)注或采取糾正措施。
措施限 action level
為無菌醫(yī)療器械生產(chǎn)潔凈室(區(qū))設(shè)定的某一參數(shù)(如微生物)的量值��,超過該值���,表明已偏離正常狀況���,需立即查明原因并采取糾正措施)。
糾正措施 corrective action
當(dāng)監(jiān)測結(jié)果表明警戒限或措施限已被超過時���,需要采取的措施���。
醫(yī)療器械生產(chǎn)潔凈室 (區(qū))的潔凈度等級應(yīng)如何劃分?
潔凈度等級中的ISO 8.5 級潔凈度等級從何而來�?
需保留ISO 8.5 級對應(yīng)的靜態(tài)指標(biāo)嗎?
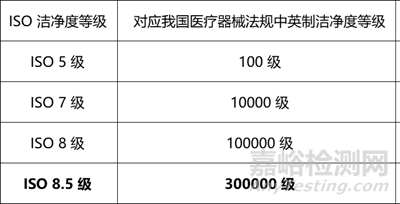
將采用國際通用的 ISO 等級(ISO 5/7/8/8.5 級),對應(yīng)我國法規(guī)英制100/10000/100000/300000 級�;
在醫(yī)藥行業(yè)所關(guān)注的≥0.5μm 粒子濃度,英制 300000 級潔凈度需通過 ISO 等級公式計算�����,代入英制 300000 級對應(yīng)的≥0.5μm 粒子濃度(約 11100000 個 /m³)���,反推得 ISO 等級約為 8.47��,取近似值為8.5����,故英制 300000 級對應(yīng) ISO 8.5 級���;
值得注意的是��,GB/T 25915.1-2021(等同 ISO 14644-1:2015)規(guī)定 ISO 8.5 級僅適用于動態(tài)�,但我國醫(yī)療器械法規(guī)(如《醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范附錄無菌醫(yī)療器械》)仍明確允許在英制 300000 級(對應(yīng) ISO 8.5 級)潔凈室(區(qū))進(jìn)行部分無菌醫(yī)療器械生產(chǎn)�����,且該等級現(xiàn)行指標(biāo)為靜態(tài)指標(biāo)����,為適配國內(nèi)法規(guī)要求及生產(chǎn)實(shí)際����,新版YY/T 0033《無菌醫(yī)療器械生產(chǎn)潔凈室 (區(qū)) 確認(rèn)及監(jiān)測要求》將 ISO 8.5 級對應(yīng)的指標(biāo)應(yīng)用于靜態(tài)�。
無菌醫(yī)療器械生產(chǎn)潔凈室(區(qū))確認(rèn)階段/內(nèi)容有哪些?
確認(rèn)項(xiàng)目的方法包括哪些����?如何選擇���?
首次確認(rèn):潔凈室(區(qū))投入使用前���,需確認(rèn)其潔凈度等級符合要求。再確認(rèn):包括定期再確認(rèn)(需定期開展���,常用項(xiàng)目包括:空氣懸浮粒子���、氣流方向、單向流風(fēng)速/換氣次數(shù)���、高效過濾器完整性)�����、觸發(fā)再確認(rèn)(潔凈室(區(qū))長期停用后復(fù)啟(新增)��,或設(shè)備����、設(shè)施、工藝發(fā)生變更后�����,需視情況進(jìn)行再確認(rèn))�;
無菌醫(yī)療器械生產(chǎn)潔凈室(區(qū))確認(rèn)項(xiàng)目需覆蓋物理參數(shù)、空氣懸浮粒子����、微生物三大核心維度。物理參數(shù)目前均按GB 50591-2010檢測���,但是國際標(biāo)準(zhǔn)ISO 14644-3也規(guī)定了潔凈室(區(qū))物理參數(shù)的測試方法����,ISO 14644-3最新版已等同轉(zhuǎn)化為我國國標(biāo)GB/T 25915.3-2024�?���?紤]到GB/T 25915.3中的方法為國際通用方法���,可優(yōu)先考慮采用GB/T 25915.3-2024中的檢測方法����。溫濕度的檢測暫不考慮采用GB/T 25915.3-2024中規(guī)定的方法����,是因?yàn)?GB/T 25915.3 未對具體溫濕度采樣點(diǎn)進(jìn)行規(guī)定,在使用時可能造成困惑����,故仍要求按GB50591-2010進(jìn)行檢測�。空氣懸浮粒子參考GB/T 16292方法檢測�。空氣微生物(沉降菌���、浮游菌)參考GB/T 16293�、GB/T 16294方法檢測�。表面微生物可參考《中國藥典》四部 9205方法檢測�����。
無菌醫(yī)療器械生產(chǎn)潔凈室(區(qū))的監(jiān)測要求有哪些�����?
潔凈室(區(qū))監(jiān)測計劃為何要求“必須動態(tài)條件下監(jiān)測”�?
監(jiān)測項(xiàng)目頻率應(yīng)如何計劃安排����?
監(jiān)測項(xiàng)目及指標(biāo):常用項(xiàng)目為溫度、相對濕度���、壓差�����、空氣懸浮粒子�、浮游菌�、沉降菌、表面微生物等����;
監(jiān)測方法:需明確采樣點(diǎn)位置����、采樣量�、采樣時間、微生物培養(yǎng)條件(如時間�、溫度、需氧和/或厭氧條件)���;
設(shè)備要求:明確監(jiān)測設(shè)備的準(zhǔn)確度及維護(hù)校準(zhǔn)要求���;
監(jiān)測狀態(tài):必須在動態(tài)條件下進(jìn)行監(jiān)測;
監(jiān)測頻次:給出推薦頻次����,可基于風(fēng)險評估調(diào)整;
限值設(shè)置:對空氣懸浮粒子��、微生物等關(guān)鍵項(xiàng)目設(shè)警戒限和措施限��;
糾正措施:明確結(jié)果超限時的具體糾正措施��;
數(shù)據(jù)管理:規(guī)定數(shù)據(jù)記錄格式�����、趨勢分析方法���、記錄存留要求;
計劃審核:明確監(jiān)測計劃的審核頻次。
動態(tài)監(jiān)測的原因:動態(tài)條件指潔凈室(區(qū))處于 “正常生產(chǎn)狀態(tài)”(含人員操作�、設(shè)備運(yùn)行、物料傳輸)�,此時的污染風(fēng)險(如人員活動、設(shè)備運(yùn)行產(chǎn)生的粒子、微生物)最接近實(shí)際生產(chǎn)場景;而靜態(tài)條件(無人員、設(shè)備停運(yùn))無法反映真實(shí)生產(chǎn)中的潔凈度變化�。無菌醫(yī)療器械生產(chǎn)對環(huán)境潔凈度的要求需貫穿全生產(chǎn)過程,動態(tài)監(jiān)測能更準(zhǔn)確評估實(shí)際生產(chǎn)環(huán)境是否符合要求��,避免靜態(tài)合格但動態(tài)超標(biāo)的情況����,故監(jiān)測需在動態(tài)條件下進(jìn)行。
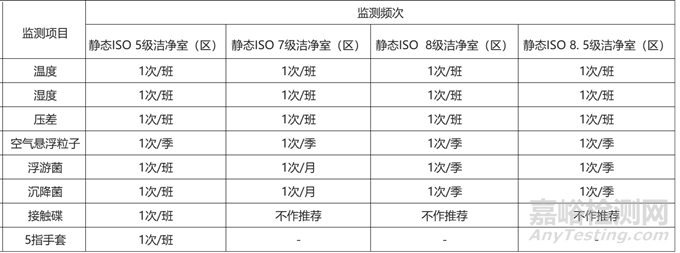
潔凈室(區(qū))常用監(jiān)測項(xiàng)目推薦的監(jiān)測頻次如下表����。推薦的監(jiān)測頻次可基于風(fēng)險評估及持續(xù)監(jiān)測結(jié)果予以調(diào)整��。