內(nèi)毒素檢測(cè)在現(xiàn)代生物制品和醫(yī)藥領(lǐng)域中扮演著至關(guān)重要的角色�����,注射類藥物��、注射器具�����,植入醫(yī)療器械等都有相應(yīng)的質(zhì)量標(biāo)準(zhǔn)��,用以確保產(chǎn)品安全性���。然而,在進(jìn)行內(nèi)毒素檢測(cè)的過程中�����,許多實(shí)驗(yàn)室和研究人員可能會(huì)面臨一系列挑戰(zhàn)和疑惑��。
其中低內(nèi)毒素回收(LER)一直是備受關(guān)注的熱門話題���,以下十個(gè)有關(guān)低內(nèi)毒素回收的問題你了解嗎��??jī)?nèi)毒素檢測(cè)專家Lonza為你解答�����。
Q:為何LER對(duì)生物制品生產(chǎn)非常重要�����?
A:法規(guī)要求生物制品需要通過兔熱原實(shí)驗(yàn)檢測(cè)熱原含量以確保產(chǎn)品的安全性�����。如果能夠證明細(xì)菌內(nèi)毒素測(cè)試于兔熱原等效�����,則可使用細(xì)菌內(nèi)毒素測(cè)試代替兔熱原進(jìn)行檢測(cè)。需要注意的是�����,某些生物制品使用內(nèi)毒素檢查法檢測(cè)時(shí)會(huì)存在LER效應(yīng)��,生產(chǎn)廠家需要使用兔熱原進(jìn)行檢測(cè)。
為了確認(rèn)LER是否和體內(nèi)的非內(nèi)毒素?zé)嵩粯赢a(chǎn)生致熱反應(yīng)��,法規(guī)要求生物制品制造廠家進(jìn)行加標(biāo)(Hold-time) 研究��,并且���,相同時(shí)間點(diǎn)也需要進(jìn)行兔熱原檢測(cè)。
Q:FDA 對(duì)LER持什么樣的態(tài)度���?
A:LER主要于生物制品有關(guān),主要是與單克隆抗體及一些治療用融合抗體��。加標(biāo)(Hold-time)研究表明LER不僅僅受到賦性劑的影響��,蛋白濃度��、內(nèi)毒素檢測(cè)方法���、檢測(cè)試劑的供應(yīng)商、Hold-time研究所用溫度及時(shí)間都是影響LER的主要因素�����。此外,角標(biāo)內(nèi)毒素的種類(RSE, CSE�����,NOE)也會(huì)影響最終結(jié)果���。
Q:怎樣進(jìn)行Hold-time 研究��?
A:
①向未稀釋樣品中加入一定濃度的內(nèi)毒素 (加標(biāo)內(nèi)毒素濃度≤樣品釋放限值)
②根據(jù)測(cè)試樣品信息確定hold-time研究參數(shù)(溫度,容器類型�����,考察時(shí)間點(diǎn))
③在特定的時(shí)間點(diǎn)進(jìn)行內(nèi)毒素檢測(cè)(例如:4小時(shí)���,24小時(shí)�����,72小時(shí)��,5天��,7天)
④計(jì)算回收率
Q:FDA對(duì)于Hold-time 研究有哪些建議���?
A:FDA對(duì)于Hold-time研究的建議總結(jié)如下:
①至少進(jìn)行3批產(chǎn)品的驗(yàn)證
②添加內(nèi)毒素濃度≤樣品的釋放限值
③對(duì)于產(chǎn)品的研究至少8天
④使用工作標(biāo)準(zhǔn)品作為最差條件進(jìn)行研究
Q:天然來源內(nèi)毒素( Naturally Occurring Endotoxin ,NOE)和標(biāo)準(zhǔn)內(nèi)毒素的區(qū)別��?
A:天然來源的內(nèi)毒素(NOE)是從革蘭氏陰性菌中粗提出來的內(nèi)毒素��。與RSE或者CSE 不同��,天然來源的內(nèi)毒素(NOE)是不經(jīng)過純化的內(nèi)毒素。與RSE或者CSE 相比, NOE不容易導(dǎo)致LER���,這可能與NOE為非精制提純內(nèi)毒素��,含有蛋白質(zhì)和細(xì)胞碎片物有關(guān)���。
Q:與RSE或者CSE相比,使用NOE 進(jìn)行研究是否有優(yōu)勢(shì)���?
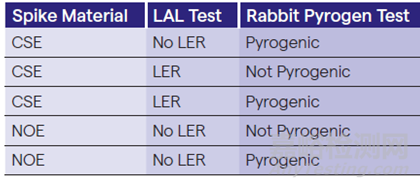
A:從提交給FDA的幾個(gè)BLA匯編數(shù)據(jù)來看(見表一)�����,不論內(nèi)毒素來源如何���,即不論使用CSE或者是NOE,細(xì)菌內(nèi)毒素測(cè)試和兔熱原檢測(cè)結(jié)果都存在沖突��。這些數(shù)據(jù)從另外一方面表明,即使使用內(nèi)毒素檢測(cè)產(chǎn)生了LER現(xiàn)象���,兔熱原檢測(cè)依然能夠檢測(cè)樣品是否會(huì)引起熱原反應(yīng)�����。這個(gè)因?yàn)檫@個(gè)原因��,F(xiàn)DA 不支持或不鼓勵(lì)在Hold-time研究中使用NOE��。此外���,每種NOE從不同的菌種中制備并且菌種也會(huì)受到不同生長(zhǎng)條件影響��。所以���,如果沒有NOE的標(biāo)準(zhǔn)化制備流程���,監(jiān)管機(jī)構(gòu)無法判斷NOE 是否能夠有效代替標(biāo)準(zhǔn)內(nèi)毒素��。
表一:提交給FDA 的BLA數(shù)據(jù)摘要
目前有一些研究學(xué)者在Hold-time研究中使用了NOE�����,并且獲得了較好的結(jié)果。并且結(jié)果發(fā)表于2015年9月的美國藥典論壇���,該論文的主要觀點(diǎn)為與標(biāo)準(zhǔn)內(nèi)毒素相比NOE更加穩(wěn)定并且引起LER的可能性更小��。然而��,也有研究學(xué)者對(duì)此持反對(duì)意見�����。因?yàn)閷?shí)驗(yàn)結(jié)果表明���,某些未稀釋樣品中添加的NOE或者CSE/RSE 不能回收回來。因此�����,關(guān)于NOE 能夠成功解決LER問題仍然未有定論。
Q:是否可以使用分散劑解決LER問題��?
A:有一些樣品能夠使用分散劑��,例如PyroSperse™來解決LER問題���。然而,由于每個(gè)樣品出現(xiàn)LER問題的原因都不盡相同���,所以分散劑并不能解決所有問題��。當(dāng)出現(xiàn)LER問題時(shí)可以先使用分散劑如PyroSperse™來進(jìn)行摸索研究���,如果分散劑不能解決問題���,則需要探究其他樣品前處理方式���。
Q:解決LER問題的樣品前處理方式有哪些?
A:解決LER問題的主要思路為去除遮蔽現(xiàn)象��。主要處理方式包括:①調(diào)節(jié)pH��,影響氫鍵②添加Mg2+/Ca2+���,防止螯合劑螯合內(nèi)毒素聚合物中的二價(jià)離子③使用分散劑PyroSperse™��,干擾內(nèi)毒素聚集
Q:LER是否有潛在公共安全性問題���?
A:FDA對(duì)于LER及其與藥物安全性的相關(guān)性問題持保守謹(jǐn)慎態(tài)度��。盡管目前沒有報(bào)道表明LER有公共安全問題��,但是FDA擔(dān)心某些藥物會(huì)因?yàn)長(zhǎng)ER問題不能通過USP<85>檢出內(nèi)毒素��,從而引起人體熱原反應(yīng)。
Q:有哪些組織正在幫助醫(yī)藥生產(chǎn)商研究LER問題���?
A:PDA (Parenteral Drug Association)以及BPOG (Biophorum Operations Group)均成立LER研究工作組�����,用于研究LER的影響以及解決LER問題的方案��。試劑供應(yīng)商�����、內(nèi)毒素檢測(cè)終端用戶與全球監(jiān)管機(jī)構(gòu)緊密合作,共同調(diào)查并給出受LER影響的產(chǎn)品的建議��。