引用本文
史宇航���,梁毅*.跨國醫(yī)藥公司實施ICH 指南的挑戰(zhàn)與對策思考[J].中國食品藥品監(jiān)管.2025.8(259):130-137.
跨國醫(yī)藥公司實施ICH 指南的挑戰(zhàn)與對策思考
Challenges and Countermeasures for Multinational Pharmaceutical Companies in Implementing ICH Guidelines
史宇航
中國藥科大學國際醫(yī)藥商學院
SHI Yu-hang
School of International Pharmaceutical Business, China Pharmaceutical University
梁毅*
中國藥科大學國際醫(yī)藥商學院
LIANG Yi*
School of International Pharmaceutical Business,China Pharmaceutical University
摘 要 Abstract
隨著全球化程度的逐漸加深與醫(yī)藥行業(yè)的不斷發(fā)展�,國際人用藥品注冊技術(shù)協(xié)調(diào)會(ICH)指南的持續(xù)更新對跨國醫(yī)藥公司的影響日益顯著�。跨國醫(yī)藥公司需要密切關(guān)注有關(guān)變化����,及時調(diào)整業(yè)務(wù)策略和運營模式,確保適應并遵循不斷更新的ICH 指南要求����。本文采用文獻分析與政策研究方法,基于ICH 發(fā)展背景與跨國醫(yī)藥公司發(fā)展模式���,分析跨國醫(yī)藥公司在實施ICH 指南時遇到的主要挑戰(zhàn)以及應對策略����,同時探索構(gòu)建跨國醫(yī)藥公司質(zhì)量管理通用標準�,以期為其更好地實施ICH 指南提供參考?���?鐕t(yī)藥公司應將適應和實施不斷更新的ICH 指南作為持續(xù)監(jiān)測的戰(zhàn)略重點�,以確保其在全球醫(yī)藥市場中保持競爭優(yōu)勢����,實現(xiàn)可持續(xù)發(fā)展。
With the deepening of globalization and the ongoing evolution of the pharmaceutical industry, frequent updates to the International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use (ICH) guidelines have had an increasingly significant impact on multinational pharmaceutical companies. These companies must closely monitor regulatory developments, promptly adjust business strategies and operational models, and ensure timely compliance with the evolving ICH requirements. This paper employs literature review and policy analysis methodologies to examine the key challenges faced by multinational pharmaceutical companies in implementing ICH guidelines, taking into account the historical development of ICH and corporate operational strategies. Furthermore, it proposes the construction of a general quality management framework adaptable across multinational operations to facilitate effective implementation of ICH standards.It is recommended that multinational pharmaceutical companies treat the adaptation to and implementation of updated ICH guidelines as a continuous strategic priority to maintain competitiveness in the global pharmaceutical market and achieve sustainable development.
關(guān)鍵詞 Key words
國際人用藥品注冊技術(shù)協(xié)調(diào)會指南�;跨國醫(yī)藥公司;監(jiān)管�;挑戰(zhàn);策略
ICH guidelines; multinational pharmaceutical companies; regulation; challenges; strategies
國際人用藥品注冊技術(shù)協(xié)調(diào)會
(The International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use���,ICH)是致力于促進全球藥品監(jiān)管協(xié)調(diào)與統(tǒng)一的國際組織���,通過制定共同的藥品監(jiān)管指南,推動國際藥品研發(fā)�、注冊、生產(chǎn)等監(jiān)管工作的合作與互認���。ICH的成立可以追溯至1990 年,全球制藥行業(yè)面臨著越來越多的挑戰(zhàn)���,如快速發(fā)展的科學技術(shù)����、日益嚴格的法律法規(guī)、不斷增長的國際貿(mào)易需求等����。為了應對相關(guān)挑戰(zhàn),歐洲���、美國和日本藥品監(jiān)管機構(gòu)及相關(guān)組織共同發(fā)起成立ICH�。2017 年6 月�,原國家食品藥品監(jiān)督管理總局正式加入ICH,標志著我國藥品標準在國際合作領(lǐng)域邁出重要的一步[1]���。ICH 指南涵蓋多個方面的內(nèi)容�,包括藥物非臨床研究����、藥物臨床試驗設(shè)計、質(zhì)量控制標準����、安全性評估以及藥品注冊申請等。這些內(nèi)容經(jīng)過廣泛的學者討論與專家評審���,具有較好的科學性����、有效性、可操作性等����。由于ICH 成員覆蓋全球主要的藥品市場,ICH 指南具有較高的國際認可度和適用性����,許多國家和地區(qū)藥品監(jiān)管機構(gòu)將ICH 指南作為藥品注冊審評審批的參考標準。
跨國醫(yī)藥公司在全球醫(yī)藥市場中扮演著重要角色����,ICH 指南的持續(xù)更新對其影響深遠。首先���,跨國醫(yī)藥公司通常承擔藥物研發(fā)的重要工作�。其通常擁有龐大的專家團隊和充足的研發(fā)資金�,致力于藥物創(chuàng)新,推動全球醫(yī)藥領(lǐng)域進步����。其次���,跨國醫(yī)藥公司通常具有較多藥品國際市場準入的現(xiàn)實任務(wù)�。其通常在多個國家和地區(qū)注冊與銷售產(chǎn)品,需要考慮藥品國際市場準入順序以及遵守不同國家和地區(qū)的監(jiān)管要求�,從而有效推動產(chǎn)品在全球范圍內(nèi)上市銷售。最后�, 跨國醫(yī)藥公司對于國際合作與協(xié)調(diào)“ 生態(tài)系統(tǒng)”的需求較大。其通常與不同國家和地區(qū)醫(yī)療機構(gòu)����、學術(shù)研究機構(gòu)等開展多方合作,促進科研成果的轉(zhuǎn)化和應用�,推動醫(yī)藥科技的發(fā)展。因此�,跨國醫(yī)藥公司需要及時監(jiān)測ICH 指南的更新動態(tài),為全球患者提供數(shù)量與質(zhì)量并重的醫(yī)藥產(chǎn)品與服務(wù)����。本文基于ICH 發(fā)展背景與跨國醫(yī)藥公司發(fā)展模式,探析ICH 指南實施過程中的主要挑戰(zhàn)和應對策略�,并探索構(gòu)建跨國醫(yī)藥公司質(zhì)量管理通用標準,以期為其更好地實施ICH 指南提供參考���。
1 ICH 及其指南發(fā)展概況
2015 年10 月����,ICH 召開大會宣布進行組織改革,根據(jù)瑞士法律�,成為一個具有法律實體的國際組織。此次會議的召開不僅代表ICH 總結(jié)并交付了已探索25 年的全球藥品監(jiān)管指南�,同時也反映出世界各國和地區(qū)對藥品研發(fā)、注冊����、生產(chǎn)等監(jiān)管環(huán)節(jié)達成長期協(xié)調(diào)穩(wěn)定的愿景。協(xié)調(diào)監(jiān)管要求是由歐共體于20 世紀80 年代初期提出的����,歐洲各國和地區(qū)向藥品市場的聯(lián)合邁進證明了協(xié)調(diào)監(jiān)管的可行性。1989年����, 在法國巴黎舉行的世界衛(wèi)生組織國際藥品監(jiān)管機構(gòu)會議(International Conference of Drug Regulatory Authorities,ICDRA)就實際操作計劃展開了研究����。隨后,世界衛(wèi)生組織與國際藥品制造商協(xié)會聯(lián)合會(The International Federation of Pharmaceutical Manufacturers and Associations����,IFPMA) 商討了關(guān)于國際協(xié)調(diào)的行業(yè)監(jiān)管聯(lián)合倡議, 并構(gòu)思成立ICH。1990 年�,歐洲制藥工業(yè)協(xié)會聯(lián)合會(European Federation of Pharmaceutical Industries and Associations,EFPIA)在布魯塞爾召開會議�, 各方代表共同討論了ICH 的意義與任務(wù)����。2015 年,ICH 被確立為獨立的法律實體���,旨在形成更加穩(wěn)定的運行結(jié)構(gòu)�,不斷增加國際外聯(lián)����,向更廣泛的利益相關(guān)者傳播更多關(guān)于藥品監(jiān)管的信息。
ICH 指南的發(fā)展歷程可主要分為4 個階段:① ICH 指南制定初期����。其內(nèi)容主要是圍繞國際藥品注冊技術(shù)要求編寫的,包括質(zhì)量(quality)���、安全性(safety)�、有效性(efficacy) 和多學科(multidisciplinary) 等方面���。② ICH 指南的修訂與進一步擴展�。ICH 指南經(jīng)過不斷修訂和擴展,以適應不斷發(fā)展的科學技術(shù)和國際藥品監(jiān)管的需求����。③全球多方利益相關(guān)者參與編寫。許多國家和地區(qū)藥品監(jiān)管機構(gòu)與全球制藥行業(yè)協(xié)會逐漸在ICH 指南研討過程中貢獻自身力量����。④ ICH 應對新興挑戰(zhàn)。近年來�,隨著科學技術(shù)在醫(yī)藥領(lǐng)域的快速發(fā)展,ICH不斷應對新興挑戰(zhàn)�,如生物標志物、人工智能等在藥品研發(fā)和注冊中得到應用���。為了應對這些新的挑戰(zhàn)����,ICH 不斷修訂和更新其指南����,以持續(xù)引領(lǐng)國際藥品注冊和監(jiān)管標準的更新。
2 跨國醫(yī)藥公司發(fā)展模式概況
跨國醫(yī)藥公司通常具有較為復雜的發(fā)展模式�,以應對快速變化的全球醫(yī)藥市場與不斷更新的國際監(jiān)管要求。
2.1 運營模式
跨國醫(yī)藥公司的運營模式主要分為2 種:研發(fā)驅(qū)動型和市場驅(qū)動型。研發(fā)驅(qū)動型運營主要是指采用研發(fā)驅(qū)動模式����,將創(chuàng)新作為主要競爭優(yōu)勢。這些公司通常在全球范圍內(nèi)擁有龐大的研發(fā)團隊�,并投入大量資金用于新藥研發(fā)。市場驅(qū)動型運營主要是指采用市場驅(qū)動模式���,注重市場營銷和銷售,將產(chǎn)品推向全球市場����。這些公司通常在全球范圍內(nèi)建立了強大的銷售網(wǎng)絡(luò)和分銷渠道,以確保產(chǎn)品的廣泛覆蓋和市場份額的增長�。
2.2 全球布局
跨國醫(yī)藥公司在全球布局時重點考慮總部協(xié)調(diào)、研發(fā)設(shè)計與生產(chǎn)基地����。總部協(xié)調(diào)即總部地區(qū)規(guī)劃���,跨國醫(yī)藥公司通常在全球范圍內(nèi)的政治金融中心設(shè)立總部���,以便管理和協(xié)調(diào)各地業(yè)務(wù),總部負責制定地區(qū)戰(zhàn)略、管理運營活動���,并與當?shù)卣?、行業(yè)組織和合作伙伴等溝通交流�。研發(fā)設(shè)計即布局研發(fā)中心,跨國醫(yī)藥公司通常在全球范圍內(nèi)的人才聚集地設(shè)立研發(fā)中心�,以便充分利用當?shù)氐目蒲腥肆Y源開展藥物研發(fā)和創(chuàng)新活動,研發(fā)中心通常擁有先進的實驗設(shè)備和技術(shù)平臺���,致力于研發(fā)新藥物����?���?鐕t(yī)藥公司的生產(chǎn)基地主要分布在全球范圍內(nèi)資源豐富之處,以滿足不同國家和地區(qū)的市場需求���,生產(chǎn)基地通常按照國際標準建設(shè)�,并受當?shù)乇O(jiān)管機構(gòu)的監(jiān)管���。
2.3 國際化戰(zhàn)略
部分跨國醫(yī)藥公司采用標準化戰(zhàn)略�,即在不同國家和地區(qū)使用相同的品牌和產(chǎn)品,并采用統(tǒng)一的營銷和銷售策略���。這種戰(zhàn)略有助于降低成本����,提高效率���,增強品牌影響力����。另有部分跨國醫(yī)藥公司采用本地化戰(zhàn)略�,根據(jù)不同國家和地區(qū)的文化�、法規(guī)和市場需求,定制產(chǎn)品以及營銷和銷售策略����。這種戰(zhàn)略可以更好地適應當?shù)厥袌霏h(huán)境,提高產(chǎn)品的市場競爭力���。目前����,較多跨國醫(yī)藥公司樂于與當?shù)叵嚓P(guān)組織和機構(gòu)進行戰(zhàn)略合作,共同開發(fā)市場和推廣產(chǎn)品���,助其更好地理解當?shù)厥袌龊托袠I(yè)環(huán)境����,更快實現(xiàn)市場準入和增長�。
3 跨國醫(yī)藥公司實施ICH 指南面臨的挑戰(zhàn)
3.1 ICH 指南更新較快
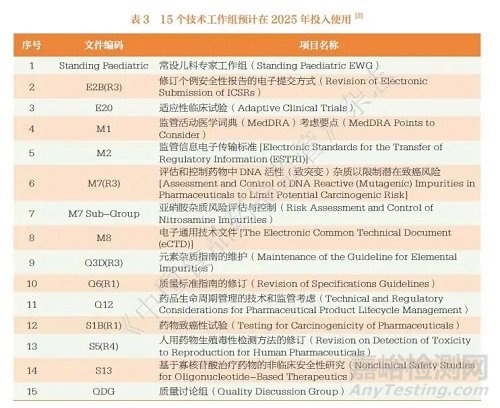
筆者分析ICH 官網(wǎng)發(fā)布的《2025 年度ICH 工作計劃》(ICH Association 2025 Annual Work Plan)[2] 發(fā)現(xiàn),ICH 于2024 年初步計劃了2025 年度5 類目工作����,其中戰(zhàn)略工作(Strategy)6 項、協(xié)調(diào)工作(Harmonisation)4 項�、運營工作(Operations)22 項、程序工作(Procedures)3 項�、溝通交流工作(Communication)4 項。此外�,工作計劃包含3 個附件:附件1 為10 個技術(shù)工作組預計在2025 年達到步驟4 或?qū)崿F(xiàn)最終交付,見表1 �;附件2 為7個技術(shù)工作組預計在2025 年達到步驟2a/b,見表2 �;附件3 為15 個技術(shù)工作組預計在2025 年投入使用,見表3����。ICH 指南逐年快速的更新與完善為跨國醫(yī)藥公司帶來了挑戰(zhàn)���,主要體現(xiàn)在以下3 個方面。
3.1.1 反應時間壓力
跨國醫(yī)藥公司通常需要花費大量時間和精力了解更新變化的ICH指南�,并將其應用到業(yè)務(wù)實踐中。不論是學習更新的ICH 指南����,還是將ICH 指南轉(zhuǎn)化到實踐中,都需要較長時間�,這可能導致項目延遲或者影響產(chǎn)品上市規(guī)劃,從而影響企業(yè)的收入和市場競爭力���。
3.1.2 技術(shù)難題壓力
部分ICH 指南的更新涉及技術(shù)要求的提升���,跨國醫(yī)藥公司需要采用新的技術(shù)以達到相關(guān)要求���。ICH 指南對非臨床研究與臨床試驗數(shù)據(jù)管理具有嚴格的要求�,跨國醫(yī)藥公司需要具備先進的數(shù)據(jù)采集���、統(tǒng)計分析����、整理歸納等技術(shù),還需要具備先進的藥物安全評價技術(shù)和監(jiān)測手段�。此外,ICH 指南對藥品的生產(chǎn)工藝���、質(zhì)量控制和質(zhì)量保證等具有較高的標準�,如在穩(wěn)定性���、純度���、雜質(zhì)等方面,跨國醫(yī)藥公司需要建立健全質(zhì)量管理體系����,確保藥品生產(chǎn)過程的合規(guī)性和產(chǎn)品質(zhì)量的穩(wěn)定性。
3.1.3 成本增加壓力
跨國醫(yī)藥公司通常需要不斷投入資源用于員工培訓與教育�,以及與監(jiān)管機構(gòu)持續(xù)溝通等,以適應ICH 指南的快速更新�。具體而言,跨國醫(yī)藥公司需要為員工提供有關(guān)ICH 指南的知識培訓�,以確保員工了解和遵循相關(guān)要求,該成本可能涉及組織內(nèi)部培訓課程����、組織外部學習活動以及雇傭?qū)I(yè)顧問等費用����。與監(jiān)管機構(gòu)溝通的成本是指跨國醫(yī)藥公司在日常運營過程中與監(jiān)管機構(gòu)進行持續(xù)交流需要付出的成本�。
3.2 國際監(jiān)管要求存在差異
3.2.1 實施進度差異
不同國家和地區(qū)的藥品監(jiān)管機構(gòu)對于ICH 指南的實施進度具有差異。有的國家和地區(qū)能夠快速落實全部ICH 指南���,也有國家和地區(qū)受各種因素影響只能實施部分ICH 指南[3]���。跨國醫(yī)藥公司需要靈活調(diào)整項目計劃���,選擇適合藥品先行進入的國家和地區(qū)�,并確保及時提交和更新注冊申請�。
3.2.2 注冊申請差異
不同國家和地區(qū)的藥品監(jiān)管機構(gòu)對于符合ICH 指南的藥品注冊申請的要求具有差異[4]。一些國家和地區(qū)藥品監(jiān)管機構(gòu)要求提交詳細和全面的數(shù)據(jù)����,也有一些國家和地區(qū)藥品監(jiān)管機構(gòu)對部分數(shù)據(jù)的要求較少���??鐕t(yī)藥公司需要根據(jù)不同國家和地區(qū)藥品監(jiān)管機構(gòu)的要求準備申請資料�,確保其符合對應市場的規(guī)范�。
3.2.3 審查標準差異
不同國家和地區(qū)的藥品監(jiān)管機構(gòu)可能采用不同的審查標準和評價方法對ICH 指南的符合性進行審查�。一些國家和地區(qū)可能更加關(guān)注藥品的安全性,也有一些國家和地區(qū)可能更加注重藥品的療效和臨床效果����。跨國醫(yī)藥公司需要根據(jù)不同國家和地區(qū)藥品監(jiān)管機構(gòu)的要求進行不同的臨床試驗設(shè)計和數(shù)據(jù)分析整理����。
3.3 跨國醫(yī)藥公司內(nèi)部調(diào)整管理困難
3.3.1 內(nèi)部組織結(jié)構(gòu)和工作流程調(diào)整困難
首先�,部分跨國醫(yī)藥公司內(nèi)部存在組織文化差異??鐕t(yī)藥公司可能在不同國家和地區(qū)設(shè)有多個分支機構(gòu),每個分支機構(gòu)具有不同的組織文化和工作方式���,不同部門或團隊可能對新的ICH指南持有不同的態(tài)度���。其次,跨國醫(yī)藥公司不同部門或團隊之間可能存在權(quán)力和利益沖突�。例如,研發(fā)部門通常希望加快新藥研發(fā)進程�,而質(zhì)量管理部門可能更關(guān)注合規(guī)性和產(chǎn)品質(zhì)量,各方可能對適應新的ICH 指南產(chǎn)生不同的意見。最后����,部分跨國醫(yī)藥公司內(nèi)部信息溝通和協(xié)調(diào)困難。不同部門或團隊之間信息溝通和交流困難�,可能導致新的ICH 指南的信息難以被有效傳達和理解,影響變革的推進和實施效果���。
3.3.2 內(nèi)部實現(xiàn)標準化困難
跨國醫(yī)藥公司在實施ICH 指南時���,其內(nèi)部在實現(xiàn)標準化過程中可能面臨多種挑戰(zhàn)。首先���,業(yè)務(wù)流程多元化����。由于地理位置不同���,市場需求存在差異���,跨國醫(yī)藥公司在不同國家和地區(qū)的業(yè)務(wù)流程呈現(xiàn)多樣性,其內(nèi)部要實現(xiàn)標準化����,需要克服不同業(yè)務(wù)流程之間的差異挑戰(zhàn)。其次�,技術(shù)平臺不一致���??鐕t(yī)藥公司在不同國家和地區(qū)可能使用不同的信息技術(shù)平臺和軟件系統(tǒng)來支持業(yè)務(wù)開展���,技術(shù)平臺不一致可能導致數(shù)據(jù)整合和信息共享困難���,阻礙標準化的實現(xiàn)[5]�。最后,標準化流程需要持續(xù)改進�。實現(xiàn)標準化不是一次性的任務(wù)���,而是一個持續(xù)改進的過程����?���?鐕t(yī)藥公司需要建立有效的監(jiān)控機制和反饋機制,及時發(fā)現(xiàn)和解決標準化過程中的問題�,并持續(xù)改進標準化流程,以確保其有效性和持續(xù)性�。
4 跨國醫(yī)藥公司應對ICH 指南更新的策略
4.1 加強溝通交流���,緊跟前沿動態(tài)
跨國醫(yī)藥公司應與藥品監(jiān)管機構(gòu)和行業(yè)協(xié)會保持密切溝通交流�,以確保及時獲取ICH 指南更新變化的重要信息����,使其運營符合最新的ICH 指南要求�。一方面,跨國醫(yī)藥公司應加強與不同國家和地區(qū)藥品監(jiān)管機構(gòu)的溝通與協(xié)調(diào)���,建立開放���、透明的溝通渠道,定期進行會議交流�,及時向監(jiān)管機構(gòu)報告項目進展信息,積極回應監(jiān)管機構(gòu)提出的問題和疑慮����,與監(jiān)管機構(gòu)形成長期穩(wěn)定的溝通交流關(guān)系���,通過參與政府部門組織的會議和研討等活動����,建立持續(xù)改進機制,不斷總結(jié)經(jīng)驗教訓���,提升內(nèi)部合規(guī)水平[6]����。另一方面���,跨國醫(yī)藥公司應積極與行業(yè)協(xié)會和倡導團體溝通交流���,如IFPMA、生物技術(shù)創(chuàng)新組織(Biotechnology Innovation Organization����,BIO)、EFPIA 等�,分享相關(guān)經(jīng)驗和資源���,共同推動ICH 指南的制定和實施。
4.2 優(yōu)化內(nèi)部組織結(jié)構(gòu)
跨國醫(yī)藥公司可建立專門的團隊或部門跟蹤ICH 指南合規(guī)工作�,并及時調(diào)整工作流程以滿足需要。該團隊或部門可以是一個典型的跨職能工作組�,例如,其成員可以包含臨床試驗�、質(zhì)量管理、藥物警戒等部門的代表�。此舉不僅可以兼顧各項工作的順利開展,也考慮到公司內(nèi)部各方利益�,有利于ICH 指南的實施���。此外����,該團隊或部門可負責不同部門之間的溝通協(xié)作�,解決跨部門合作中的問題和矛盾,確保信息暢通�,并識別現(xiàn)存的瓶頸問題,采取優(yōu)化措施�,建立健全質(zhì)量控制和風險管理系統(tǒng),確保所有業(yè)務(wù)活動符合質(zhì)量標準和合規(guī)要求����。
4.3 制定內(nèi)部標準化流程
跨國醫(yī)藥公司可制定和實施內(nèi)部標準化流程和操作規(guī)范���,并不斷改進,以確保持續(xù)遵循ICH指南要求�,提高業(yè)務(wù)運作的效率和質(zhì)量,增強市場競爭力���。首先,全面分析和評估當前的業(yè)務(wù)流程和操作規(guī)范����,確定與ICH 指南要求相符的部分,并認定其為標準化流程���,重點關(guān)注有待調(diào)整或持續(xù)更新的環(huán)節(jié)���。其次,確保已被認定的標準化流程的質(zhì)量管控工作按照統(tǒng)一的標準進行�,包括標準化的操作流程、文件模板����、記錄格式等[7]����。最后�,建立持續(xù)改進機制,不斷優(yōu)化和完善標準化流程和操作規(guī)范����,以適應業(yè)務(wù)發(fā)展的需要和指南更新的要求。
5 對于跨國醫(yī)藥公司構(gòu)建質(zhì)量管理通用標準的思考
跨國醫(yī)藥公司需要在復雜多變的市場環(huán)境中重點關(guān)注并堅持實施ICH 指南����,筆者探索構(gòu)建跨國醫(yī)藥公司的質(zhì)量管理通用標準,以期為跨國醫(yī)藥公司進行常態(tài)化運營的合理監(jiān)管提供參考���。
5.1 嚴格執(zhí)行藥物非臨床研究質(zhì)量管理規(guī)范
跨國醫(yī)藥公司應遵守藥物非臨床研究質(zhì)量管理規(guī)范(good laboratory practice���,GLP),以符合ICH 指南的相關(guān)要求�。精心設(shè)計研究方案,確保研究結(jié)果的可靠性和可重復性����。合理選擇動物模型和研究方法,避免潛在的偏差。尋找并應用新的技術(shù)和方法�,以提高研究效率和準確性。建立完善的數(shù)據(jù)管理系統(tǒng)���,確保數(shù)據(jù)的完整性和安全性����,并利用統(tǒng)計學方法對數(shù)據(jù)進行深入分析����,發(fā)現(xiàn)其潛在的規(guī)律和趨勢。
5.2 優(yōu)化藥物臨床試驗設(shè)計與執(zhí)行
跨國醫(yī)藥公司可通過開展多中心臨床試驗����、隨機雙盲對照試驗等����,確保試驗結(jié)果的準確性和可靠性[8]。同時���,采用先進的臨床試驗技術(shù)和方法���,如生物標志物分析、適應性設(shè)計等���,提高臨床試驗效率和成本效益[9]����。
5.3 加強藥品生產(chǎn)與流通質(zhì)量管理
跨國醫(yī)藥公司應建立健全質(zhì)量管理體系,包括標準化的質(zhì)量控制流程����、質(zhì)量文檔管理系統(tǒng)、質(zhì)量審核和評估機制等���。具體而言����,建立標準化的質(zhì)量控制流程���,包括原材料采購���、生產(chǎn)制造、包裝和分銷等環(huán)節(jié)的質(zhì)量控制和監(jiān)督���;制定可追溯的質(zhì)量文檔管理系統(tǒng)���,包括電子文檔管理系統(tǒng)���、數(shù)據(jù)采集和分析平臺、物聯(lián)網(wǎng)平臺等�,實現(xiàn)數(shù)據(jù)的實時監(jiān)測和管理[10] ;實施質(zhì)量審核和評估機制���,定期對質(zhì)量管理體系進行內(nèi)部審核和外部認證���,以確保符合ICH指南和相關(guān)法規(guī)要求。
5.4 健全藥物警戒體系
跨國醫(yī)藥公司應建立完善的藥物安全評價與監(jiān)測體系�,包括臨床試驗前、臨床試驗過程中和上市后的藥物安全監(jiān)測和報告機制����。通過實時監(jiān)測���,及時發(fā)現(xiàn)并應對藥物安全問題����,保障患者的安全與權(quán)益���。加強藥物風險評估與控制�,通過分析產(chǎn)品生命周期中可能存在的風險,建立風險評估和管理控制體系���,及時識別潛在的質(zhì)量風險���,并采取措施加以預防和控制[11]。
6 討論與小結(jié)
本文主要探析了跨國醫(yī)藥公司在實施ICH 指南時面臨的挑戰(zhàn)�,包括ICH 指南更新較快、國際監(jiān)管要求存在差異���、跨國醫(yī)藥公司內(nèi)部調(diào)整管理困難等���。針對這些挑戰(zhàn),筆者提出了相關(guān)對策思考�,如加強多方溝通以掌握ICH 更新的前沿動態(tài)、優(yōu)化內(nèi)部組織結(jié)構(gòu)并建立標準化流程等���,以期幫助跨國醫(yī)藥公司更好地應對ICH 指南的更新�,不斷提高產(chǎn)品質(zhì)量和合規(guī)水平���。同時����,本文為跨國醫(yī)藥公司建立質(zhì)量管理通用標準提供了參考,以期幫助跨國醫(yī)藥公司更好地實施ICH 指南����。需要說明的是,由于ICH 指南研究范圍廣泛且內(nèi)容深入���,跨國醫(yī)藥公司受國際藥品監(jiān)管環(huán)境變化的影響較大����,本文的分析不足以涵蓋全部要點���,有待進一步完善����。未來�,隨著全球藥品監(jiān)管趨于標準化與統(tǒng)一化,跨國醫(yī)藥公司需要不斷優(yōu)化和完善自身管理體系和運營策略���,加強合作伙伴關(guān)系和溝通交流,推動數(shù)字化轉(zhuǎn)型�,提高創(chuàng)新能力和管理水平����,以更好地適應國際藥品監(jiān)管環(huán)境的變化����,保持競爭優(yōu)勢,應對新的機遇與挑戰(zhàn)���。