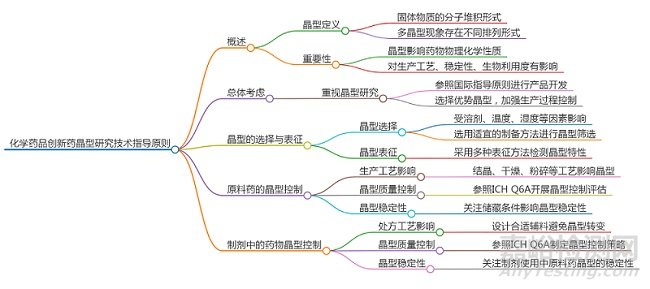
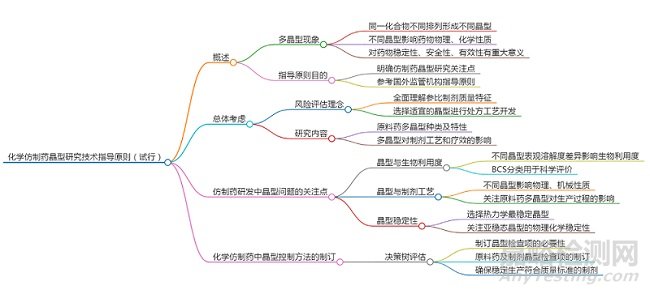
藥物晶型研究是藥物研發(fā)與質(zhì)量控制中的關(guān)鍵環(huán)節(jié)�,直接影響藥物的理化性質(zhì)�、穩(wěn)定性、溶出行為、生物利用度及最終產(chǎn)品的安全性與有效性。2025年9月23日�,CDE發(fā)布了《化學(xué)藥品創(chuàng)新藥晶型研究技術(shù)指導(dǎo)原則(征求意見(jiàn)稿)》(以下簡(jiǎn)稱“創(chuàng)新藥指南”),而《化學(xué)仿制藥晶型研究技術(shù)指導(dǎo)原則(試行)》(以下簡(jiǎn)稱“仿制藥指南”)已于2021年12月23日發(fā)布���,兩者在目標(biāo)藥物類型�、研究思路�、控制策略等方面存在顯著差異�����,同時(shí)也共享若干基本科學(xué)原則與方法�����。本文將對(duì)這兩份指南進(jìn)行系統(tǒng)對(duì)比�����,從總體思路、晶型選擇�����、表征方法�����、質(zhì)量控制及穩(wěn)定性研究等多個(gè)維度展開(kāi)分析,以期為藥物研發(fā)人員提供清晰的指導(dǎo)理解與實(shí)踐參考���。
01總體思路
創(chuàng)新藥指南側(cè)重于藥物研發(fā)的全過(guò)程���,強(qiáng)調(diào)在藥物生命周期中持續(xù)進(jìn)行晶型研究�����,從早期篩選到上市申請(qǐng)各階段均需系統(tǒng)考察晶型的影響�。其目標(biāo)是通過(guò)科學(xué)的風(fēng)險(xiǎn)管理和質(zhì)量源于設(shè)計(jì)(QbD)理念�,確保所選晶型在工藝放大、穩(wěn)定性�、制劑性能等方面的穩(wěn)健性���。指南多次引用ICH Q6A�、Q8���、Q9、Q11等國(guó)際技術(shù)指南�,體現(xiàn)出對(duì)國(guó)際化標(biāo)準(zhǔn)的重視���,也反映了創(chuàng)新藥研發(fā)中“未知風(fēng)險(xiǎn)多�����、需前瞻控制”的特點(diǎn)。
仿制藥指南則明確以參比制劑為對(duì)照�����,聚焦于如何通過(guò)晶型研究實(shí)現(xiàn)與參比制劑的生物等效(BE)和質(zhì)量一致�。其研究思路更具針對(duì)性�,強(qiáng)調(diào)對(duì)已有晶型信息的利用(如文獻(xiàn)、專利�、藥典)�,并通過(guò)風(fēng)險(xiǎn)評(píng)估決定是否需要進(jìn)行晶型控制�����。指南中引入“決策樹(shù)”工具�����,幫助申請(qǐng)人在不同情景下制定合理的控制策略���,體現(xiàn)出仿制藥研發(fā)中“以終為始���、效率優(yōu)先”的務(wù)實(shí)導(dǎo)向。
02晶型選擇
在晶型選擇上���,兩份指南的根本區(qū)別在于“有無(wú)參比制劑”這一前提。
創(chuàng)新藥指南指出�����,應(yīng)通過(guò)系統(tǒng)的晶型篩選�����,考察不同晶型的溶解度���、穩(wěn)定性、引濕性等理化性質(zhì)�,結(jié)合劑型特點(diǎn)與臨床需求�����,選擇“優(yōu)勢(shì)晶型”�����。通常推薦使用熱力學(xué)最穩(wěn)定的晶型���,以降低生產(chǎn)和貯存過(guò)程中的轉(zhuǎn)晶風(fēng)險(xiǎn)�。若選擇亞穩(wěn)態(tài)晶型或無(wú)定型���,則需加強(qiáng)穩(wěn)定性研究并制定相應(yīng)的控制策略。
仿制藥指南則明確���,原則上應(yīng)選擇與參比制劑相同的晶型�。只有在有充分?jǐn)?shù)據(jù)證明不同晶型仍能保證生物
等效且穩(wěn)定性可控時(shí)�,才可考慮使用其他晶型。這一選擇不僅基于科學(xué)合理性�,也涉及專利規(guī)避與市場(chǎng)競(jìng)爭(zhēng)的實(shí)務(wù)考量�。指南特別指出���,若參比制劑使用穩(wěn)定晶型���,且仿制藥也采用相同晶型,通常無(wú)需在制劑標(biāo)準(zhǔn)中設(shè)立晶型檢查項(xiàng)���。
03表征方法
兩份指南在晶型表征方法上高度一致�����,均列舉了單晶X射線衍射�����、粉末X射線衍射(PXRD)�、熱分析(DSC���、TGA)�����、光譜法(IR�、Raman�����、ssNMR)等常用技術(shù)���。這些方法從不同維度反映晶體的結(jié)構(gòu)、熱行為與分子環(huán)境�����,共同構(gòu)成晶型確證的多維證據(jù)鏈。
創(chuàng)新藥指南更強(qiáng)調(diào)表征的系統(tǒng)性與代表性���,要求結(jié)合工藝特點(diǎn)選擇具有代表性的樣品進(jìn)行表征�,并在方法開(kāi)發(fā)中注重專屬性與可靠性。仿制藥指南則更關(guān)注方法的適用性與可轉(zhuǎn)移性���,尤其在參考藥典方法時(shí),需驗(yàn)證其是否適用于目標(biāo)晶型的控制�。兩者均指出�����,單一方法往往不足以全面表征晶型�,需多種方法聯(lián)用�。
04質(zhì)量控制
在原料藥層面���,兩份指南均強(qiáng)調(diào)工藝參數(shù)(如結(jié)晶���、干燥�、粉碎)對(duì)晶型的影響���,并要求建立相應(yīng)的控制策略。創(chuàng)新藥指南更注重工藝開(kāi)發(fā)階段的系統(tǒng)研究,如晶種的使用���、干燥方式的選擇�����、粉碎參數(shù)的優(yōu)化等,以保障工藝的穩(wěn)健性�����。仿制藥指南則更多關(guān)注是否需要在質(zhì)量標(biāo)準(zhǔn)中設(shè)立晶型檢查項(xiàng)���,并借助BCS分類判斷晶型差異對(duì)生物等效性的潛在影響�����。
在制劑層面���,創(chuàng)新藥指南要求全面考察處方工藝(如輔料選擇�、工藝參數(shù))對(duì)晶型穩(wěn)定性的影響,并在穩(wěn)定性研究中持續(xù)監(jiān)測(cè)晶型變化���。仿制藥指南則強(qiáng)調(diào)�����,若制劑性能檢測(cè)(如溶出度)能有效反映晶型變化,則可替代晶型檢查項(xiàng)�����,這一做法在效率與成本控制上更具優(yōu)勢(shì)�。
05穩(wěn)定性研究
兩份指南均重視晶型在貯存與使用過(guò)程中的穩(wěn)定性���,要求根據(jù)晶型轉(zhuǎn)變風(fēng)險(xiǎn)選擇合適的包裝與貯藏條件。創(chuàng)新藥指南更強(qiáng)調(diào)在臨床試驗(yàn)期間藥學(xué)變更時(shí)���,需評(píng)估變更對(duì)晶型的潛在影響�,體現(xiàn)其“動(dòng)態(tài)管控”的特點(diǎn)�����。仿制藥指南則通過(guò)決策樹(shù)工具�,將穩(wěn)定性風(fēng)險(xiǎn)與質(zhì)量控制策略直接掛鉤���,使研究更具可操作性�����。
06總結(jié)
總體而言,創(chuàng)新藥與仿制藥在晶型研究上的根本區(qū)別在于:創(chuàng)新藥是“從無(wú)到有”的晶型探索與優(yōu)化過(guò)程�,注重全面性與前瞻性;仿制藥是“從有到仿”的晶型對(duì)標(biāo)與驗(yàn)證過(guò)程,注重效率與一致性。
盡管如此�����,兩者在科學(xué)基礎(chǔ)���、表征方法、質(zhì)量控制理念上高度一致�����,均體現(xiàn)了以風(fēng)險(xiǎn)為基礎(chǔ)、以質(zhì)量為核心的研究思路���。隨著藥物研發(fā)模式的多樣化(如改良型新藥、505(b)(2)類申報(bào)等),兩類指南的交叉參考價(jià)值日益凸顯。未來(lái)�����,隨著晶體工程學(xué)���、原位分析與建模預(yù)測(cè)技術(shù)的發(fā)展,晶型研究將更加精準(zhǔn)���、高效,也為創(chuàng)新藥與仿制藥的晶型控制策略帶來(lái)更多共性提升空間�����。
參考文獻(xiàn)
[1] 國(guó)家藥品監(jiān)督管理局藥品審評(píng)中心�����?����!痘瘜W(xué)藥品創(chuàng)新藥晶型研究技術(shù)指導(dǎo)原則(征求意見(jiàn)稿)》���,2025年9月�����。
[2] 國(guó)家藥品監(jiān)督管理局�����,《化學(xué)仿制藥晶型研究技術(shù)指導(dǎo)原則(試行)》���,2022年1月�。