本文評估分析人血白蛋白與其現(xiàn)用內(nèi)包裝系統(tǒng)(中硼硅玻璃模制注射劑瓶和注射液用鹵化丁基橡膠塞)的浸出物風(fēng)險。通過設(shè)計浸出試驗,依據(jù)相關(guān)指導(dǎo)原則���、產(chǎn)品工藝等要求���,評估出浸出物試驗需測定的元素及有機物,并采用ICP-MS�、ICP-OES測定0天���、加速3月正置和倒置的3批樣品中的元素�,采用HS-GC-MS�、GC-MS測定0天�、加速3月倒置的2批樣品中的有機物���,同時通過SEM掃描電鏡觀察樣品的玻璃內(nèi)表面情況。結(jié)果顯示經(jīng)評估確定需檢測元素19種(Pb�、Co����、Cd�、As���、Li�、Sb�、Ba、Fe�、Zn����、Cr、Si���、B����、Al�、Mn�、Ti、Zr�、Mo、W和Pt)�、有機物2種(抗氧劑264和甲基環(huán)戊烷)����。檢測結(jié)果表明�,各檢測時間點樣品的浸出物元素、有機物測定結(jié)果均小于ICH Q3D和指導(dǎo)原則規(guī)定的限值�,玻璃內(nèi)表面未觀察到侵蝕或脫片現(xiàn)象。人血白蛋白現(xiàn)用藥液內(nèi)包材系統(tǒng)對藥物質(zhì)量無影響�,滿足人血白蛋白對包裝材料浸出物要求,能夠保障產(chǎn)品安全����、有效。
人血白蛋白(Human Albumin)系由健康人血漿中提取���、分離和純化制備后經(jīng)病毒滅活可直接靜脈注射的血液制品����,因其可增加血容量維持膠體滲透壓���,也可作為氮源提供營養(yǎng)供給等藥理作用���,在臨床上可用于低血容量的緊急治療、肝硬化和腎病引起的水腫或腹水等病癥 [1-4]����。目前行業(yè)普遍采用中硼硅模制注射劑瓶與注射液用鹵化丁基橡膠塞作為人血白蛋白常用的內(nèi)包裝材料系統(tǒng)����。根據(jù)國家藥品監(jiān)督管理局發(fā)布的《化學(xué)藥品與彈性體密封件相容性研究技術(shù)指導(dǎo)原則》����、《化學(xué)藥品注射劑與藥用玻璃包裝容器相容性研究技術(shù)指導(dǎo)原則》[5-6] 的要求,已有文獻(xiàn)報道了該制劑與包裝材料的相容性研究 [7]����,雖然可提取物研究結(jié)果顯示無需對檢出物質(zhì)進(jìn)行目標(biāo)浸出物專項考察�,但內(nèi)包裝組件與藥物制劑實際貯存過程中可能發(fā)生浸出并對藥品質(zhì)量產(chǎn)生一定影響,且包裝材料的不穩(wěn)定分解產(chǎn)物�、反應(yīng)產(chǎn)物等都存在浸出風(fēng)險 [8-9]。因此�,浸出物雜質(zhì)對于患者用藥安全引入的整體風(fēng)險較高。
為確保實際生產(chǎn)條件下浸出物水平始終處于限值內(nèi)���,且不會對藥品質(zhì)量屬性產(chǎn)生不良影響���,基于現(xiàn)行法規(guī)及指導(dǎo)原則、產(chǎn)品特性及生產(chǎn)工藝等因素����,設(shè)計開展浸出試驗����,旨在完善人血白蛋白藥液與內(nèi)包裝材料間的相容性研究內(nèi)容數(shù)據(jù)體系����,為保障最終上市產(chǎn)品的安全、有效�、質(zhì)量可控提供科學(xué)依據(jù)。
Part1材料與方法
1.1材料與設(shè)備
人血白蛋白(規(guī)格:10 g / 50 mL����,國藥集團蘭州生物制藥有限公司,批號:202108031���、202108032�、202109033)�,50 mL 中硼硅玻璃模制注射劑瓶(簡稱:注射劑瓶)(山東藥用玻璃股份有限公司,批號:20201024)���,φ20 注射液用鹵化丁基橡膠塞(簡稱:膠塞)(江蘇省華蘭藥用新材料股份有限公司�,批號:200402268-10)�,鋁塑組合蓋(簡稱:鋁蓋���,輔助密封)(上海久正醫(yī)用包裝材料有限公司,批號:20120815)�,甲醇、乙醇���、無水磷酸氫二鈉�、氯化鉀均為分析純����,水為純化水。
ICP-MS 電感耦合等離子體質(zhì)譜儀(型號 7900���,Agilent 公司)���、ICPMS 電感耦合等離子體質(zhì)譜儀(型號NexION1000G����,PerkinElmer 公司)、石墨消解儀(型號 Digiblock ED54���,北京萊伯泰科(Labtech)公司)�、超純水儀(型號 Unique-R40,廈門銳思捷)����、ICP - OES 電感耦合等離子體發(fā)射光譜 儀( 型 號 AVIO 200,PerkinElmer公司)�、SEM 掃描電子顯微鏡(型號Sigma500,Zeiss 公司)����。
1.2試驗方法
本文依據(jù)《化學(xué)藥品與彈性體密封件相容性研究技術(shù)指導(dǎo)原則》、《化學(xué)藥品注射劑與藥用玻璃包裝容器相容性研究技術(shù)指導(dǎo)原則》的相關(guān)要求����,結(jié)合產(chǎn)品信息、產(chǎn)品生產(chǎn)工藝評估浸出物測定項目����,設(shè)計加速試驗,檢測人血白蛋白產(chǎn)品的浸出元素�、有機物,并通過SEM 掃描電鏡觀察玻璃瓶內(nèi)表面����,全面研究分析人血白蛋白藥液與內(nèi)包裝材料間的浸出物。
1.2.1測定項目評估
人血白蛋白浸出物需測定元素及有機物選擇依據(jù)見表 1。經(jīng)評估最終確定浸出物測定元素有 19 種���,分別是Pb�、Co���、Cd�、As����、Li、Sb���、Ba����、Fe���、Zn�、Cr�、Si�、B、Al、Mn�、Ti、Zr���、Mo�、W 和 Pt����,浸出物測定有機物有 2 種,分別是抗氧劑 264(2,6 -二叔丁基對甲酚�,別稱 BHT)和甲基環(huán)戊烷。
表 1 浸出物測定選擇評估表
1.2.2浸出物試驗樣品制備
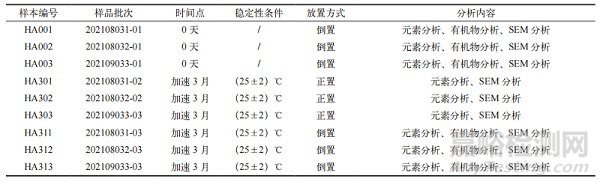
選擇正式內(nèi)包裝系統(tǒng)(即 50 mL中硼硅玻璃模制注射劑瓶�、φ20 注射液用鹵化丁基橡膠塞及 φ20 鋁塑組合蓋)的三批人血白蛋白產(chǎn)品(批號:202108031、202108032�、202109033)各三組,按照表 2 中的設(shè)計條件制備浸出物試驗檢測樣品����。
表 2 浸出物試驗樣品信息
1.2.3標(biāo)準(zhǔn)曲線溶液的制備
1.2.3.1 元素標(biāo)準(zhǔn)曲線溶液的制備
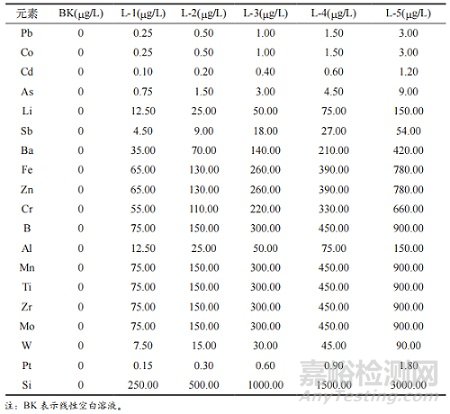
量取純化水 2 250 mL 于聚丙烯塑料試劑瓶中,緩慢加入 250 mL 硝酸���,搖勻后作為稀釋劑���。分別量取適量不同標(biāo)準(zhǔn)物質(zhì)溶液于 50 mL 塑料量瓶中,用稀釋劑梯度稀釋至刻度,搖勻轉(zhuǎn)移至塑料離心管����,配制成不同物質(zhì)的標(biāo)準(zhǔn)曲線溶液。標(biāo)準(zhǔn)曲線溶液中各元素的濃度梯度見表 3���。
表 3 標(biāo)準(zhǔn)曲線溶液中各元素濃度
1.2.3.2 抗氧劑 264 標(biāo)準(zhǔn)曲線溶液的制備
精確稱取抗氧劑 264 標(biāo)準(zhǔn)物質(zhì)268.05 mg 于 10 mL 量瓶中���,用乙腈稀釋至刻度后搖勻,作為抗氧劑 264 儲備液�。量取抗氧劑 264 儲備液 18.7 μL 于10 mL 量瓶中,用乙腈稀釋至刻度后搖勻�,得到抗氧劑 264 濃度為 50.0 μg/mL 標(biāo)準(zhǔn)物質(zhì)溶液。分別量取不同抗氧劑 264 標(biāo)準(zhǔn)物質(zhì)溶液于 10 mL 量瓶中�,用正己烷稀釋至刻度后搖勻,取約 1 mL 溶液于進(jìn)樣小瓶���,配制成標(biāo)準(zhǔn)曲線溶液���,抗氧劑 264 標(biāo)準(zhǔn)物質(zhì)濃度依次為 60.0、120.0�、200.0、300.0����、500.0 μg/L。
1.2.3.3 甲基環(huán)戊烷標(biāo)準(zhǔn)曲線溶液的制備
精確稱取甲基環(huán)戊烷標(biāo)準(zhǔn)物質(zhì)151.515 mg 于 10 mL 量瓶中���,用二氯甲烷溶解后稀釋至刻度后搖勻����,作為甲基環(huán)戊烷儲備液����。量取甲基環(huán)戊烷儲備液 66.0 μL 于 10 mL 量瓶中,用 DMF稀釋至刻度后搖勻���,得到甲基環(huán)戊烷濃度為 100.0 μg/mL 的標(biāo)準(zhǔn)物質(zhì)溶液�。分別量取不同甲基環(huán)戊烷標(biāo)準(zhǔn)物質(zhì)溶液于10 mL 量瓶���,加入純化水 500.0 μL����,用稀釋劑稀釋至刻度后搖勻���,配制成標(biāo)準(zhǔn)曲線溶液����,甲基環(huán)戊烷標(biāo)準(zhǔn)物質(zhì)濃度依次為 90.0、150.0�、300.0、450.0����、600.0 μg/L。
1.2.4樣品溶液的制備
1.2.4.1 元素測定樣品溶液的制備
量取樣品藥液 3.100 mL 于 50 mL聚丙烯消解管中�,加入硝酸 5.000 mL。將消解管置于石墨消解儀上�,120℃消解 60 min,至溶液澄清����。待溶液冷卻至室溫后,將溶液轉(zhuǎn)移至 50 mL 塑料量瓶中����,用純化水沖洗消解管內(nèi)壁 3 次,洗液一并轉(zhuǎn)移至同一個塑料量瓶中�,用純化水稀釋至刻度后搖勻,取不含樣品的空容器作為空白試驗���。
1.2.4.2 有機物測定樣品溶液的制備
抗氧劑 264 樣品溶液:量取樣品藥液 500.0μL 于 20mL 樣品瓶中���,加入正己烷 10.00mL�,振搖 30s 后靜置2min���,取上層溶液約 1mL 于進(jìn)樣小瓶,純化水作為空白溶液���。
甲基環(huán)戊烷樣品溶液:量取樣品藥液 500.0μL 于 10mL 量瓶中�,加入稀釋劑稀釋至刻度����,量取 1.000mL 于頂空瓶中,純化水作為空白溶液���。
1.2.4.3 SEM 電鏡分析樣品的制備
選取浸出物測定樣品的注射劑瓶���,參考王亞麗等 [6] 玻璃內(nèi)表面脫片分析樣品制備方法 1.2.2.2 制備電鏡分析樣品。
1.3檢定方法
1.3.1元素測定方法
采用 ICP-MS 對樣品中 Pb���、Co�、Cd���、As����、Li、Sb���、Ba�、Fe���、Zn����、Cr�、B、Al����、Mn、Ti����、Zr、Mo����、W 和 Pt 元 素進(jìn)行檢測�,采用 ICP-OES 對 Si 元素進(jìn)行檢測���。
1.3.2有機物測定方法
采用 HS-GC-MS�、GC-MS 對樣品中抗氧劑 264���、甲基環(huán)戊烷進(jìn)行檢測。1.3.3浸出物的結(jié)果分析方法
為定量限(LOQ):標(biāo)準(zhǔn)曲線溶液最低濃度 L-1 測定結(jié)果作為溶液定量限(LOQ)(μg/L)���。根據(jù)下列公式計算定量限(μg/ 瓶):定量限(μg/ 瓶)= 定量限(μg/L)× 最終體積(mL)÷ 取樣體積(μL)× 裝量體積(mL/ 瓶)�;
限值:元素����、有機物限值結(jié)果參考 ICH Q3D 中推薦的每日允許暴露量(Permitted Daily Exposure,PDE)[13],結(jié)合藥包材相容性研究中安全性評估方法 [14]�,利用每日允許暴露量 PDE(µg/d)與人血白蛋白每日最大用藥量(6 瓶 /d)的比值,得到限值(μg/ 瓶)���。對無推薦PDE 的元素���,按照 ICH Q3D 中限值最高的 1 500 µg/ 天進(jìn)行初步評價���,限值計算公式如下:限 值(µg/ 瓶 )=PDE(µg/d)÷MDI(瓶 /d);
SEM 電鏡分析方法:樣品表面噴金后�,采用 SEM 電鏡在低倍數(shù)條件(200 ~ 2 000)下進(jìn)行初步篩選,再在 8 000 倍條件下進(jìn)行觀察分析���。
Part2結(jié)果與分析
2.1元素測定結(jié)果
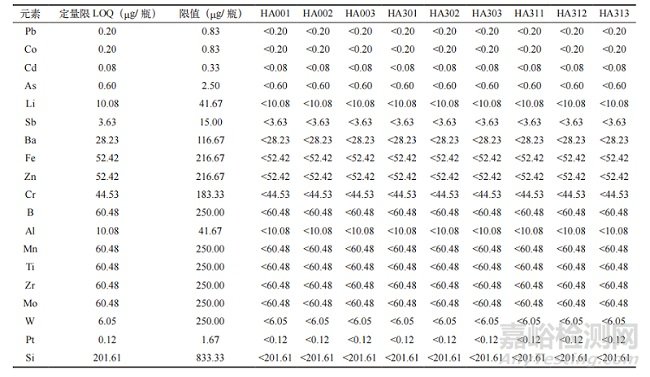
將樣品按照不同條件處理后����,得到元素測定結(jié)果如表 4 所示����。所有元素檢測結(jié)果均低于定量限,且元素檢測結(jié)果均小于限值����。根據(jù)《化學(xué)藥品注射劑與藥用玻璃包裝容器相容性研究技術(shù)指導(dǎo)原則》規(guī)定,浸出物含量低于限值時����,可認(rèn)為浸出物的量不會改變藥品的安全性,對患者的安全性風(fēng)險小�,若浸出物的含量高于限值,則認(rèn)為包裝容器與藥品不具有相容性,建議更換包裝材料����。參考 ICH Q3D 包裝系統(tǒng)中浸出的元素雜質(zhì)識別和風(fēng)險評估建議,如當(dāng)包裝系統(tǒng)組成的綜述資料表明包裝系統(tǒng)不含元素雜質(zhì)時����,無需進(jìn)行額外的風(fēng)險評估。王亞麗等 [7] 已通過模擬加速試驗檢測Si����、B 和 Al 三種元素的含量,結(jié)果顯示三種元素含量穩(wěn)定并未出現(xiàn)數(shù)量級的增長趨勢�。本試驗浸出物元素測定結(jié)果均小于定量限和限值,說明浸出物不會影響藥品的安全性和有效性�,不對人體健康造成威脅�。
表 4 元素測定結(jié)果
2.2有機物測定結(jié)果
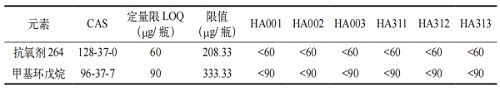
對 0 月、加速 3 月倒置樣品測定抗氧劑 264���、甲基環(huán)戊烷����,檢測結(jié)果見表 5�。有研究表明 [15],抗氧劑 264 分子量較小,易遷移���,藥液中含量過量會直接損害人體肝肺功能���,促進(jìn)腫瘤發(fā)生的可能。按照《化學(xué)藥品與彈性體密封件相容性研究技術(shù)指導(dǎo)原則》要求����,如果浸出物含量低于限值時,可認(rèn)為浸出物的水平對人體產(chǎn)生的風(fēng)險是可以接受的����;如果浸出物的含量高于限值,則認(rèn)為浸出物的水平所產(chǎn)生的風(fēng)險是不可以接受的�。有機物測定結(jié)果顯示,抗氧劑 264 和甲基環(huán)戊烷測定結(jié)果均小于定量限����,表明現(xiàn)使用的內(nèi)包材與藥品相容性良好,藥品的浸出物對人體產(chǎn)生的風(fēng)險可接受����。
表 5 有機物測定結(jié)果
2.3SEM 電鏡結(jié)果
中硼硅玻璃主要成分為 SiO2,基本骨架由 [SiO4] 四面體構(gòu)成����,注射劑瓶接觸中性和酸性溶液時�,會導(dǎo)致堿性金屬離子溶出并釋放出氫氧根離子����;在堿性溶液中,玻璃骨架易被破壞����,超出限度后可能會析出微粒,這些相互作用均會導(dǎo)致玻璃骨架疏松�,玻璃內(nèi)表面出現(xiàn)薄片剝落,形成侵蝕脫片現(xiàn)象 [16]����。參照《化學(xué)藥品注射劑與藥用玻璃包裝容器相容性研究技術(shù)指導(dǎo)原則》要求,藥品對玻璃內(nèi)表面的影響結(jié)果評估過程中�,如有脫屑、微?;蚯治g痕跡���,則表示藥品質(zhì)量已經(jīng)產(chǎn)生顯著影響����。圖 1 顯示人血白蛋白浸出物測定樣品 0 月和 3月的 SEM 電鏡圖,通過掃描電鏡對不同樣品注射劑瓶的瓶肩����、瓶身和瓶底進(jìn)行觀察,未發(fā)現(xiàn)有脫片���、侵蝕或微粒情況���,僅觀察到黑灰色背景,表明不同試驗條件下玻璃內(nèi)表面無侵蝕脫片現(xiàn)象���。
圖 1 人血白蛋白浸出物測定樣品 SEM 電鏡圖
Part3討論
近年來�,隨著社會各界對藥品質(zhì)量安全性和有效性的高度關(guān)注�,藥品與內(nèi)包裝材料的相容性評價研究工作也日益受到重視。在不同劑型的藥品中����,注射液體制劑由于與包裝材料直接接觸,更容易促進(jìn)浸出物的溶出�。浸出物的研究能夠進(jìn)一步識別和量化藥物制劑在實際使用過程在從包裝材料中遷移出的物質(zhì),從而反映真實條件下包裝材料對藥品質(zhì)量的影響 [17]����。人血白蛋白源于健康人血液分離提取的血液制品���,藥理作用廣泛,目前我國約 70% 人血白蛋白來源于進(jìn)口�,臨床用藥需求較大,呈穩(wěn)態(tài)緩慢增長趨勢 [18-20]�,深入探究人血白蛋白浸出物的風(fēng)險至關(guān)重要。參照 ICH Q3D(R2)[11] 指導(dǎo)原則指出“本指導(dǎo)原則不適用于植物藥����、放射性藥物、疫苗���、細(xì)胞代謝產(chǎn)物���、DNA 產(chǎn)品、過敏原提取物���、細(xì)胞����、全血����、血細(xì)胞成份或包括血漿及血漿衍生物在內(nèi)的血液衍生物、非體循環(huán)透析液����、以及為了治療作用而特意添加到藥品中的元素”。因此����,本試驗在浸出物有機物測定評估過程中,未依據(jù) ICH Q3D(R2)中規(guī)定的注射且非有意添加的 10 種元素(Cd�、Pb、As�、Hg、Co���、V���、Ni、Li���、Sb 和Cu)考察���。比對 ICH Q3D(R2)規(guī)定和評估得到的浸出物元素,僅 V 元素未進(jìn)行測定分析���。參考王亞麗等 [7] 人血白蛋白和內(nèi)包裝材料可提取物研究結(jié)果顯示����,V 元素檢測結(jié)果≤ 0,因此能夠證明人血白蛋白現(xiàn)用藥液內(nèi)包材系統(tǒng)對藥物質(zhì)量無影響�。
參考文獻(xiàn)
[1] 倪道明 . 血液制品 [M]. 北京 : 人民衛(wèi)生出版社 ,2013:91.
[2] 竇 姿 , 趙小潔 , 張齊明 , 等 . 人血白蛋白生產(chǎn)過程中多聚體含量的檢測 [J]. 中國輸血雜志 ,2021,34(08):909-913.
[3] L I U M B R U N O GM,BENNARDELLO F,LATTANZIOA,et al. Recommendations for the use of albumin and immunoglobulins[J].Blood Transfus,2009,7(3):216-234.
[4] 邊原 , 陳岷 , 杜姍 , 等 . 第二批國家重點監(jiān)控藥品合理使用規(guī)范 [J].中國藥房 ,2023,34(20):2433-2453.
[5] 原國家食品藥品監(jiān)督管理局 . 化學(xué)藥品注射劑與藥用玻璃包裝容器相容性研究技術(shù)指導(dǎo)原則(試行)