將于2026年3月1日施行的《中藥生產(chǎn)監(jiān)督管理專門規(guī)定》中明確指出:持有人�����、中藥生產(chǎn)企業(yè)應(yīng)當(dāng)對(duì)所采購(gòu)的中藥材開(kāi)展質(zhì)量評(píng)估��,保證基原準(zhǔn)確、來(lái)源清楚��。對(duì)于使用道地中藥材��、使用符合中藥材GAP要求的中藥材或者直接從產(chǎn)地中藥材生產(chǎn)企業(yè)采購(gòu)中藥材的,經(jīng)審核可以引用該中藥材基原鑒定資料��,但應(yīng)注明來(lái)源�����。這意味著���,基原鑒定將成為中藥生產(chǎn)必不可少的強(qiáng)制環(huán)節(jié)。持有人/生產(chǎn)企業(yè)應(yīng)當(dāng)深入學(xué)習(xí)“基原鑒定”的相關(guān)法規(guī)要求��,以保證“基原鑒定”的合規(guī)性��。
核心要求1:鑒定單位資質(zhì)
基原鑒定機(jī)構(gòu)應(yīng)具備中國(guó)境內(nèi)植(動(dòng))物基原鑒定資質(zhì)�����。滿足下列情況之一即可:
1) 相關(guān)單位該檢測(cè)項(xiàng)目應(yīng)獲得CNAS實(shí)驗(yàn)室認(rèn)可:持有人/生產(chǎn)企業(yè)可登錄中國(guó)合格評(píng)定國(guó)家認(rèn)可委員會(huì)網(wǎng)站(https://www.cnas.org.cn/)核實(shí)機(jī)構(gòu)的資質(zhì)��。
2) 獲得省部級(jí)相關(guān)行政主管部門認(rèn)可:獲得地方藥監(jiān)局���、公安部�����、民政部等省部級(jí)行業(yè)行政主管部門認(rèn)可,其資質(zhì)證明由具體認(rèn)證單位出具。
核心要求2:鑒定報(bào)告內(nèi)容規(guī)范
不同單位出具的基原鑒定報(bào)告內(nèi)容格式存在差異,但至少應(yīng)涵蓋以下內(nèi)容:
1) 樣本(標(biāo)本)基本信息:包括標(biāo)本名稱���、送樣單位��、產(chǎn)地、樣本(標(biāo)本)保存地點(diǎn)及鑒定日期等�����。
2) 鑒定技術(shù)相關(guān)信息:應(yīng)明確鑒定依據(jù)���、技術(shù)方法��、樣本關(guān)鍵形態(tài)特征及鑒定結(jié)論�����,必要時(shí)提供分類檢索表��。
3) 報(bào)告的有效性憑證:鑒定人需對(duì)報(bào)告簽字并加蓋鑒定機(jī)構(gòu)公章,附標(biāo)本圖片及必要的關(guān)鍵信息。
核心要求3:鑒定手段
基原鑒定手段應(yīng)為“傳統(tǒng)+現(xiàn)代”的融合�����,以傳統(tǒng)的分類學(xué)方法為基礎(chǔ)���,現(xiàn)代的高技術(shù)手段(如:圖像識(shí)別技術(shù)��、DNA分子鑒定技術(shù))為補(bǔ)充��。因?yàn)楝F(xiàn)代鑒定技術(shù)雖然強(qiáng)大,但每種鑒定手段都有其局限性��,分類學(xué)作為中藥材基原鑒定的基石�����,仍然是鑒定的權(quán)威依據(jù)。沒(méi)有進(jìn)行分類學(xué)鑒定的基原鑒定��,其鑒定依據(jù)被認(rèn)為是不充分的,無(wú)法支持鑒定結(jié)論��。
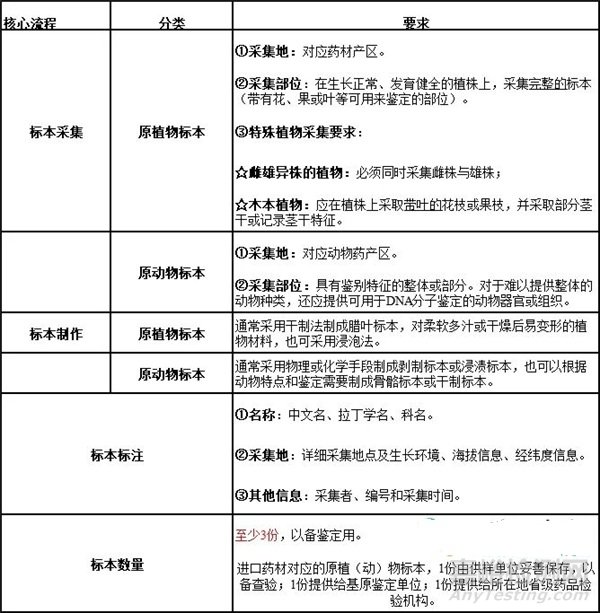
核心要求4:用于鑒定的樣本及相關(guān)材料
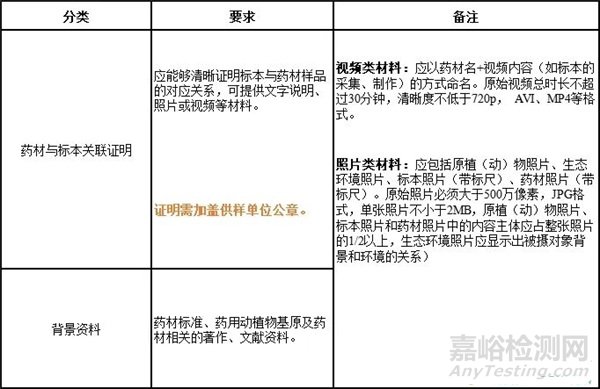
規(guī)范化的標(biāo)本制作、完整的證明材料是基原鑒定結(jié)果可靠性的基礎(chǔ)�����。
1) 標(biāo)本的規(guī)范性要求
2) 藥材的規(guī)范性要求
3) 證明材料的要求
參考文獻(xiàn):
【1】《中藥生產(chǎn)監(jiān)督管理專門規(guī)定》
【2】《藥材基原鑒定技術(shù)要求(征求意見(jiàn)稿)》