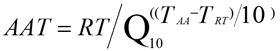醫(yī)療器械的性能直接關系到患者的健康與安全,因此���,穩(wěn)定性研究不僅是產品設計開發(fā)階段的關鍵環(huán)節(jié)���,也是醫(yī)療器械注冊審評中的重點關注項。
通常���,醫(yī)療器械的穩(wěn)定性研究涵蓋三個方面:貨架有效期、使用穩(wěn)定性和運輸穩(wěn)定性���。本公眾號將分三期為大家逐一解析�����。
本期聚焦于貨架有效期的研究方法與核心要點�����。
No.1 貨架有效期的定義
醫(yī)療器械貨架有效期是指保證醫(yī)療器械終產品正常發(fā)揮預期功能的期限�,一旦超過醫(yī)療器械的貨架有效期,就意味著該器械可能不再滿足已知的性能指標�����,發(fā)揮預期功能���,在使用中具有潛在的風險�����。
No.2 產品的貨架有效期的影響因素
影響貨架有效期的因素有很多���,這些因素主要分為內部和外部兩大類:
1. 內部因素
原材料或組件自身的老化、降解�。
各原材料或組件之間的相互反應或遷移。
初級包裝材料的化學特性及其與產品的相容性���。
無菌包裝系統(tǒng)的微生物屏障性能隨時間的變化�。
2. 外部因素
貯存環(huán)境的溫度���、濕度�、光照���、氣壓等���。
運輸過程中的震動、沖擊���、擠壓等機械應力�。
因此�����,在產品說明書中明確儲存條件至關重要���,尤其是對于溫濕度敏感或含有活性成分(如含藥器械)的產品�����。
No.3 貨架研究研究的方法
貨架有效期的研究方法通常有:加速老化穩(wěn)定性試驗和實時老化穩(wěn)定性試驗�����。
1. 加速老化穩(wěn)定性試驗
加速老化試驗是通過提高環(huán)境應力(如溫度)���,在較短時間內模擬產品長期老化效果的研究方法。
該方法基于阿列紐斯(Arrhenius)�,其核心假設是:材料化學反應速率隨溫度升高而加快。通常認為���,溫度每升高10℃�����,反應速率約提高一倍(即Q10=2)�?��;诖?����,得到簡化的加速老化公式:
AAT:加速老化時間�;
RT:實時老化時間�;
Q10:溫度升高或降低10℃的老化系數(shù)(一般取2)�;
TAA:加速老化溫度���;
TRT:預設的實際貯存溫度�。
在醫(yī)療器械注冊申報時�����,通??上忍峤患铀倮匣囼瀳蟾孀鳛橹С帧?/span>
2. 實時穩(wěn)定性試驗
這是最直接�����、最可靠的研究方法���。它將樣品置于規(guī)定的實際貯存條件下�����,在整個預設的有效期內定期進行監(jiān)測和測試�。
實時老化試驗的條件應盡可能模擬真實的儲存�、運輸環(huán)境。若產品有專用標準或指導文件�,應優(yōu)先遵循其規(guī)定。
雖然產品注冊申報時可能無法完成全部的實時老化研究���,但必須在研究啟動時�,就同步制定好實時老化與加速老化的方案�����,并嚴格按照方案中的時間點進行檢測和記錄�����。
3. 老化后的測試項目
無論采用哪種老化方法�,試驗結束后都需要對產品進行系統(tǒng)評估,主要包括:
1). 產品自身性能測試:依據(jù)《成品檢驗規(guī)程》進行全項目檢驗�,確保其功能、安全性仍符合標準�����。
2). 包裝系統(tǒng)性能測試:評估包裝在老化后是否仍能提供有效保護���,主要測試包裝系統(tǒng)的微生物屏障性能等���,如阻菌性測試�、剝離強度測試���、染料滲透測試���、耐壓性測試等。
4. 重要原則
實時老化試驗的結果是驗證產品貨架有效期的最直接證據(jù)�����。
當加速老化試驗結果與實時老化試驗結果不一致時�����,必須以實時老化試驗結果為準�。
No.4 貨架有效期研究的注意事項
1. 典型型號選擇:對于系列產品,無需對所有型號進行研究���?����?蛇x擇結構最復雜���、組件最全���、材料最具代表性的型號進行研究,其結論應能覆蓋同系列其他產品�����。
2. 最差條件原則:試驗應建立在最苛刻的條件下進行�����,例如采用滅菌參數(shù)的上限���、使用性能臨界的組件等,以充分評估風險�����。
3. 批次一致性:用于貨架有效期研究的產品���,最好與進行注冊檢驗的產品為同一批次�,以保證數(shù)據(jù)的一致性和可追溯性�。
4. 包裝單獨研究(空白包裝):包裝系統(tǒng)的驗證可以使用空白產品或模擬物進行,以節(jié)省產品的浪費。
5. 多批次研究:對于高風險產品(如植入物)�����,監(jiān)管機構可能要求提供多批次(如三批)產品的穩(wěn)定性數(shù)據(jù)�,以證明工藝的穩(wěn)健性,具體參考產品的指導原則�。
6. 期末測試:關鍵的性能驗證,特別是安全相關測試�,應在貨架有效期末尾或剛過有效期時進行,以確認產品的安全邊界���。
7. 變更觸發(fā)再研究:當發(fā)生主要原材料/組件變更�、包裝材料變更或滅菌方式改變等情況時�,必須重新進行貨架有效期驗證。
最后�����,希望本篇對貨架有效期研究框架的梳理���,能為您的研發(fā)與注冊工作提供有價值的參考�。