本文聚焦生物發(fā)酵制藥中微生物菌株篩選與改良的策略研究���,系統(tǒng)探索微生物菌株篩選與改良策略。研究方法整合傳統(tǒng)方法與現(xiàn)代技術:傳統(tǒng)方法包括自然篩選和誘變育種�;現(xiàn)代技術涉及分子生物學(基因重組、編輯及表達調(diào)控)���、代謝工程(網(wǎng)絡分析����、系統(tǒng)優(yōu)化����、底盤設計)�、合成生物學(元件構建、基因線路設計),并結合高通量篩選與人工智能輔助�。研究證實���,傳統(tǒng)方法仍具應用價值�,現(xiàn)代技術可顯著提升菌株性能:其中谷氨酸棒狀桿菌經(jīng)代謝工程改造后賴氨酸產(chǎn)量提升80%,大腸桿菌生產(chǎn)1,3-丙二醇的產(chǎn)量提升200%,芽孢桿菌通過基因重組技術優(yōu)化后高溫淀粉酶產(chǎn)量增幅超1000%,為生物制藥產(chǎn)業(yè)提供理論支撐與實踐路徑,推動生物產(chǎn)業(yè)智能化����、綠色化發(fā)展�。
生物發(fā)酵制藥作為現(xiàn)代生物技術的關鍵分支,在抗生素����、氨基酸����、維生素���、酶制劑及重組蛋白藥物等生產(chǎn)中占據(jù)重要地位。微生物菌株作為發(fā)酵過程的核心���,其性能直接決定藥物生產(chǎn)的效率����、成本與質(zhì)量���。實踐數(shù)據(jù)顯示���,通過菌株改良技術�,不同類別目標產(chǎn)物產(chǎn)量提升效果顯著:氨基酸類(如賴氨酸)產(chǎn)量可提升 80%[1],小分子化合物類(如1,3-丙二醇)產(chǎn)量提升200%[2-3],酶制劑類(如高溫淀粉酶)產(chǎn)量增幅甚至超1000%[4]�。隨著分子生物學����、代謝工程及合成生物學等學科的發(fā)展���,菌株改良技術從傳統(tǒng)隨機誘變向理性設計轉變[5]���。本研究旨在系統(tǒng)剖析生物發(fā)酵制藥中微生物菌株篩選與改良策略���,助力產(chǎn)業(yè)發(fā)展����。
Part.01微生物菌株篩選的傳統(tǒng)策略與技術
1.1 自然篩選策略
自然篩選策略基于微生物在自然環(huán)境中的變異特性,通過定向培養(yǎng)和篩選獲取目標菌株���。其流程涵蓋樣品采集、預處理����、分離純化以及初篩與復篩����。從土壤���、水體����、動植物體表等采集樣本后,經(jīng)高溫����、離心等預處理去除雜菌����,再用平板劃線法、稀釋涂布法分離單菌落����,最后通過形態(tài)觀察�、生理生化試驗及目標產(chǎn)物檢測篩選陽性菌株�。該方法操作簡便、成本低����,無須了解菌株遺傳背景�,常用于從極端環(huán)境篩選特殊功能微生物,但存在篩選效率低����、周期長����、難以獲得性能顯著提升菌株的局限[2]�。
1.2誘變育種技術
誘變育種技術借助物理、化學或生物誘變劑處理微生物����,誘導基因突變后篩選優(yōu)良性狀菌株���,是工業(yè)微生物菌株改良的常用方法���。物理誘變劑如紫外線可誘導脫氧核糖核酸(deoxyribonucleic acid, DNA)形成嘧啶二聚體����,電離輻射能引起DNA雙鏈斷裂或堿基損傷;化學誘變劑包括堿基類似物�、烷化劑、移碼誘變劑等����,通過不同機制導致基因突變;生物誘變劑如轉座子可引起插入突變或基因表達調(diào)控改變����。篩選時常用抗性篩選����、形態(tài)學篩選和高通量篩選等方法���。然而���,該技術存在隨機性高、表型與基因型關聯(lián)差���、多輪誘變效率遞減以及難以改良復雜性狀等問題[6]���。
1.3傳統(tǒng)篩選策略的局限性
傳統(tǒng)自然篩選與誘變育種雖取得一定成效,但弊端明顯�。誘變育種突變隨機,需大規(guī)模篩選�;難以針對目標代謝途徑改良,常出現(xiàn)生長缺陷等負效應�;長期誘變會導致基因組損傷積累,菌株性能提升幅度下降�;對于多基因協(xié)同調(diào)控的復雜性狀改良效果不佳,這促使新型菌株改良策略發(fā)展[7-8]���。
Part.02基于分子生物學的菌株改良策略
2.1基因重組技術基因重組技術通過體外DNA進行操作����,將目的基因?qū)胧荏w菌株�,實現(xiàn)基因功能定向改變。質(zhì)粒介導的基因克隆需構建合適載體����,插入目的基因及調(diào)控元件,再導入受體菌篩選陽性克隆�,并優(yōu)化目的基因表達水平����;染色體整合技術利用同源重組或轉座子介導整合,可避免質(zhì)粒丟失問題���。該技術已廣泛應用于酶制劑生產(chǎn)菌株改良,如將高溫淀粉酶基因?qū)胙挎邨U菌���,提升酶的熱穩(wěn)定性和表達量[9]�。
2.2 基因編輯技術的發(fā)展與應用
人工智能輔助新藥研發(fā)所展現(xiàn)出的能力和潛力得到了全球主流藥企認可����,規(guī)律間隔成簇短回文重復序列相關蛋白9(clustered regularly interspaced short palindromic repeats/CRISPR-associated proteing, CRISPR-Cas9)作為第三代基因編輯技術�,憑借高效性和簡便性成為菌株改良核心工具。它由 Cas9 核酸酶和單導核糖核酸 (single guide ribonucleic acid, sgRNA) 組成�,可精準切割目標DNA 序列���,觸發(fā)細胞 DNA 修復機制����,實現(xiàn)基因敲除�、敲入或定點突變,在基因敲除���、調(diào)控及多基因編輯等方面廣泛應用���。此外���,鋅指核酸酶(zinc-finger nucleases, ZFN)、類轉錄激活因子效應核酸酶(transcription activator-like effector nucleases, TALEN)���、CRISPR關聯(lián)蛋白(CRISPR-associated protein, CRISPR-Cpf1) 等基因編輯技術也各有特點和應用范圍����。
2.3 表達調(diào)控網(wǎng)絡優(yōu)化
微生物代謝表型是基因表達調(diào)控網(wǎng)絡綜合作用的結果�,該網(wǎng)絡精密調(diào)控著細胞內(nèi)各類代謝活動。因此����,優(yōu)化這一網(wǎng)絡成為提升目標產(chǎn)物合成效率的關鍵突破口�。啟動子作為基因表達起始的關鍵元件,其工程通過篩選微生物基因組中天然存在的具有不同強度和調(diào)控特性的啟動子���,利用易錯聚合酶鏈式反應(polymerase chain reaction, PCR)等手段進行定向進化�,或基于核心序列從頭設計合成啟動子����,實現(xiàn)對基因表達水平的精準把控。轉錄后調(diào)控層面����,優(yōu)化核糖體結合位點(ribosome binding site, RBS)序列能增強信使RNA(messenger RNA,mRNA)與核糖體的結合效率�;小RNA(sRNA)可特異性結合靶標 mRNA,調(diào)控其穩(wěn)定性與翻譯過程����;核糖“開關”則能響應代謝物信號����,動態(tài)調(diào)節(jié)基因表達���,這些調(diào)控方式協(xié)同作用,有效提升菌株合成目標產(chǎn)物的性能���。
Part.03代謝工程導向的菌株改良策略
3.1 代謝網(wǎng)絡分析與途徑重構
代謝工程通過系統(tǒng)分析微生物代謝網(wǎng)絡���,設計基因操作優(yōu)化目標產(chǎn)物合成途徑���。包括解析目標產(chǎn)物合成途徑����,構建從頭合成途徑或優(yōu)化天然途徑���;通過增強前體供應�、阻斷競爭途徑、平衡輔酶因子供應等方式�,實現(xiàn)代謝通量重分配����,提高目標產(chǎn)物產(chǎn)量�,如表1所示。
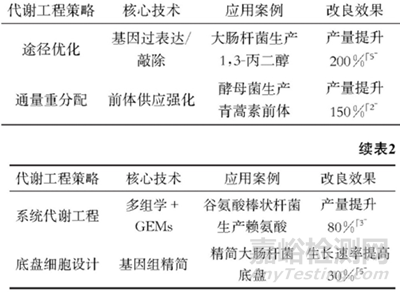
表1 代謝途徑重構主要優(yōu)化策略及應用
3.2 系統(tǒng)代謝工程策略
系統(tǒng)代謝工程通過整合多組學數(shù)據(jù)與計算生物學模型,搭建起代謝網(wǎng)絡全局優(yōu)化的系統(tǒng)性框架���。借助轉錄組學技術可解析不同生理狀態(tài)下的基因表達譜,代謝組學能精準檢測胞內(nèi)代謝物濃度動態(tài)變化�,蛋白質(zhì)組學則揭示蛋白質(zhì)互作與修飾調(diào)控機制�。通過轉錄組學����、代謝組學、蛋白質(zhì)組學數(shù)據(jù)的交叉分析(如基于生物信息學工具對差異表達基因�、關鍵代謝物及互作蛋白進行關聯(lián)映射),可定位代謝網(wǎng)絡中的關鍵節(jié)點與潛在瓶頸(表2)。在此基礎上�,結合基因組規(guī)模代謝模型(如大腸桿菌 iJO1366 模型)與通量平衡分析(FBA)等計算工具,通過數(shù)學建模預測不同基因擾動或環(huán)境條件下代謝通量分布�,進而指導基因敲除�、過表達等改造策略的設計�,實現(xiàn)從局部途徑優(yōu)化到全局代謝網(wǎng)絡重分配的精準調(diào)控�,為菌株高效生產(chǎn)目標產(chǎn)物提供數(shù)據(jù)驅(qū)動的理性改造方案[9]���。
3.3 底盤細胞設計
底盤細胞是經(jīng)定向改造���、適配制藥需求的 “標準化生產(chǎn)平臺”,核心技術有:對大腸桿菌等模式菌用基因組精簡剔除冗余基因�、定制代謝網(wǎng)絡,如精簡大腸桿菌生長速率���,提高至30%[5];對非模式/極端菌通過代謝網(wǎng)絡重構“適配” 合成模塊���、基因編輯改特殊代謝機制�;用標準化元件接口改造實現(xiàn) “一底盤多產(chǎn)品”���。其側重宿主架構優(yōu)化�,與系統(tǒng)代謝工程的全局通量調(diào)控形成 “基礎—應用” 遞進���。
表2 代謝工程主要策略及應用案例
Part.04合成生物學驅(qū)動的菌株創(chuàng)新改良
4.1 標準化生物元件構建
合成生物學以工程化理念重塑微生物改造邏輯,通過設計標準化����、模塊化的生物元件,構建可預測�、可復用的“生物積木”體系����,從而實現(xiàn)微生物功能的定向編程����。在基因表達層面,標準化元件包括強度可量化的啟動子(如大腸桿菌 lac 啟動子)���、翻譯效率可控的核糖體結合位點(RBS)及高效轉錄終止子���,形成基因表達的 “開關系統(tǒng)”;代謝功能模塊則將復雜代謝途徑拆解為獨立功能單元,如萜類合成模塊���、脂肪酸延伸模塊,配合四環(huán)素響應調(diào)控模塊等實現(xiàn)途徑動態(tài)調(diào)控����;細胞行為控制元件如 LuxI/LuxR 群體感應系統(tǒng)���,可同步菌群代謝行為����,而芽孢桿菌細胞周期調(diào)控元件能分離生長與合成階段���。這些標準化元件通過模塊化組裝���,賦予微生物底盤定制化的代謝生產(chǎn)能力[6]。
4.2 人工基因線路設計
人工基因線路通過組合生物元件設計遺傳調(diào)控網(wǎng)絡�,賦予微生物新功能或優(yōu)化現(xiàn)有功能���。邏輯門電路實現(xiàn)不同信號響應下的基因表達調(diào)控�;振蕩系統(tǒng)使基因表達周期性變化,提高代謝產(chǎn)物合成效率�;記憶系統(tǒng)記錄細胞歷史狀態(tài),用于環(huán)境脅迫響應或產(chǎn)物合成時序調(diào)控���。組合生物合成通過模塊化重組生物合成基因簇����,可重構次級代謝途徑以創(chuàng)造新型化合物����,或優(yōu)化關鍵酶組合提升目標產(chǎn)物產(chǎn)量。
4.3 合成生物學在菌株改良中的前沿應用
合成生物學在復雜天然產(chǎn)物全合成�、細胞工廠智能化設計和基因組編輯重編程等方面展現(xiàn)出巨大潛力。在酵母菌中重構阿片類生物堿合成途徑���,突破傳統(tǒng)提取限制����;設計智能響應系統(tǒng)�,使微生物自動調(diào)整代謝通量;構建最小基因組����,優(yōu)化生產(chǎn)底盤。
Part.05菌株篩選與改良的高通量技術平臺
5.1 高通量篩選技術
微流控芯片技術利用納升級反應單元實現(xiàn)單個細胞培養(yǎng)與篩選����,高通量且低試劑消耗;流式細胞術結合熒光報告蛋白���,可快速分選海量細胞���;自動化篩選平臺整合多種設備,實現(xiàn)菌株培養(yǎng)到活性檢測全流程自動化���,大幅提高篩選效率���。定向進化技術通過易錯 PCR、DNA shuffling 構建基因突變庫���,結合酵母表面展示/噬菌體展示(用于酶等蛋白突變體的高效篩選),可定向優(yōu)化功能蛋白活性���,為菌株性能提供精準靶向改良手段。
5.2 人工智能在菌株設計中的應用
機器學習預測模型通過監(jiān)督學習(以已知基因-表型關聯(lián)數(shù)據(jù)為標簽���,訓練隨機森林�、神經(jīng)網(wǎng)絡等模型)或無監(jiān)督學習(對多組學數(shù)據(jù)聚類�,挖掘未知基因-型關聯(lián))分析多組學數(shù)據(jù),構建精準基因-表型映射模型�,高效預測菌株改良靶點。自動化設計平臺結合計算模型與機器學習���,實現(xiàn)菌株設計流程智能化�,加速開發(fā)進程���。
Part.06結 論
生物發(fā)酵制藥中微生物菌株篩選與改良技術經(jīng)歷了從傳統(tǒng)到現(xiàn)代的演進���。傳統(tǒng)篩選策略如自然篩選���、誘變育種雖存在一定局限性,但仍在特定場景發(fā)揮作用�;基于分子生物學、代謝工程和合成生物學的現(xiàn)代技術�,實現(xiàn)了對菌株的精準設計與高效改造,顯著提升了目標產(chǎn)物產(chǎn)量與生產(chǎn)效率�。高通量篩選技術和人工智能的應用,進一步加速菌株開發(fā)進程����。未來,隨著多學科交叉融合的深入���,菌株改良技術將朝著智能化���、綠色化、高效化方向發(fā)展���,有望攻克更多技術難題�,為生物發(fā)酵制藥產(chǎn)業(yè)的高質(zhì)量發(fā)展注入強勁動力�。
參考文獻
[1]陳宇翔.微生物發(fā)酵技術在生物制藥產(chǎn)業(yè)中的智能化應用研 究[J].高科技與產(chǎn)業(yè)化,2025,31(4):67-70.
[2]王偉,劉巧,方雪,等.新工科視域下生物制藥專業(yè)“微生物工 程”教學改革探索與實踐———以合肥師范學院為例[J].合肥 師范學院學報,2024,42(6):90-94.
[3]白立勇,葛新霞,王建華.微生物發(fā)酵制藥技術[J].化工設計 通訊,2020,46(10):148-149.
[4]蔣敏,劉朋,李恒,等.生物特色的制藥工藝綜合實驗[J].實 驗技術與管理,2020,37(4):78-81.
[5]郭建勇.生物發(fā)酵制藥工業(yè)的膜技術分析[J].山東工業(yè)技 術,2017,(15):3.
[6]李鵬飛.生物制藥技術在制藥工藝中的應用[J].當代化工研 究,2024,(14):164-166.
[7]王會會,程啟東,戴夢,等.萬古霉素高產(chǎn)菌株選育及發(fā)酵配 方優(yōu)化[J].河北工業(yè)科技,2022,39(3):253-260.
[8]楊順楷.甾體微生物轉化:糖皮質(zhì)激素氫化可的松生物轉化 的魯棒性及其研究應用[J].應用與環(huán)境生物學報,2022,28(1):230-238.
[9]于晴,黃婷婷,鄧子新.微生物藥物產(chǎn)業(yè)現(xiàn)狀與發(fā)展趨勢[J].中國工程科學,2021,23(5):69-78.