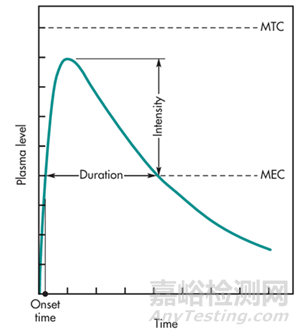
藥物的消除半衰期(t½)在藥代動力學(xué)中,被定義為藥物在體內(nèi)的濃度或總量降低一半所需的時間���。這個參數(shù)是血藥濃度-時間曲線(C-tcurve)分析中的一個核心指標(biāo)�����。一條典型的C-t曲線描繪了藥物經(jīng)吸收���、分布、代謝�、排泄(ADME)全過程后,血漿中藥物濃度隨時間的變化情況���。半衰期主要反映了藥物從體內(nèi)消除(代謝和排泄)的速率�����。一個簡短的半衰期意味著藥物被機體快速清除�����,反之則意味著清除緩慢�����。
圖1 口服給藥一般的藥時曲線
在臨床前或臨床研究中���,通過對不同時間點采集的血樣進(jìn)行分析�,可以繪制出完整的血藥濃度-時間曲線�,并從中計算出半衰期、達(dá)峰濃度(Cmax)�、達(dá)峰時間(Tmax)和曲線下面積(AUC)等關(guān)鍵PK參數(shù)。這些數(shù)據(jù)是后續(xù)制劑設(shè)計的基礎(chǔ)和依據(jù)���。通常���,為了獲得完整的曲線,采樣時間需要持續(xù)3-5個半衰期�。
1半衰期為何是制劑設(shè)計的關(guān)鍵錨點
半衰期在制劑設(shè)計中占據(jù)核心地位�,理論上,為了維持血藥濃度在有效治療窗(即最低有效濃度MEC和最低中毒濃度MTC之間)內(nèi)�����,給藥間隔應(yīng)約等于藥物的半衰期。這意味著短半衰期藥物需要頻繁給藥���,而長半衰期藥物則可以實現(xiàn)較長的給藥間隔�。頻繁給藥不僅降低了患者的依從性�����,還容易導(dǎo)致血藥濃度的劇烈波動——在給藥后出現(xiàn)過高的峰濃度(Cmax)�����,可能引發(fā)毒副作用���;而在下次給藥前出現(xiàn)過低的谷濃度�,可能導(dǎo)致療效不足�����。對于天然半衰期不理想的藥物�����,制劑科學(xué)的目標(biāo)就是通過技術(shù)手段“修飾”或“重塑”其在體內(nèi)的釋放行為,從而人為地延長其作用時間�����,實現(xiàn)更理想的給藥方案�����。這正是緩釋���、控釋�����、長效制劑等特殊遞送系統(tǒng)發(fā)揮作用的核心場景�。因此���,拿到一個候選化合物的半衰期數(shù)據(jù)�����,是制劑科學(xué)家開啟配方設(shè)計之旅的第一步�。
2.基于不同半衰期范圍的制劑設(shè)計總體策略
根據(jù)半衰期的長短�,我們可以將藥物大致分為三類,并采用截然不同的制劑設(shè)計策略���,當(dāng)然了分類僅供參考�,實際設(shè)計中需結(jié)合藥效學(xué)與臨床需求���。
2.1短半衰期藥物(t½<4-6小時)的挑戰(zhàn)與對策
短半衰期藥物是制劑開發(fā)中最常遇到也最具挑戰(zhàn)性的情況���。一天需要給藥3-4次甚至更多,患者依從性極差�,尤其對于需要長期治療的慢性病(如高血壓�����、糖尿?。┒裕@是一個巨大的障礙�����。典型的“峰谷”現(xiàn)象明顯���,增加了Cmax相關(guān)的毒性風(fēng)險和谷濃度時“藥物假期”導(dǎo)致的療效喪失風(fēng)險�����?;颊咭归g無法按時服藥,導(dǎo)致治療效果中斷���。延長作用時間�,實現(xiàn)“降頻增效”�。針對短半衰期藥物,制劑設(shè)計的首要目標(biāo)是將其開發(fā)成緩釋或控釋制劑�,以減少給藥頻率至每日一次或兩次。
口服緩控釋制劑(Oral Sustained/Controlled-Release Formulations):這是最常用和最成熟的策略�。
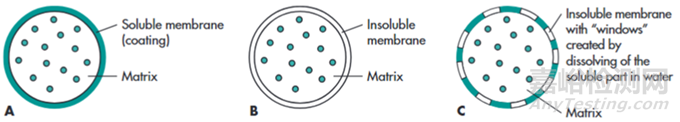
骨架型緩釋片:將藥物與高分子材料(如HPMC)混合壓片,藥物通過溶蝕或擴散緩慢釋放�����。
圖2 三種不同類型的修飾性基質(zhì)釋放機制示例�。
膜控型緩釋制劑:將藥物制成丸芯,再包上一層不溶或半透的高分子膜�����,通過膜上的微孔或滲透壓來控制藥物釋放速率。滲透泵片是其中的高精尖代表�����。
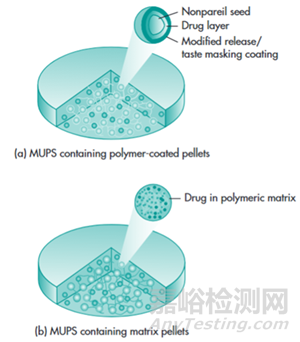
微丸或微球系統(tǒng)(Microspheres):將藥物制成微小的球狀顆粒���,再填充到膠囊或壓成片劑。這些微球本身可以是骨架型或膜控型���,能夠?qū)崿F(xiàn)平穩(wěn)的藥物釋放���。這種劑型在胃腸道中分散廣,受食物影響小�����,個體差異小���。
圖3 多單元微丸系統(tǒng)(MUPS)片劑類型示意圖——(a) 由包衣微丸組成�,(b) 未包衣/基質(zhì)微丸�。
長效注射劑(Long-Acting Injectables ,LAI):對于需要通過注射給藥的短半衰期藥物(如多肽、蛋白質(zhì))�,或者為了實現(xiàn)更長給藥周期(如一周、一月甚至數(shù)月)的藥物,LAI是理想選擇�。
聚合物微球/原位凝膠:將藥物包裹在可生物降解的聚合物(如PLGA)微球中,注射后微球在體內(nèi)緩慢降解釋放藥物�����?;蛘咦⑸湟环N液體,在體內(nèi)形成凝膠儲庫���,緩慢釋放藥物���。
油性注射液/混懸劑:利用藥物在油相中的低溶解度或制成結(jié)晶混懸液,延緩藥物從注射部位的吸收�。
透皮給藥系統(tǒng)(Transdermal Delivery Systems ,TDS):如果藥物的理化性質(zhì)(如分子量小、親脂性適中�����、日劑量?。┖线m,可以設(shè)計成透皮貼劑�����。貼劑能夠以接近零級速率的方式,連續(xù)數(shù)日向血液循環(huán)中輸送藥物�����,提供極其平穩(wěn)的血藥濃度�,完美解決了短半衰期藥物的難題。
最后需要強調(diào)���,當(dāng)你打算為一個半衰期短的藥物開發(fā)緩釋制劑時,第一步必須是判斷它的短半衰期是由“快速消除”還是“慢速吸收”引起的�����。如果是快速消除�,那么緩釋技術(shù)是對癥下藥的正確策略。如果是慢速吸收�����,那么緩釋技術(shù)可能就是雪上加霜的危險操作���。此時�����,制劑科學(xué)家首先應(yīng)該考慮的是如何改善藥物的吸收(例如通過增溶�、使用吸收促進(jìn)劑、改變給藥途徑等)�����,而不是進(jìn)一步去延緩它�。
案例分享:鹽酸哌甲酯緩釋片(Concerta®)
鹽酸哌甲酯是一種中樞神經(jīng)系統(tǒng)興奮劑,適用于治療注意缺陷多動障礙(ADHD)���,常用于6歲及以上的兒童���。哌甲酯口服后吸收迅速,消除半衰期約為3.5小時�����。
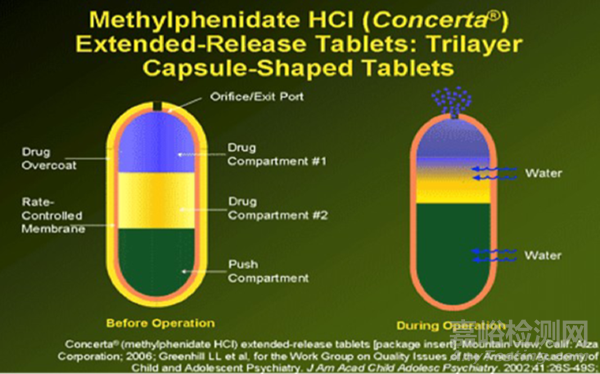
鹽酸哌甲酯緩釋片(Concerta)包含一個具有滲透活性的控釋核心和一層速釋藥物外衣���。該產(chǎn)品利用滲透壓以可控速率遞送鹽酸哌甲酯���。此系統(tǒng)外觀與普通片劑相似,由一個滲透活性的三層核心�、包裹其的半透膜以及一層速釋藥物外衣組成�����。三層核心包含兩個含藥物及輔料的藥物層和一個含滲透活性成分的推動層�。
本品為每日一次口服給藥的緩釋片劑�,含有18、27���、36或54 mg USP標(biāo)準(zhǔn)鹽酸哌甲酯���,設(shè)計有效時長為12小時?����?诜﨏oncerta后���,血漿哌甲酯濃度迅速上升,約1小時達(dá)到首次峰值�����,隨后在接下來的5至9小時內(nèi)濃度逐漸升高���,之后開始逐漸下降�。平均達(dá)峰時間出現(xiàn)在服藥后6至10小時。
當(dāng)患者在早晨服用此產(chǎn)品時�,會先獲得一個初始負(fù)荷劑量,隨后是維持劑量�。由于藥物具有較短的消除半衰期,其在傍晚患者需要入睡時已基本消除�����,因此不會在體內(nèi)產(chǎn)生蓄積�����。
圖4 鹽酸哌甲酯緩釋片(Concerta®)制劑設(shè)計
2.2中等半衰期藥物(t½≈8-12小時)的制劑設(shè)計考量
這類藥物的半衰期使其天然適合每日一到兩次的給藥方案�,因此制劑設(shè)計的重點有所不同。雖然每日兩次是可接受的�,但每日一次的方案無疑能進(jìn)一步提升患者依從性。保證生物利用度���,確保藥物能夠被充分�����、穩(wěn)定地吸收是首要任務(wù)�。針對特定治療需求,可能需要快速起效或與其他藥物聯(lián)用�����。
制劑設(shè)計對策經(jīng)常是常規(guī)與優(yōu)化并舉�,如常規(guī)速釋制劑(Immediate-Release Formulations)是最基礎(chǔ)的選擇,如普通片劑或膠囊�����。制劑工作的核心在于解決藥物的溶解度和滲透性問題���,以確保其生物利用度�����。這需要充分考慮化合物的pKa、溶解度���、穩(wěn)定性等理化性質(zhì)�����。例如�,對于溶解度差的藥物,可能需要采用微粉化�����、制成鹽�����、或開發(fā)成固體分散體等技術(shù)來增溶�����;每日一次的緩釋制劑將每日兩次的給藥方案優(yōu)化為每日一次�,可以顯著提高患者的生活質(zhì)量。此時���,不需要像短半衰期藥物那樣復(fù)雜的控釋技術(shù)�����,可能一個簡單的親水凝膠骨架片就足以將其作用時間延長至24小時�����。
優(yōu)化型劑型�,如口腔崩解片(ODT),無需用水即可在口中迅速崩解���,方便吞咽困難的兒童或老年患者�����;復(fù)方制劑(FDC)�,將此藥物與另一個治療相關(guān)藥物(可能具有不同半衰期)組合在同一片劑中�����,簡化治療方案���;對于治療窗窄的中等半衰期藥物�,也可考慮控釋制劑以平穩(wěn)血藥濃度�����。
2.3長半衰期藥物(t½>24小時)的挑戰(zhàn)與對策
長半衰期藥物在給藥頻率上具有天然優(yōu)勢�����,但同時也帶來了新的挑戰(zhàn)�����。連續(xù)給藥時���,由于消除緩慢,藥物容易在體內(nèi)蓄積���,導(dǎo)致血藥濃度逐漸升高���,最終可能超過中毒濃度(MTC),引發(fā)毒副作用�����。需要經(jīng)過多個半衰期(通常是4-5個t½)才能達(dá)到穩(wěn)態(tài)血藥濃度���,對于需要快速起效的疾病來說可能無法滿足需求�����。一旦發(fā)生嚴(yán)重不良反應(yīng)�����,由于藥物在體內(nèi)清除緩慢���,不良反應(yīng)會持續(xù)很長時間���。
制劑設(shè)計對策一般是側(cè)重安全性、快速起效與精準(zhǔn)控制���。
常規(guī)速釋制劑結(jié)合給藥方案調(diào)整:對于大多數(shù)長半衰期藥物���,常規(guī)的速釋片劑或膠囊是標(biāo)準(zhǔn)選擇。其挑戰(zhàn)不在于劑型本身�,而在于給藥方案的設(shè)計。
負(fù)荷劑量(Loading Dose):為了快速達(dá)到穩(wěn)態(tài)濃度���,可以在治療開始時給予一個或數(shù)個較高的初始劑量,隨后轉(zhuǎn)為較低的維持劑量�����。制劑上可以開發(fā)不同規(guī)格的片劑來配合這種方案���。
避免進(jìn)一步緩釋:通常不推薦將長半衰期藥物開發(fā)成緩釋劑型�,因為這會進(jìn)一步加劇藥物蓄積的風(fēng)險�,導(dǎo)致不可控的毒性。
靶向遞送系統(tǒng)(Targeted Delivery):對于一些毒性較大的長半衰期藥物(如某些抗癌藥)�����,盡管其半衰期很長�,但全身暴露仍然是有害的。此時�����,制劑設(shè)計的方向是“空間選擇性”而非“時間控制”�。可以利用脂質(zhì)體�����、納米粒���、抗體-藥物偶聯(lián)物(ADC)等載體���,將藥物主動或被動地靶向遞送至病變組織或器官。這樣可以在不影響全身半衰期的情況下,提高病灶部位的藥物濃度�����,同時顯著降低在健康組織中的暴露���,從而“解耦”療效與全身毒性�����。靶向系統(tǒng)可能改變藥物的PK特性�,需重新評估其半衰期與給藥方案���。
3.制劑設(shè)計中必須綜合考量的其他關(guān)鍵因素
半衰期是制劑設(shè)計的起點�����,但絕非終點。一個成功的制劑方案�����,必須是多維度因素綜合平衡的結(jié)果���。
3.1化合物的理化性質(zhì):藥物的溶解度�����、pKa���、滲透性、穩(wěn)定性�����、分子量等是劑型設(shè)計的根本制約因素�。例如,一個水溶性極差的藥物�,即使半衰期很短,也難以制成簡單的口服緩釋片�����,因為釋放出的藥物無法溶解�����,也就無法吸收�����。此時可能需要先通過增溶技術(shù)(如制成納米混懸劑)再結(jié)合緩釋技術(shù)。同樣���,大分子藥物(如蛋白質(zhì))通常無法口服���,也難以透皮吸收,其制劑設(shè)計路線基本被限定在注射給藥�����。
3.2給藥途徑與生物利用度:選擇何種給藥途徑(口服�����、注射���、透皮���、吸入等)直接影響制劑設(shè)計的技術(shù)平臺?����?诜o藥方便,但面臨胃腸道降解和肝臟首過效應(yīng)的挑戰(zhàn)�,這可能導(dǎo)致表觀半衰期縮短�。對于存在嚴(yán)重首過效應(yīng)的藥物,其口服生物利用度本就低下�,若再疊加‘吸收速率限制’,則開發(fā)口服緩釋制劑的挑戰(zhàn)和風(fēng)險會進(jìn)一步加劇�。而注射給藥生物利用度高,但便利性差且需要無菌生產(chǎn)�����。制劑科學(xué)家必須權(quán)衡利弊�。
3.3治療窗與毒理學(xué)特性:治療窗窄的藥物�,對血藥濃度的平穩(wěn)性要求極高。即使其半衰期中等�����,也通常需要開發(fā)成控釋制劑���,以精確地將血藥濃度維持在狹窄的治療窗內(nèi)���,避免因微小波動引發(fā)的毒性或失效���。
3.4適應(yīng)癥與患者群體:藥物用于治療急性病還是慢性病�����?患者是兒童�、成人還是老人?這些臨床需求深刻影響劑型選擇�����。例如���,用于急救的藥物必須是速效劑型(如靜脈注射液)�����;而用于老年癡呆癥患者的藥物�,則應(yīng)優(yōu)先考慮能提高依從性的長效貼劑或長效注射劑�����。
4.總結(jié)
綜上所述,化合物的消除半衰期是藥物制劑設(shè)計過程中的一個核心導(dǎo)航參數(shù)���。它像一個指南針�,為制劑科學(xué)家指明了初步的設(shè)計方向:對于短半衰期藥物���,核心任務(wù)是通過緩釋、控釋技術(shù)“延長”藥物的作用時間�,將頻繁給藥轉(zhuǎn)變?yōu)槊咳找淮位蚋皖l率的便捷方案。對于中等半衰期藥物���,重點在于優(yōu)化吸收和提升便利性�,可以在速釋和適度緩釋之間靈活選擇�。對于長半衰期藥物���,關(guān)鍵在于控制蓄積風(fēng)險���,確保用藥安全,劑型上通常選擇速釋制劑�����,并配合給藥方案的調(diào)整�,或在特定情況下采用靶向遞送策略�����。
然而�,必須強調(diào)�����,制劑設(shè)計是一門“平衡的藝術(shù)”���。半衰期不能孤立地作為唯一決策依據(jù)�����。最終的制劑方案���,必然是綜合考量了藥物的理化性質(zhì)、預(yù)期的給藥途徑�����、藥理與毒理特性以及最終的臨床需求等多方面因素后�,做出的最優(yōu)選擇。未來的藥物遞送系統(tǒng)將更加智能化和個性化,但深刻理解并善用半衰期這一基本藥代動力學(xué)原理���,將永遠(yuǎn)是所有復(fù)雜制劑設(shè)計工作的基石�。
參考資料
1.Applied Biopharmaceutics &Pharmacokinetics 19 Modified-Release Drug Products and Drug Devices
2.https://www.accessmhct.com/wp-content/uploads/2021/01/ADHD-201-v.1.7.2021.pptx