對(duì)于志在開(kāi)拓東南亞市場(chǎng)的制藥企業(yè)而言,菲律賓無(wú)論從地理位置還是人口結(jié)構(gòu)來(lái)說(shuō)�����,都是一個(gè)表現(xiàn)優(yōu)秀的市場(chǎng)�����。獲得菲律賓FDA的GMP認(rèn)證�����,不僅是法規(guī)要求,更是產(chǎn)品質(zhì)量的體現(xiàn)�����。菲律賓GMP檢查嚴(yán)格遵循PIC/s指南�,并且對(duì)細(xì)節(jié)極致關(guān)注。檢查依據(jù)主要有以下三個(gè):PIC/s GMP指南PE009-14及其相關(guān)附錄�����,菲律賓《食品與藥品管理法》RA(Republic Act)9711���,行政命令A(yù).O.(Administrative Order)2012-0008���。
近日,筆者參與了一場(chǎng)菲律賓FDA為期數(shù)日的現(xiàn)場(chǎng)檢查�����,并最終以“近乎零缺陷”的優(yōu)異表現(xiàn)順利通過(guò)���。這場(chǎng)勝利�,并非偶然�����,而是源于對(duì)標(biāo)準(zhǔn)的深刻理解���、系統(tǒng)化的萬(wàn)全準(zhǔn)備和現(xiàn)場(chǎng)專業(yè)從容的應(yīng)對(duì)。筆者將結(jié)合陪審期間的經(jīng)驗(yàn)所得和檢查官的關(guān)注點(diǎn)���,來(lái)深度復(fù)盤(pán)這場(chǎng)“大考”�����,也希望能給同行一些參考�。
01洞悉規(guī)則——菲律賓GMP檢查的獨(dú)特視角
筆者本次參與的檢查,有三名檢查官�,共檢查四天�����。菲律賓檢查官有非常清晰的檢查邏輯:
1. 流程導(dǎo)向的檢查路線:檢查嚴(yán)格遵循物料與產(chǎn)品流向���,從倉(cāng)庫(kù)接收開(kāi)始�,到生產(chǎn)的每一環(huán)節(jié)�、到取樣送檢至QC實(shí)驗(yàn)室,直至產(chǎn)品放行�。這要求我們的質(zhì)量體系必須是一個(gè)無(wú)縫銜接的閉環(huán)。
2. 分工協(xié)作與語(yǔ)言保障:本次三位檢查官采用分工模式:組長(zhǎng)與一員查看生產(chǎn)車(chē)間,另一員專查QC實(shí)驗(yàn)室�。這意味著我們至少需要兩組具備專業(yè)知識(shí)的陪檢人員和翻譯同步進(jìn)行,任何一環(huán)的溝通不暢都可能造成誤解���。
3. 基于PIC/s指南的逐條核對(duì):檢查官在文件審查時(shí)會(huì)直接參照PIC/s指南條款,并索要相關(guān)SOP進(jìn)行比對(duì)���,其嚴(yán)謹(jǐn)程度可見(jiàn)一斑�。
4. “看得見(jiàn)”的質(zhì)量:檢查官不固執(zhí)于必須進(jìn)入潔凈區(qū),但前提是通過(guò)觀察窗或監(jiān)控�,他們能對(duì)關(guān)鍵崗位的操作和環(huán)境建立信心。因此�����,現(xiàn)場(chǎng)的定置管理、人員操作的規(guī)范性和可視化的良好印象至關(guān)重要���。
02萬(wàn)全準(zhǔn)備——基于差距分析的精準(zhǔn)整改
正式的檢查通知會(huì)提前三個(gè)月由菲律賓官方通過(guò)郵件發(fā)送至進(jìn)口商�����,進(jìn)口商再通知生產(chǎn)企業(yè)���。收到檢查通知的那一刻起,公司的生產(chǎn)質(zhì)量體系就應(yīng)進(jìn)入迎檢狀態(tài)�����。其實(shí)�����,在向官方遞交PTR(與GMP體系相關(guān)的一套資料)時(shí)�����,公司就應(yīng)做好迎檢準(zhǔn)備�����。臨時(shí)抱佛腳很難通過(guò)檢查,準(zhǔn)備工作的核心是“模擬審計(jì)�,精準(zhǔn)整改”���。
1. 成立跨職能迎檢團(tuán)隊(duì)與模擬審計(jì):建議組建覆蓋質(zhì)量�、生產(chǎn)、QC�����、工程技術(shù)���、倉(cāng)儲(chǔ)的核心團(tuán)隊(duì)�����,進(jìn)行模擬審計(jì)�。模擬審計(jì)完全仿照菲律賓檢查模式�����,根據(jù)物料流向設(shè)計(jì)檢查路線�,確保每個(gè)環(huán)節(jié)都有專人負(fù)責(zé)�����,并能流利英文應(yīng)答�。
2. 合理利用外部資源幫助整改:為系統(tǒng)性彌補(bǔ)內(nèi)部差距�����,建議引入第三方權(quán)威視角�����,聘請(qǐng)資深的GMP合規(guī)顧問(wèn)進(jìn)行模擬審計(jì)�����。旨在借助其豐富的迎檢經(jīng)驗(yàn),精準(zhǔn)識(shí)別因“熟視無(wú)睹”而難以發(fā)現(xiàn)的潛在缺陷�,并就整改措施的有效性與合規(guī)性提供專業(yè)指導(dǎo)���,從而確保我們的迎檢準(zhǔn)備工作經(jīng)得起最嚴(yán)格的檢驗(yàn)���。
03現(xiàn)場(chǎng)應(yīng)對(duì)——專業(yè)�、坦誠(chéng)與溝通的藝術(shù)
現(xiàn)場(chǎng)檢查是對(duì)準(zhǔn)備工作的終極檢驗(yàn)�����。
1. 開(kāi)場(chǎng)亮相:在首次會(huì)議上�����,建議用準(zhǔn)備好的廠區(qū)平面圖、車(chē)間平面圖�、人物流圖、潔凈分區(qū)圖進(jìn)行講解�,直觀地展示了工廠的合理布局和質(zhì)量控制思路���,奠定了專業(yè)的基調(diào)�。生產(chǎn)企業(yè)需要按照菲律賓檢查官的要求,準(zhǔn)備中英雙語(yǔ)的各類圖紙���,并用A3紙彩色打印給到每一位檢查官。
2. 嚴(yán)格執(zhí)行入場(chǎng)程序:檢查官進(jìn)入任何受控區(qū)域前�����,都需要由陪審人員嚴(yán)格按照SOP�,利用圖示和實(shí)物對(duì)其進(jìn)行更衣培訓(xùn)�,并在記錄表上詳細(xì)登記�����,一絲不茍的做法會(huì)給檢查官留下了嚴(yán)格遵守GMP的第一印象���。需要注意的是,菲律賓檢查官要求退更流程及圖示也需要張貼在更衣間���。
3. 生產(chǎn)現(xiàn)場(chǎng)引導(dǎo)及溝通原則:在車(chē)間入口處介紹平面圖和人物流走向后,從物料入口開(kāi)始引導(dǎo)�����。崗位人員和陪檢翻譯人員始終堅(jiān)持“問(wèn)什么,答什么”的原則���。對(duì)于挑戰(zhàn)性問(wèn)題,不延伸、不辯解�,而是基于事實(shí)和文件,結(jié)合風(fēng)險(xiǎn)評(píng)估進(jìn)行專業(yè)�、坦誠(chéng)的溝通。這種態(tài)度反而會(huì)贏得檢查官的尊重和信任�����。
4. 高效的文檔支持:操作現(xiàn)場(chǎng)的相關(guān)SOP及記錄藥品按規(guī)定懸掛在固定區(qū)域���,并定時(shí)定期維護(hù)���,菲律賓檢查官對(duì)記錄的維護(hù)尤其關(guān)注。當(dāng)檢查官參照PIC/s條款索要相關(guān)文件時(shí)�����,需要快速響應(yīng)���,這是對(duì)文件管理能力的一種考查�����。
04復(fù)盤(pán)與升華——將觀察項(xiàng)轉(zhuǎn)化為提升的階梯
檢查官提出的每一項(xiàng)觀察和建議,都是我們寶貴的財(cái)富�����。建議容易整改的項(xiàng)目�����,在檢查期間就立即展開(kāi)整改行動(dòng)���,這樣最終體現(xiàn)在檢查報(bào)告上的缺陷項(xiàng)目就會(huì)盡可能少,能夠最大可能的拿到最高的符合性等級(jí)�����。
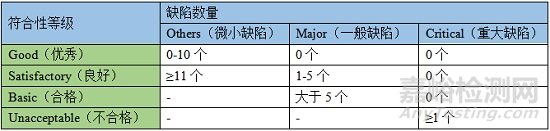
菲律賓的GMP符合性等級(jí)評(píng)估如下:
以下是與GMP咨詢專家交流后,總結(jié)出菲律賓現(xiàn)場(chǎng)檢查中出現(xiàn)的典型問(wèn)題與高頻不符合項(xiàng)�,旨在為同業(yè)提供詳實(shí)的參考,助力企業(yè)對(duì)標(biāo)自查�,規(guī)避類似風(fēng)險(xiǎn),持續(xù)優(yōu)化質(zhì)量管理體系���。
● 人員培訓(xùn)與行為規(guī)范
1. 對(duì)制水�、滅菌等關(guān)鍵崗位的操作與監(jiān)控�����,建議崗位相關(guān)人員快速并準(zhǔn)確回答日常監(jiān)控項(xiàng)目���、頻次、取樣點(diǎn)���、設(shè)備維護(hù)�����、清洗消毒規(guī)程等所有關(guān)鍵點(diǎn)���。
2. 建議在更衣室醒目位置張貼包含退更流程的完整圖示,圖示需與SOP及現(xiàn)場(chǎng)設(shè)施(如衣物筐、洗手臺(tái))完全一致�����。只有更衣流程而缺少退更流程���,也會(huì)成為一項(xiàng)缺陷���。更衣室的鏡子如是半身鏡,建議更換為全身鏡���,確保員工可自查整體著裝符合性。
3. 檢查官格外比較關(guān)注《燈檢人員管理制度》�����,需要在崗人員回答視力檢查的標(biāo)準(zhǔn)(如視力要求���、色覺(jué)要求)�、體檢頻次(如上崗前�����、每年)、具體項(xiàng)目以及工間休息安排(如每工作1小時(shí)休息10-15分鐘)���。建議所有記錄(體檢報(bào)告�、休息記錄)歸檔備查�,工作中的休息時(shí)間需要體現(xiàn)在批生產(chǎn)記錄中,并簽字復(fù)核�����。
● 設(shè)備�、設(shè)施與計(jì)量管理
1. 所有關(guān)鍵設(shè)備(如稱量罩)、設(shè)施部件(如所有回風(fēng)口)都需要有唯一性編號(hào)�����,并建立臺(tái)賬�����。確?,F(xiàn)場(chǎng)無(wú)一儀器設(shè)備超校準(zhǔn)有效期���。校準(zhǔn)證書(shū)需明確校準(zhǔn)機(jī)構(gòu)(內(nèi)?��;蛲庑#?����、標(biāo)準(zhǔn)�、頻次和結(jié)果���。對(duì)于關(guān)鍵工藝設(shè)備(如滅菌柜)�,應(yīng)在其附近設(shè)置專用記錄板�,及時(shí)放置批生產(chǎn)記錄和設(shè)備使用日志。
2. 對(duì)于器具存放間的軟管等工器具���,需要為每根軟管配備標(biāo)識(shí)卡�,明確記錄清潔人���、清潔日期�����、有效期���。同時(shí)�����,需要規(guī)定清潔后管口的保護(hù)方法(如使用無(wú)菌袋包扎)和存放要求(如懸掛�����,管口不得觸地)�����。對(duì)于有破損風(fēng)險(xiǎn)的金屬軟管���,立即更換并納入預(yù)防性維護(hù)計(jì)劃。
● 生產(chǎn)與工藝控制
1. 對(duì)于滅菌柜�,建議在現(xiàn)場(chǎng)張貼各種裝載模式的示意圖和操作要點(diǎn)。對(duì)于除菌過(guò)濾系統(tǒng)�,建議準(zhǔn)備一張系統(tǒng)流程圖,清晰標(biāo)注各級(jí)過(guò)濾器的安裝位置�、所屬潔凈區(qū)、濾芯孔徑和編號(hào)�,便于快速向檢查官展示。
2. 對(duì)于金屬檢測(cè)儀和檢重稱�,應(yīng)基于風(fēng)險(xiǎn)評(píng)估���,確定日常挑戰(zhàn)測(cè)試的必要性和頻次�。若評(píng)估后認(rèn)為必要,需訂入SOP���,規(guī)定每班次生產(chǎn)前使用標(biāo)準(zhǔn)測(cè)試塊進(jìn)行測(cè)試并記錄���。若評(píng)估后認(rèn)為依靠定期驗(yàn)證即可,則必須準(zhǔn)備好完整的驗(yàn)證報(bào)告和風(fēng)險(xiǎn)評(píng)估資料�����,以應(yīng)對(duì)檢查官的挑戰(zhàn)���。
● 物料與倉(cāng)庫(kù)管理
1. 建議根據(jù)物料的特性(如蔗糖的吸濕性)來(lái)評(píng)估和規(guī)劃倉(cāng)庫(kù)布局�,確保存儲(chǔ)條件最優(yōu)���。物料接收SOP需要明確對(duì)外包裝的清潔消毒程序���、查驗(yàn)運(yùn)輸途中溫度記錄的要求。嚴(yán)格區(qū)分研發(fā)與商業(yè)用途的物料/產(chǎn)品�����,并用醒目的標(biāo)識(shí)和文件(如《研發(fā)物料臺(tái)賬》)進(jìn)行隔離與管理。
2. 建議在SOP中明確規(guī)定物料稱量后剩余物料的退庫(kù)程序�,包括密封要求、標(biāo)簽變更和賬務(wù)處理�。對(duì)標(biāo)簽等計(jì)數(shù)管理的包材,必須建立嚴(yán)格的收發(fā)存臺(tái)賬和計(jì)數(shù)復(fù)核程序�,確保賬物卡一致率100%。
迎檢不是“應(yīng)付檢查”���,而是對(duì)日常質(zhì)量管理水平的一次“體檢”和“校準(zhǔn)”�。成功的關(guān)鍵在于建立一個(gè)真正有效���、持續(xù)運(yùn)行的質(zhì)量體系���,并輔以充分、細(xì)致的準(zhǔn)備和開(kāi)放���、專業(yè)的溝通心態(tài)���。希望這份結(jié)合了實(shí)戰(zhàn)細(xì)節(jié)的經(jīng)驗(yàn)分享,能夠?yàn)檎诨蚣磳⑻ど戏坡少e國(guó)際認(rèn)證的同行們提供一份有價(jià)值的參考�。