12月16日���,FDA發(fā)布2025財年 483缺陷列表�。
本文從兩個維度對FDA 483缺陷項進行統(tǒng)計梳理���。一是2013-2025財年FDA 483各類別缺陷項出現(xiàn)頻次和比例����;二是對FDA在2025財年(2024年10月1日至2025年9月30日)發(fā)布的483中所涉及的所有缺陷項按照類別和出現(xiàn)頻次進行了排序�,從而幫助業(yè)界更清楚地了解FDA檢查的最新關注點和GMP檢查中最常出現(xiàn)的缺陷項,進而有針對性地進行自檢和迎檢工作���,提高合規(guī)水平���。
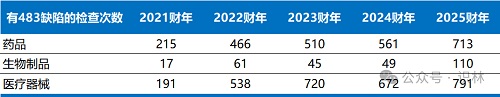
表1從藥品、生物制品���、醫(yī)療器械三個維度����,對比了近5個財年有483缺陷的檢查次數(shù),可以看到���,2025財年藥品���、生物制品、醫(yī)療器械的483缺陷相比于前幾個財年均有所增加���。
表1. 近5個財年有483缺陷的檢查次數(shù)對比
各類別缺陷項歷年出現(xiàn)頻次和比例統(tǒng)計
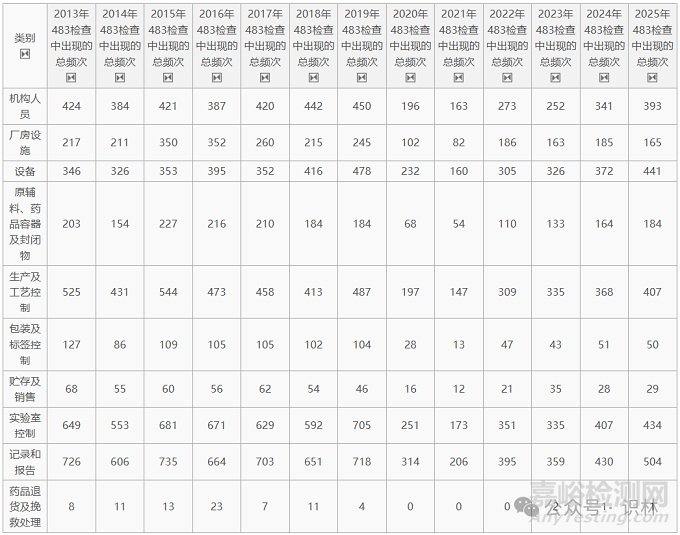
表2. 各類別缺陷項在歷年483中出現(xiàn)頻次統(tǒng)計表
由于新冠疫情導致FDA前幾年檢查數(shù)量明顯減少����,因此下表統(tǒng)計了各類別缺陷項在所有缺陷項中所占的比例�,這樣可以剔除掉檢查數(shù)量的影響,客觀反映各類別缺陷項在歷年中的比例變化�,即FDA近年來檢查關注點的變化(見表3)。
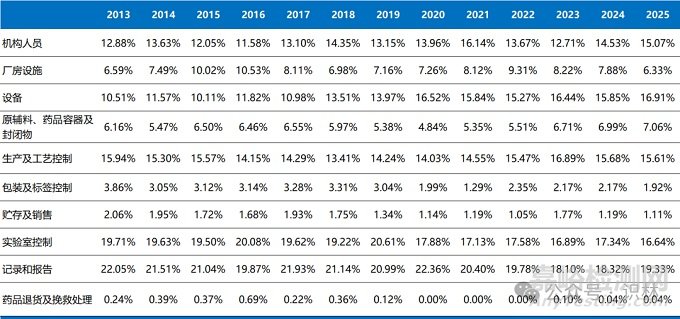
表3. 各類別缺陷項在歷年483中所占比例統(tǒng)計表
從表3中的統(tǒng)計結果來看���,設備����、實驗室控制����、記錄和報告、生產及工藝控制仍然是歷年占比較高的缺陷類別�,其中設備相關缺陷呈現(xiàn)明顯上升趨勢,從2013年的約10.5%逐步增長至2025年的16.9%����,這與我們此前的分析是一致的,尤其是“主批記錄的計算機化控制”相關缺陷上升趨勢明顯���。實驗室控制占比雖略有波動�,但始終維持在較高水平(約17%–20%)�,顯示其一直是質量體系中的關鍵環(huán)節(jié)。記錄和報告類缺陷在早期占比較高(2013年約22%)���,隨后整體呈緩降趨勢�,至2023–2025年穩(wěn)定在18%–19%左右�,說明該類問題雖仍重要,但相對有所改善�。此外,機構人員相關缺陷近年來也有上升趨勢���,體現(xiàn)了藥監(jiān)部門對質量部門職責的關注�,而廠房設施�、原輔料等類別占比相對較低且波動不大����。
2025財年各類別高頻缺陷項
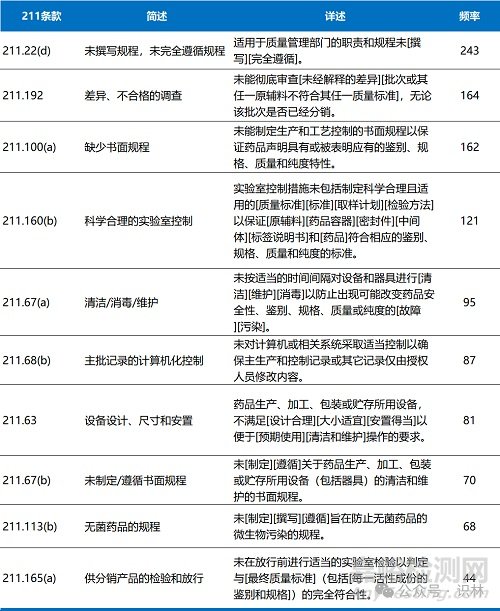
表4. 2025財年出現(xiàn)頻率最高的10類483缺陷項
2025財年與211有關的缺陷項分類�、簡述、詳述����、頻率以及具體條款,見下列各表����。(注:下列各表中僅列舉各類別中出現(xiàn)頻率較高的缺陷項類別,并非所有483缺陷項)
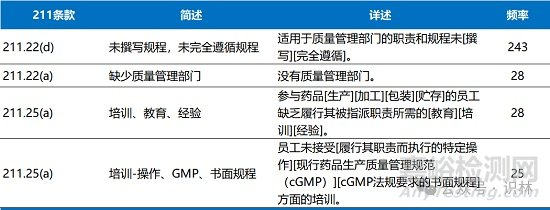
機構人員
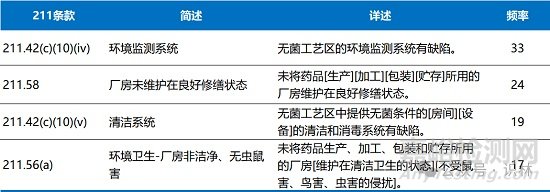
廠房與設施
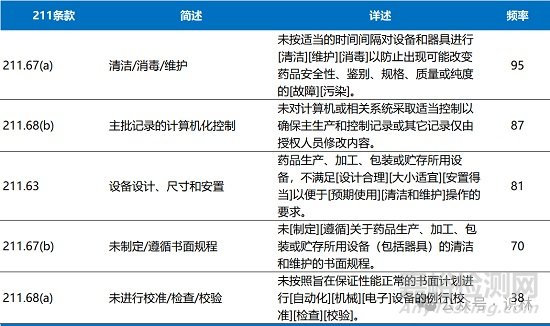
設備
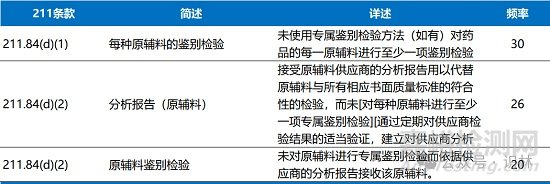
原輔料�、藥品容器及封閉物的控制
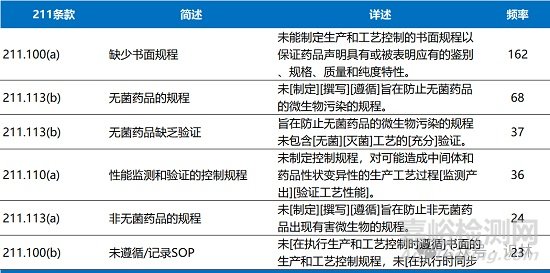
生產及工藝控制
包裝及標簽控制
貯存及銷售
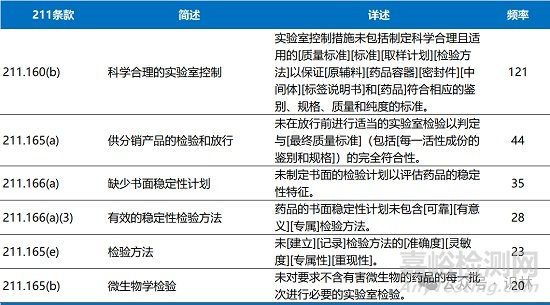
實驗室控制
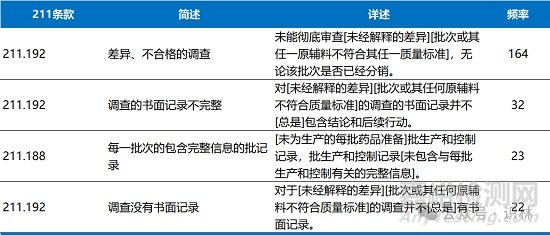
記錄和報告