飲用水一般由天然水或自來水經(jīng)相應(yīng)處理所得�����。天然水中通常含有少量溴離子�����,經(jīng)過處理后會產(chǎn)生溴酸鹽�����、有機溴化物(以溴代甲烷為主)等副產(chǎn)物�����。其中�����,溴酸鹽最受關(guān)注�����,該物質(zhì)被國際癌癥研究中心(IARC)定為2B級潛在致癌物�����。根據(jù)國家標準GB 5749—2022《生活飲用水衛(wèi)生標準》和 GB 8537—2018《食品安全國家標準 飲用天然礦泉水》規(guī)定�����,飲用水中溴酸鹽的質(zhì)量濃度不得超過0.01mg·L−1�����,該指標是飲用水安全重點監(jiān)控項目�����。
目前離子色譜法(IC)是溴離子和溴酸鹽的主流分析方法�����,根據(jù)檢測需求可配套選用電導(dǎo)檢測法、柱后衍生法�����、電感耦合等離子體質(zhì)譜法(ICP-MS)等�����。此外�����,文獻報道的方法還包括分光光度法�����、電化學(xué)法以及色譜-質(zhì)譜聯(lián)用法等�����。在IC應(yīng)用中�����,電導(dǎo)檢測法雖可實現(xiàn)µg·L−1級別的檢測靈敏度�����,但易受假陽性結(jié)果干擾�����;柱后衍生法則存在操作流程繁瑣�����、化學(xué)試劑危害性強且靈敏度受限等缺陷�����;而ICP-MS作為元素特異性檢測方法�����,兼具高靈敏度和優(yōu)異的選擇性�����,能有效彌補電導(dǎo)檢測器的技術(shù)缺陷�����,但因色譜分離時間較長,導(dǎo)致整體檢測通量較低�����。
基于飲用水中溴形態(tài)相對簡單的特性�����,研究人員采用固相萃取-ICP-MS測定飲用水中溴酸鹽的含量�����。在前處理過程中�����,分別使用Ag-改性堿性氧化鋁和酸性氧化鋁選擇性吸附溴離子和溴酸鹽�����,而有機溴化物不被吸附�����,然后用 5%(體積分數(shù)�����,下同)硝酸溶液洗脫被吸附的溴酸根離子�����,洗脫液再采用ICP-MS進行定量分析�����。該方法靈敏度高�����、選擇性好�����,適合于飲用水中溴酸鹽的測定以及溴的形態(tài)分析�����,尤其是樣品批次數(shù)較大時�����,分析速率優(yōu)勢更加明顯。
1 試驗方法
取200目中性氧化鋁粉末各約50g置于錐形瓶中�����,分別以100mL0.1mol·L−1鹽酸溶液和0.1mol·L−1氫氧化鈉溶液浸泡處理1h�����,超聲30min�����,棄去浸泡液�����,以水洗滌氧化鋁粉末至洗滌液呈中性�����,分別得到酸性氧化鋁和堿性氧化鋁�����。用0.1mol·L−1硝酸銀溶液浸泡堿性氧化鋁粉末1h�����,超聲 30min�����,棄去浸泡液�����,以水洗滌氧化鋁粉末至洗滌液中不含Ag+(以氯離子標準溶液檢測)即制得 Ag-改性堿性氧化鋁�����。取約2g上述處理好的兩種氧化鋁粉末制成兩種固相萃取柱�����,將50mL樣品以流量5mL·min−1依次過酸性氧化鋁柱�����、Ag-改性堿性氧化鋁柱�����,兩種固相萃取柱均用水沖洗一次,酸性氧化鋁柱再用5mL5%硝酸溶液洗脫兩次�����,每次5mL�����,合并洗脫液�����,按照儀器工作條件測定�����。
2 結(jié)果與討論
2.1 固相萃取條件的選擇
2.1.1 樣品流量
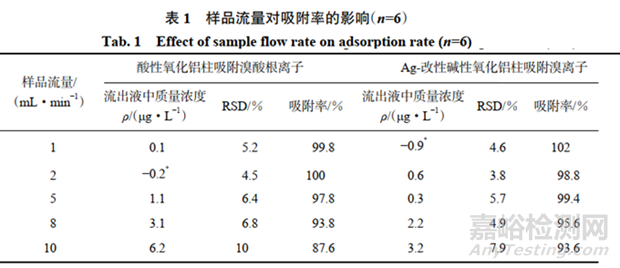
萃取過程是一個動態(tài)平衡過程�����,樣品流量越小�����,萃取率越高�����,但所需時間越長�����。為優(yōu)化萃取效果�����,以10mL含50.0μg·L−1的溴酸根離子和溴離子的樣品溶液為研究對象�����,當樣品流量從1mL·min−1增至10mL·min−1時�����,監(jiān)測水沖洗的流出液中目標離子的質(zhì)量濃度�����,計算相對標準偏差(RSD)和吸附率,結(jié)果如表1所示�����。其中�����,“*”表示所得質(zhì)量濃度接近儀器的檢出限�����,其與樣品空白的差值為負值�����,屬于儀器正常的波動�����。
由表1可知�����,當樣品流量不超過5mL·min−1時�����,溴酸根離子能被酸性氧化鋁定量吸附,而溴離子能被Ag-改性堿性氧化鋁柱完全吸附�����。而進一步試驗證明�����,在流量5 mL·min−1的條件下�����,酸性氧化鋁柱能夠定量吸附溴離子和溴酸根離子�����,而 Ag-改性堿性氧化鋁柱只能定量吸附溴離子�����,溴代烴不被這兩種材料吸附(10mL50μg·L−1的一氯二溴甲烷以5mL·min−1的流量通過兩種固相萃取柱時�����,在兩種吸附材料上的吸附率均低于1%)�����,這是將它們分離的基礎(chǔ)�����。因此�����,試驗選擇將樣品以流量5mL·min−1過固相萃取柱�����。
2.1.2 樣品體積
試驗中分別選擇10�����,20�����,50�����,80,100mL的含50.0μg·L−1溴酸根離子的樣品溶液�����,以流量5mL·min−1過固相萃取柱�����,測定流出液中目標離子的質(zhì)量濃度�����。結(jié)果顯示�����,樣品量不大于100mL時�����,固相萃取柱均能很好地吸附目標離子�����?����?紤]到樣品分析效率�����,試驗選擇樣品體積為50mL�����。如果在分析實際樣品時目標離子含量過小�����,可以適當增大樣品量�����,提高靈敏度�����。
2.1.3 洗脫劑和洗脫次數(shù)
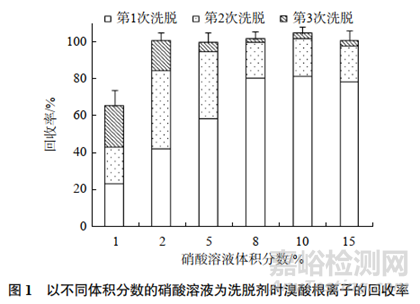
試驗考察了分別以體積分數(shù)為1%�����,2%,5%�����,8%�����,10%�����,15%的硝酸溶液為洗脫劑�����,每次5mL�����,連續(xù)洗脫3次�����,測定洗脫液中的目標離子�����,計算回收率�����,結(jié)果如圖1所示�����。
結(jié)果表明�����,酸性氧化鋁柱吸附的溴酸根離子必須分兩次(每次5mL)用 5%硝酸溶液洗脫定量回收�����,即使提高硝酸溶液體積分數(shù)也難以單次完全洗脫�����。因此�����,試驗選擇的洗脫劑為5%硝酸溶液,分兩次(每次5mL)洗脫�����。
2.2 干擾試驗
以溴酸根離子測定值相對誤差絕對值不大于5.0%為指標�����,試驗考察了飲用水中主要的陰離子如氯離子�����、硝酸根離子�����、硫酸根離子�����、氟離子�����、甲酸根離子�����、乙酸根離子對10.0µg·L−1溴酸根離子吸附的影響�����。結(jié)果表明�����,200mg·L−1硫酸根離子�����,100mg·L−1氯離子和硝酸根離子�����,10 mg·L−1 氟離子�����、甲酸根離子和乙酸根離子對酸性氧化鋁柱吸附溴酸根離子的行為無影響。亞氯酸鹽的干擾主要來自IC分離�����,而以 ICP-MS檢測則不存在亞氯酸鹽的干擾�����。此外�����,試驗還考察了溴代甲烷和溴離子對溴酸根離子測定的影響�����,結(jié)果顯示�����,1mg·L−1溴代甲烷及溴離子不干擾 10.0µg·L−1溴酸根離子的測定�����。在實際飲用水中�����,常見陰離子的質(zhì)量濃度通常為20~50mg·L−1�����,而溴離子�����、溴代甲烷(如一氯二溴甲烷�����、二氯一溴甲烷�����、三溴甲烷等)的質(zhì)量濃度均低于0.1mg·L−1�����,因此采用本方法時�����,飲用水中常見的陰離子和含溴物質(zhì)對目標離子的檢測無干擾�����。
2.3 標準曲線和檢出限
按照儀器工作條件測定溴酸鹽標準溶液系列�����,以溴酸鹽的質(zhì)量濃度為橫坐標�����,對應(yīng)的信號強度為縱坐標繪制標準曲線�����。結(jié)果顯示,溴酸鹽標準曲線的線性范圍為 0.5~500.0µg·L−1�����,線性回歸方程為y=374.2x+327.0�����,相關(guān)系數(shù)為 0.9992�����。
按照儀器工作條件測定樣品空白�����,并計算測定值標準偏差s�����,按3s得到溴酸鹽的檢出限為0.1µg·L−1�����。
2.4 精密度試驗
按照試驗方法平行測定5份加標樣品溶液(加標量為5.0µg·L−1)�����,計算測定值的RSD�����。結(jié)果顯示�����,測定值的RSD為 5.5%�����,說明方法精密度較好�����。
2.5 樣品分析
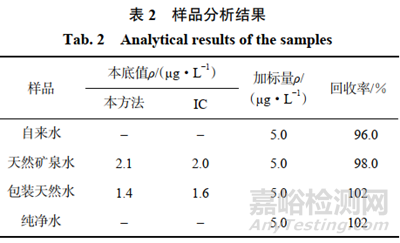
按照試驗方法測定飲用水中溴酸根離子的質(zhì)量濃度�����,并與GB 8538—2022《食品安全國家標準飲用天然礦泉水檢驗方法》中IC所得的測定結(jié)果進行對比�����,結(jié)果見表2。還對飲用水樣品進行加標回收試驗�����,計算回收率�����,結(jié)果見表2。
由表2可知�����,飲用水中溴酸根離子的回收率為96.0%~102%,本方法的測定結(jié)果與IC的基本一致�����。
3 試驗結(jié)論
研究人員采用固相萃取-ICP-MS測定飲用水中溴酸鹽的含量�����。該方法具有簡單�����、快速�����、穩(wěn)定�����、檢出限低等特點�����,滿足檢測要求�����,為飲用水中溴酸鹽的測定提供了一種科學(xué)可靠的確證手段�����。另外�����,制備的Ag-改性堿性氧化鋁柱對水中溴離子具有較高的吸附率�����,后續(xù)洗脫和定量方法有待進一步研究確定�����。
作者:蔡翠翠�����,段建坤�����,齊瓊�����,趙楊陽
單位:武漢產(chǎn)品質(zhì)量監(jiān)督檢驗所
來源:《理化檢驗-化學(xué)分冊》2025年第9期