摘要:開發(fā)共晶是改善藥物溶解性����、穩(wěn)定性和固態(tài)特性的一種技術手段�,在藥物開發(fā)中具有重要價值。國內外已有多個共晶藥物上市��。目前美國FDA 和歐洲EMA 對共晶的監(jiān)管框架有所不同����。我國尚無對共晶的技術要求。本文參考共晶藥物監(jiān)管現狀�,結合審評實際工作,從共晶結構確證�、關鍵理化性質、工藝研究及控制�、共晶質量研究幾個方面探討共晶藥學研究。
化合物的水溶性是藥物開發(fā)時重點考慮的基本理化特性之一����,據統(tǒng)計有40% 的候選藥物因水溶性較差制約其進一步成藥。目前已有多種技術手段用于解決水溶性差的問題����,包括成鹽、結構修飾����、微粉化�、固體分散體等��。近年來通過制備共晶( co-crystals)來提高藥物水溶性的研究也日益增多[1]�。
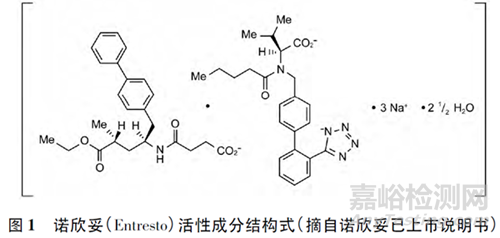
共晶由2 種或更多的組分通過非共價鍵( 如氫鍵、π-π 堆積作用和范德華力等) 以固定化學計量比的形式共存于同一晶格中��。這些組分包括活性成分( active pharmaceutical ingredient��,API) 和共晶形成物( co-crystal coformer�,CCF) ,通常溶劑化物或者水合物不認為是共晶����。需要關注的是,共晶各組分間通過非共價鍵��、非離子鍵互相作用�,但是各組分有可能還是離子形式,如諾欣妥( Entresto) �,其組分沙庫巴曲和纈沙坦通過氫鍵等作用形成了共晶,同時纈沙坦結構中的羧酸仍與鈉成鹽��。諾欣妥的結構式見圖1。根據晶格中組成物質的不同����,目前共晶主要包括2 種類型����,以活性成分相互作用形成的共晶( 即藥物-藥物共晶) ,和以活性成分與非活性成分相互作用形成的共晶( 即藥物-非活性成分共晶) �。
共晶能夠改善藥物的理化特性,如溶解度��、溶出速率��,改善藥物體內行為����,實現提高有效性、降低毒性的目的[2 - 3]�。此外,共晶優(yōu)良的固態(tài)特性和穩(wěn)定性��,也可以提高制劑生產的可行性�。從專利角度,共晶可擴大化合物專利的保護范圍�,延長專利保護期[4],這也成為制藥公司開發(fā)共晶的原因之一。但仍需清楚地認識到��,相比傳統(tǒng)藥物��,共晶的篩選難度大��、制備方法有限����,這些都制約了該技術的發(fā)展。但經過多年的技術積累�,對共晶藥物的研究也不斷增加,近年已有多個共晶藥物獲批上市����。本文擬通過分析國外對共晶藥物的監(jiān)管要求,探討目前共晶藥物藥學研究的重點��,旨在為我國共晶藥物的開發(fā)和藥學研究提供參考����。
1 共晶監(jiān)管現狀
美國FDA 在2018 年正式發(fā)布《藥物共晶監(jiān)管指南》[5],美國FDA 認定共晶類似于新的多晶型而非新的API����。由2 個或2 個以上已獲批API 組成的共晶作為復方制劑監(jiān)管�,而非新的API��。歐洲EMA并未發(fā)布共晶指導原則��,但是發(fā)布了關于藥物共晶的思考文件�。歐洲EMA 的監(jiān)管立場與美國FDA 相似����,共晶不被認為是全新的API。歐洲EMA 認為共晶中API 和CCF 之間存在非共價鍵的弱相互作用����,其在胃腸道環(huán)境中能夠快速釋放API,這種情況與結晶性API����、鹽、水合物或者溶劑化物類似����。共晶不需要作為新API( new active substance) 程序進行審評,除非在安全性��、有效性顯示出差異[6]����。WHO 發(fā)布的《國際藥典》〈Polymorphism〉章節(jié)對于共晶的認識與美國FDA 基本一致[7]��,但并未就共晶提出明確技術要求��。
《中華人民共和國藥典》四部通則9015 定義共晶為由2 種或2 種以上的化學物質共同形成的晶態(tài)物質��,并明確共晶屬于晶型物范疇��。目前我國并未發(fā)布共晶的注冊分類和技術要求����。
2 已上市及研究中的共晶藥物
前文所述����,共晶包括藥物-藥物共晶和藥物-非活性成分共晶2 種形式。已上市藥物-藥物共晶有2種藥品��,分別為諾欣妥( Entresto) 和Seglentis��。諾欣妥用于治療心力衰竭和高血壓��,活性成分是沙庫巴曲纈沙坦鈉��,由腦啡肽酶抑制劑沙庫巴曲和血管緊張素受體阻滯藥纈沙坦以1 ∶ 1 的摩爾比形成共晶����,是一種具有特定化學和晶體結構的超分子復合物[8]�。與沙庫巴曲/纈沙坦的物理混合物相比��,其生物利用度明顯提高[9]�。Seglentis 用于治療急性疼痛,是鹽酸曲馬多和塞來昔布摩爾比1∶ 1的共晶��,與單獨或藥物混合物相比����,曲馬多的溶解速度變慢��,塞來昔布的溶解速度加快[10 - 11]��,提高了塞來昔布體內的血漿濃度����,改善塞來昔布和曲馬多的藥動學特性[12]。
藥物-非活性成分的共晶藥物代表為“格列凈”類����,如伊格列凈、艾托格列凈�、加格列凈�、恒格列凈等�,多以L-脯氨酸作為CCF[13]。藥物-非活性成分的共晶常見CCF 包括羥酸類����、胺類和醇類。已有報道使用己二酸�、苯甲酸、丙二酸����、阿斯巴甜、尿素����、氨基酸、甘露醇等幾十種物質作為CCF 制備共晶����。從結構上看,氨基酸是藥物-非活性成分類共晶具有前景的共形成物候選物��,因為其具有能夠形成氫鍵并通過兩性離子基團增加穩(wěn)定性的功能基團��,有助于形成共晶�,而且氨基酸是一種安全的非活性成分[14]�。代表性已上市共晶藥物和已有研究藥物見表1 和表2�。
3 藥學研究思考
已有研究顯示共晶開發(fā)的方法包括基于pKa模型、劍橋結構數據庫����、漢森溶解度參數等[1]。此外也有報道人工神經網絡等新興技術在共晶預測方面的應用[16]����。對于非活性成分的CCF,開發(fā)中需關注API 和CCF 的相容性�,通常應該選擇無藥理活性、有安全支持依據的物質作為CCF����,避免影響活性成分的藥理活性或引入安全性風險��。CCF 的篩選應是共晶藥物開發(fā)的重點工作�,建議利用計算機模擬技術,開展大量不同種類的CCF 篩選和比對�,選擇理化穩(wěn)定、固體特性符合要求的共晶��。相比藥物-非活性成分類共晶�,藥物-藥物類共晶相關開發(fā)更具挑戰(zhàn)性��,不僅要考慮藥物-藥物相互作用�,而且也需要結合藥物體內發(fā)揮藥效的機制�、臨床用法用量等因素綜合確定共晶各活性成分比例的合理性。
共晶藥物從開發(fā)早期��,就需要明確需要獲得何種關鍵質量特性的共晶��,例如: 具備優(yōu)良的溶解性��、固體特性�、穩(wěn)定性或者具有一定藥物比例的多組分藥物組合等。共晶藥物表現出與其各組分物理混合物不同的理化特性�,某些理化性質可能影響藥物吸收,從而影響安全性和有效性����。已有類似結構或者共晶組合的研究對于共晶開發(fā)參考意義重大,建議開發(fā)前系統(tǒng)梳理已有研究資料��,為共晶藥物后續(xù)篩選�、理化性質預測、工藝開發(fā)提供指導����。在確定目標共晶的前提下����,應就共晶的結構確證��、理化特性研究��、生產工藝及質量控制進行系統(tǒng)全面的研究�。
3. 1 共晶結構確證
結合國外共晶監(jiān)管要求,證明藥物形成共晶的主要策略包括: ① 證明各組分在同一晶胞中��。② 如果API 和CCF 都具有可電離官能團����,需證明它們在共晶中以非離子方式相互作用。判定方法是API 和CCF 的ΔpKa < 1��,或使用光譜法和其他方法補充證明�。③ 確保API 在到達藥理作用部位之前從共晶形式中實質解離出來��,一般使用體外溶出或溶解度方法證明[5]��。建議藥學研究中要對以上3 個方面的內容都進行研究和論述�。
從具體的技術手段來看,單晶X 射線衍射( Xray diffraction����,XRD) 是確認共晶最直觀的方法�,可以提供共晶詳細的晶型數據��、組分間結合類型等信息����。建議共晶培養(yǎng)選擇合適的溶劑體系,并與實際結晶工藝體系對比研究����,確認所制備單晶樣品的代表性。單晶X 射線衍射需要培養(yǎng)一定尺寸的單晶����,但很多藥物并不一定能形成所需尺寸的單晶,甚至不能形成單晶�。對于難以獲得單晶的共晶,微晶電子衍射( microcrystal electron diffraction�,MicroED) 技術通過降低單晶制備要求呈現出較大優(yōu)勢。通過計算機模擬提供共晶的結構信息��,并且生成模擬的X射線衍射圖��,可與實際樣品的粉末X 射線衍射的特征衍射峰對比,對于共晶確證提供較為重要的信息�。
除單晶衍射外,建議采用多種技術手段進一步佐證共晶結構����。固態(tài)核磁可用來分析共晶的結構信息,通常能夠識別共晶氫鍵等特征結合方式�,是共晶結構表征的重要補充[17]。另外��,也可以采用光譜技術進行共晶表征����,包括紅外光譜、拉曼光譜等����,主要用于識別化學鍵和分子間相互作用類型、質子轉移情況����。場發(fā)射掃描電子顯微鏡用于研究共晶的表面形態(tài)學,提供共晶體的顯微照片����。熱分析方法包括差示掃描量熱法和熱臺顯微鏡法,結合顯微鏡和熱分析����,研究固體形式的物理化學特性,如熔點����、熔程和結晶轉變等,對于共晶和物理混合物具有較好的區(qū)分能力[18]�。上述方法不僅是定性方法,也具備定量的能力����,如測定目標共晶中游離API 雜晶和其他結晶的比例。
在共晶結構表征應重點對目標共晶�、API 和CCF 的物理混合物、單獨的API 和單獨的CCF 依次采用上述表征技術進行比對研究����,分析不同物質間各檢測方法結果的異同,綜合判斷是否形成共晶��。其確證重點是分子量��、相互作用位點等與共晶形成密切相關的信息��。實際審評中發(fā)現,采用紅外光譜( infrared spectroscopy��, IR) ��、拉曼光譜( raman spectroscopy����,RM) 、固態(tài)核磁譜( nuclear magnetic resonance spectroscopy�,NMR) 、熱分析等方法對共晶����、API 以及物理混合物測定后,對分析結果的解讀過于簡單��,甚至認為共晶��、API 以及物理混合物測定結果不同����,就證明形成的必然是共晶,缺乏理論結合數據的分析����。MicroED 技術在共晶中的應用以及研究尚少��,其在共晶結構表征中的可靠性仍待繼續(xù)觀察。
3. 2 關鍵理化特性研究
共晶表現出與游離API或者其他晶型不同的固態(tài)特性和理化性質��,如溶解度和溶出度�,其主要影響因素是晶型和粒度。建議開展目標共晶中加標游離API 或者其他晶型��、不同粒徑共晶比較研究����,確認在不同介質中的溶解度或溶出度,為雜晶及粒度限度制定提供支持依據����。對于存在溶解或溶出過程中API 重結晶的情況,更需要慎重考慮重結晶對體內行為的影響�,積累體內外研究數據。必要時可能要開展生物等效性研究確認共晶和游離API 或者其他晶型����、不同粒徑共晶的體內行為,論述游離API 或者其他晶型��、粒徑對安全性和有效性產生的潛在風險��。對于熱熔擠出制備共晶的工藝,熔點也是一個重要的理化指標��。
3. 3 工藝研究及控制
共晶常見的制備方法通??煞譃? 種: 共研磨法、溶劑法( 蒸發(fā)法�、結晶法等) ,此外超臨界流體結晶����、微波誘導結晶技術、熱熔擠出法等也可以用于制備共晶�,但應用范圍相對較小[19 - 20]����。工藝研究的重點是基于對共晶熱力學和動力學行為的深入理解,結合實際開發(fā)中對不同條件的篩選研究確認最終共晶結晶方法及工藝參數����。工藝開發(fā)過程中需要重點識別影響目標共晶的工藝條件,確保工藝參數波動能夠始終生產出符合質量要求的目標共晶�。以溶劑結晶工藝為例,建議在申報資料開發(fā)部分重點就API 與CCF 的投料比����、溶劑體系選擇依據進行論述�,確保在合適的控制范圍內僅生成共晶�,而非其他晶型( 如游離堿晶型、共晶形成物結晶等) ����。另外建議對結晶的晶種控制����、投料速度、結晶溫度��、攪拌參數��、攪拌設備�、干燥溫度等可能影響共晶形成的工藝參數進行研究,確認合理的控制范圍�,確保能持續(xù)穩(wěn)定生產出目標共晶。
3. 4 共晶質量研究
與傳統(tǒng)化學藥物一樣��,共晶的質量研究也需要包括理化特性����、雜質研究、含量研究等方面����。由于結構原因�,共晶的主要特點是其在儲存以及制劑過程中可能會失去CCF 變成游離API����。API 可能呈現晶型、無定形或者液態(tài)����。另外,過去認為共晶藥物不傾向于形成多晶型[21]�,然而后續(xù)不斷研究發(fā)現,共晶與單組分藥物的多晶型相似��,可能產生不同類型的共晶[22]��。共晶不同晶型間��、共晶與API 可能表現出不同理化特性����,進而影響藥物體內釋放和吸收[23]。因此共晶質量研究的重點在于確保共晶在生產及儲存過程中晶型的穩(wěn)定可控�。理想的狀態(tài)是共晶始終保持穩(wěn)定[24]。對于確實存在共晶轉化的情況,需充分了解與驗證共晶轉化的條件�、類型和比例,并從生產工藝��、生產環(huán)境����、包裝系統(tǒng)、貯藏條件多方面控制��。必要時需開展不同共晶轉變類型和比例的體內研究�,為共晶的轉變及比例提供支持依據�。
結合共晶知識以及開發(fā)研究數據的積累,通過不同的篩選技術盡可能獲得共晶藥物及其API 的潛在形態(tài)��,特別是API 晶型�,篩選優(yōu)勢晶型,對各種晶型的產生條件�、理化性質進行深入研究,采用風險評估的方式確認潛在不同晶型對產品質量以及安全性和有效性的影響��,例如: 溶解性相差較大����,可能對體內行為影響更大,則風險較高。其次�,建議開發(fā)具有一定檢測靈敏度的方法確認共晶并有效區(qū)分雜晶或其他形態(tài)。重點關注原料藥和制劑生產過程中��、穩(wěn)定性期間目標晶型的穩(wěn)定性��,積累多批次樣品晶型數據��。建議收集單晶衍射數據計算理論的粉末衍射圖譜����,或直接以所培養(yǎng)的單晶進行粉末X 衍射,采用疊加圖譜形式與多批次樣品的粉末衍射圖譜的對比����,進一步確認共晶的一致性及穩(wěn)定性[25]。
4 展望
2021 年國家發(fā)展改革委員會印發(fā)《“十四五”生物經濟發(fā)展規(guī)劃》的通知����,文件明確提及鼓勵發(fā)展基于人工智能的藥物結晶。從共晶形成的分子機制層面�,高通量、預測性及人工智能在共晶開發(fā)中具有良好發(fā)展基礎�。最新的研究表明,計算機輔助共晶設計在生成模型��、物理性能預測和優(yōu)化方面取得了顯著進展。GEMCODE( generative method for co-crystaldesign) 是一種基于深度生成模型和優(yōu)化的自動共晶篩選新型方式�,可實現共晶至固體制劑的全程開發(fā)指導。機器學習模型( machine learning models) 在共晶預測中的應用已經取得一些進展��,但大多數研究集中在已知共晶的性質預測上����。此外,利用3D分子構象信息�,通過增強共晶預測的準確性,快速篩選出潛在的CCF[26]��。人工智能在共晶中的研究依賴于大量的數據支持����,另外共晶研究涉及化學����、物理學以及藥學多個學科融合[27],各學科與人工智能整體協同發(fā)展仍需進一步加強�。隨著技術發(fā)展,人工智能在藥物共晶領域的應用會成為極具潛力的研究方向��。
參考文獻
[1] RAHEEM THAYYIL A����,JUTURU T��,NAYAK S����,et al. Pharmaceuticalco-crystallization: regulatory aspects��,design��,characterization����,and applications[J]. Adv Pharm Bull,2020��,10( 2) :203 - 212.
[2] CHETTRI A����,SUBBA A,SINGH GP��,et al. Pharmaceutical cocrystals:a green way to enhance drug stability and solubility forimproved therapeutic efficacy[J]. J Pharm Pharmacol�,2024,76( 1) : 1 - 12.
[3] TIAN ZH�,MAI YP�,MENG TT�,et al. Nanocrystals for improvingoral bioavailability of drugs: intestinal transport mechanisms and influencing factors[J]. AAPS Pharm Sci Tech,2021�,22( 5) : 179.
[4] KUMAR A,KUMAR S�,NANDA AR. A review about regulatorystatus and recent patents of pharmaceutical co-crystals[J]. AdvPharm Bull,2018����,8( 3) : 355 - 363.
[5] FDA. Regulatory Classification of Pharmaceutical Co-Crystals;Guidance for Industry[EB/OL]. ( 2018 - 02) [2024 - 12 - 07].https: / /www. fda. gov /files /drugs /published /Regulatory-Classification-of-Pharmaceutical-Co-Crystals. pdf.
[6] EMA. Guideline on the investigation of co-crystals of active substances[EB/OL]. ( 2015 - 07 - 16) [2024 - 12 - 07]. https: / /www. ema. europa. eu /en /use-cocrystals-active-substances-medicinal-products-scientific-guideline.
[7] WHO. Polymorphism The International Pharmacopoeia[EB/OL].( 2022) [2024 - 12 - 07]. https: / /www. drugfuture. com/Pharmacopoeia/PhInt11 /data /10. 3. 5. Polymorphism. pdf.
[8] FDA. Drugs@ FDA: FDA-Approved Drugs[EB/OL]. ( 2024 -04 - 12) [2024 - 12 - 07]. https: / /www. accessdata. fda. gov/drugsatfda _ docs/label /2024/218591Orig1s000,207620Orig1s025lbl.pdf.
[9] BERG DD��,BRAUNWALD E����,DEVORE AD,et al. Efficacyand safety of sacubitril /valsartan by dose level achieved in the PIONEER-HF trial[J]. JACC Heart Fail����,2020,8( 10) : 834 -843.
[10] FDA. Drugs@ FDA: FDA-Approved Drugs[EB/OL]. ( 2021 -10 - 15) [2024 - 12 - 07]. https: / /www. accessdata. fda. gov /drugsatfda_docs /label /2021 /213426s000lbl. pdf.
[11] PORT A��,ALMANSA C��,ENRECH R����,et al. Differential solution behavior of the new API-API co-crystal of tramadol-celecoxib( CTC) versus its constituents and their combination[J]. CrystGrowth Des,2019�,19( 6) : 3172 - 3182.
[12] VISCUSI ER,LANGFORD R�,MORTE A,et al. Safety of cocrystal of tramadol-celecoxib ( CTC) in patients with acute moderate-to-severe pain: pooled analysis of three phase 3 randomizedtrials[J]. Pain Ther����,2024,13( 6) : 1617 - 1631.
[13] 趙盼盼����,谷君,許崢嶸�,等. 藥物共晶技術在2 型糖尿病治療藥物研發(fā)中的作用研究進展[J]. 山東醫(yī)藥,2023��,63( 24) : 107 - 110.
[14] NUGRAHANI I�,JESSICA MA. Amino acids as the potential coformerfor co-crystal development: a review[J]. Molecules,2021����,26( 11) : 3279.
[15] DEVI P,BUDHWAR V��,KAKKAR S,et al. Pharmaceutical cocrystallization:strategies for co-crystal design: pharmaceutics
[J]. Int J Life Sci Pharm Res�,2023,13( 6) : 87 - 105.
[16] DEVOGELAER JJ�,MEEKES H,TINNEMANS P��,et al. Cocrystalprediction by artificial neural networks[J]. Angew ChemInt Ed�,2020,59( 48) : 21711 - 21718.
[17] 陳婷����,李琦,劉琪文��,等. 固態(tài)核磁共振技術在晶型藥物研究中的應用[J]. 醫(yī)藥導報�,2022,41( 5) : 655 - 663.
[18] RAJENDRAN MAP��,ALLADA R����,SAJID SS. Co-crystals for genericpharmaceuticals: an outlook on solid oral dosage formulations[J]. Recent Adv Drug Deliv Formul,2021��,15( 1) : 15 -36.
[19] CHAVAN RB��,THIPPARABOINA R��,YADAV B����,et al. Continuousmanufacturing of co-crystals: challenges and prospects[J].Drug Deliv Transl Res,2018����,8( 6) : 1726 - 1739.
[20] BISCAIA IFB,GOMES SN��,BERNARDI LS�,et al. Obtaining cocrystals by reaction crystallization method: pharmaceutical applications[J]. Pharmaceutics,2021�,13( 6) : 898.
[21] KAVANAGH ON,CROKER DM�,WALKER GM,et al. Pharmaceutical cocrystals: from serendipity to design to application[J]. Drug Discov Today�,2019,24( 3) : 796 - 804.
[22] 范瑩����,李敏,楊楠�,等. 藥物共晶研究進展[J]. 中國藥業(yè)��,2022����,31( 6) : 1 - 6.
[23] BOLLA G�,SARMA B,NANGIA AK. Crystal engineering of pharmaceutical cocrystals in the discovery and development of improved drugs[J]. Chem Rev�,2022,122( 13) : 11514 - 11603.
[24] 潘靜��,黃曉龍. 藥物共晶技術研究進展及藥學研究思考[J].中國新藥雜志�,2025,34( 5) : 477 - 482.
[25] 鄧雪珍��,陳樂樂����,譚雨夢,等. 氫氯噻嗪-氟胞嘧啶共晶的制備�、表征及溶解性考察[J]. 中國醫(yī)藥工業(yè)雜志,2024��,55( 1) : 113 - 119�,131.
[26] ESSEN CV,LUEDEKER D. In silico co-crystal design: assessment of the latest advances[J]. Drug Discov Today,2023�,28( 11) : 103763.
[27] 沙莎,吳麗莎��,劉桂永��,等. 地拉羅司-煙酰胺共晶的制備�、表征及性質研究[J]. 中國現代應用藥學�,2025,42( 6) : 965 -969.
內容來源:中國新藥雜志2025 年第34 卷第22 期