2025年版《中國藥典》于2025年10月1日起正式實施,其中四部新增通則1109洋蔥伯克霍爾德菌群檢查法,這一變革在我國藥品微生物質(zhì)量控制領(lǐng)域具有重大意義���。具體內(nèi)容如下:
潛在危害的微生物
在四部通則1107非無菌藥品微生物限度標準中表明,本限度標準所列的控制菌對于控制某些藥品的微生物質(zhì)量可能并不全面����,因此���,對于原料����、輔料及某些特定的制劑����,根據(jù)原輔料及其制劑的特性和用途、制劑的生產(chǎn)工藝等因素�,可能還需檢查其他具有潛在危害的微生物����。
洋蔥伯克霍爾德菌群
洋蔥伯克霍爾德菌群(Burkholderia cepacia complex,Bcc)作為一種典型的不可接受微生物,多年來一直被FDA和制藥行業(yè)所關(guān)注和研究����,因Bcc污染而導致的非無菌產(chǎn)品召回事件層出不窮。此前各國藥典中僅美國藥典收載了Bcc檢查法章節(jié),即USP <60> Microbiological Examination of Nonsterile Products—Tests for Burkholderia CepaciaComplex.
《中國藥典》2025年版四部通則1109
洋蔥伯克霍爾德菌群檢查法
方法介紹
洋蔥伯克霍爾德菌群
洋蔥伯克霍爾德菌群(Burkholderia cepacia complex����,Bcc)由二十多種表型近似����、基因型存在差異的菌種組成����。本方法中選擇以下具有代表性的3株Bcc菌株作為培養(yǎng)基適用性試驗和檢查方法適用性試驗的試驗菌株���。
洋蔥伯克霍爾德菌(Burkholderia cepacia)
〔CMCC(B)23005〕
新洋蔥伯克霍爾德菌(Burkholderiacenocepacia)
〔CMCC(B)23006〕
神秘伯克霍爾德菌(Burkholderia aenigmatica)
〔CMCC(B)23010〕
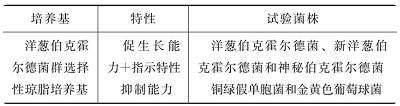
培養(yǎng)基及培養(yǎng)基適用性檢查
檢查方法適用性試驗
供試液制備:取供試品�,照非無菌產(chǎn)品微生物限度檢查:微生物計數(shù)法(通則1105)制成1∶10供試液。取相當于1g����、1ml���、1貼或10cm2供試品的供試液���,和不大于100cfu的試驗菌(洋蔥伯克霍爾德菌����、新洋蔥伯克霍爾德菌和神秘伯克霍爾德菌)接種至適宜體積的胰酪大豆胨液體培養(yǎng)基或適當稀釋的胰酪大豆胨液體培養(yǎng)基中(如對制藥用水進行檢驗時,可考慮用稀釋10倍的胰酪大豆胨液體培養(yǎng)基)���,混勻����,按照檢查方法,在規(guī)定的溫度和最短時間下培養(yǎng)����,應能檢出所加試驗菌相應的反應特征����。
結(jié)果判斷:各試驗菌若在上述試驗中均被檢出,按此供試液制備方法和檢查方法進行供試品檢查�。
供試品檢查
供試品的檢查應按經(jīng)方法適用性試驗確認的方法進行�。
陽性對照試驗:實驗室綜合評估確定日常檢驗過程中陽性對照試驗的必要性����、頻次及其他要求�。根據(jù)方法適用性試驗結(jié)果,選擇1株試驗菌作為陽性對照菌株���,陽性對照試驗應檢出相應的試驗菌�。
陰性對照試驗:以稀釋劑代替供試液照相應檢查法檢查�,陰性對照試驗應無菌生長。如果陰性對照有菌生長���,應進行調(diào)查����。
供試液制備和增菌培養(yǎng):取供試品���,照非無菌產(chǎn)品微生物限度檢查:微生物計數(shù)法(通則1105)制成1∶10供試液。取相當于1g�、1ml���、1貼或10cm2供試品的供試液����,接種至適宜體積(經(jīng)方法適用性試驗確定)的胰酪大豆胨液體培養(yǎng)基或適當稀釋(經(jīng)方法適用性試驗確定)的胰酪大豆胨液體培養(yǎng)基中(如對制藥用水進行檢驗時,可考慮用稀釋10倍的胰酪大豆胨液體培養(yǎng)基進行增菌培養(yǎng))����,混勻,30~35℃培養(yǎng)48~72小時�。
選擇和分離培養(yǎng):取上述培養(yǎng)物劃線接種至洋蔥伯克霍爾德菌群選擇性瓊脂培養(yǎng)基平板上�,30~35℃培養(yǎng)48~72小時。
結(jié)果判斷:若洋蔥伯克霍爾德菌群選擇性瓊脂培養(yǎng)基上有菌落生長����,如表現(xiàn)為下表中的生長特征等���,應進行分離���、純化����,并采用適宜的鑒定試驗,確證是否為洋蔥伯克霍爾德菌群����;若洋蔥伯克霍爾德菌群選擇性瓊脂培養(yǎng)基上沒有菌落生長����,或有菌落生長但鑒定結(jié)果為陰性���,判供試品未檢出洋蔥伯克霍爾德菌群���。