大家應該對ISO 14971并不陌生,但是對ISO/TR 24971可能并不熟悉�,我們今天跟大家說一下24971和14971的聯(lián)系。在新改版的ISO 14971:2019中��,已經(jīng)將很多以前屬于附錄的內(nèi)容調(diào)整到ISO/TR 24971中了����,我們不僅要關注ISO 14971:2019,還要關注ISO/TR 24971��,ISO/TR 24971是ISO 14971:2019的指南文件��。ISO 14971:2019版的風險管理標準和ISO/TR 24971:2020有非常緊密的聯(lián)系�。
24971正文有10個章節(jié)和8個附錄,14971改版后新版標準的附錄大幅減少����,附錄基本都挪到 24971中去了����,把14971標準和24971緊密聯(lián)系在一起�。
在2019年5月,國際標準化組織官方發(fā)布消息�,ISO/TR 24971-2020 醫(yī)療器械風險管理對 ISO 14971 應用指南 Medical devices — Guidance on the application of ISO 14971正式生效。
本標準提供幫助制造商在開發(fā)����、實施和保持醫(yī)療器械的風險管理過程的指南,旨在滿足ISO14971:2019《醫(yī)療器械-風險管理對醫(yī)療器械的應用》的要求。本標準為ISO14971:2019在各種醫(yī)療器械上應用提供指南這些醫(yī)療器械包括有源的�、無源的、植入的和非植入的,以及作為醫(yī)療器械的軟件和體外診斷醫(yī)療器械�。
2.ISO/TR 24971的具體內(nèi)容
1.范圍
ISO/TR24971根據(jù)ISO14971:2019標準,為醫(yī)療器械風險管理過程的開發(fā)、實施和保持提供指南����。
2.術語和定義
ISO 14971:2019中給出的術語和定義也適用于ISO/TR24971��。
可用于標準化工作的ISO和IEC術語數(shù)據(jù)庫,網(wǎng)址如下:
ISO在線瀏覽平臺:
http:/www.iso.org/obp
IEC電子百科:
http://www.electropedia.org
3.風險管理流程
14971要求制造商在醫(yī)療器械的整個生命周期內(nèi)建立����、實施、記錄和維護持續(xù)的風險管理流
程�。14971給出了這一過程中所需的要素和最高管理層的職責�,并在ISO/TR24971中作了更詳細的解釋����。風險管理的一般流程,分析��、評價����、控制、綜合剩余風險可接受性評價�、生產(chǎn)及生產(chǎn)后活動。
4.風險管理計劃
風險管理計劃描述了風險管理活動的范圍�、所涉及人員的職責和權限、風險可接受性的標準��、要為醫(yī)療器械收集和審查的生產(chǎn)和生產(chǎn)后信息�,以及在整個產(chǎn)品生命周期內(nèi)進行的所有風險管理活動。
風險管理計劃是一份“動態(tài)文件”�,在醫(yī)療器械的整個生命周期內(nèi),當有新信息可用時�,將對其進行審查和更新。應持續(xù)收集信息��,即使在最后一臺醫(yī)療器械售出并投放市場后也應如此����。
5.風險分析
制造商應根據(jù)預期用途�、合理可預見的誤用以及正常和故障條件下與安全相關的特性��,識別和記錄與醫(yī)療器械相關的已知和可預見的危險�。
示例:一次性醫(yī)療器械設計為僅使用一次,但可以合理預見的是��,某些用戶可能會嘗試重復使用該醫(yī)療器械�。因此,隨附文檔中包括了針對重復使用的警告和因重復使用而可能產(chǎn)生的危害的指示��。根據(jù)IEC62366-1的可用性工程應用證明此安全信息將是有效的��,即用戶將知道正確的使用并了解重復使用醫(yī)療器械的風險��。然而��,可用性評估也顯示�,一些用戶可能會忽視這些信息,并故意重復使用醫(yī)療器械����。有意的重用可以被認為是不正常的使用�,這超出了可用性工程過程的范圍�,因為相關的風險無法在用戶界面中控制.由于這種行為可被視為可合理預見的誤用����,因此在風險管理過程中分析了這種重復使用的風險,并根據(jù)IS0 14971 的風險可接受性標準進行了評估��??赡苡斜匾谟脩艚缑嬷鈱嵤╋L險控制措施。
6.風險評價
ISO 14971:2019規(guī)定了風險評價的過程��。但此標準并未規(guī)定可接受風險的水平�。風險可接受性準則基于制造商的判定可接受風險的方針,并以文件的形式記錄在風險管理計劃中在風險評價中,制造商將估計的風險與風險可接受性準則進行對比從而決定這些準則是否得到滿足。在風險評價中風險可接受性準則的應用示例和進一步指南請見ISO/TR24971附錄C�。
7.風險控制
風險控制方案,存在多種方案來降低與醫(yī)療器械相關的風險����。這些方案既可單獨使用也可聯(lián)合使用。制造商可以研究不同的方案,以合理可行的方式將風險降低到可接受的水平��。如ISO14971:2019中所強調(diào)的,優(yōu)先順序很重要��。
受益風險分析��,如果使用風險管理計劃中建立的標準不能判定剩余風險是可接受的����,并且進一步的風險控制是不可行的����,制造商可以收集和審查數(shù)據(jù)和文獻��,以確定預期使用的受益是否大于剩余風險��。
制造商還需要確定是否還有他們必須符合的法規(guī)要求,如歐盟的MDR����,其中的附加要求可能超出了本標準的規(guī)定。在ISO/TR 24971:2020第7.4條增加了近3頁�,包括廣泛的收益和收益-風險分析,包含了那些不涉及經(jīng)濟或商業(yè)優(yōu)勢的收益�。第7.4.5條列舉了收益-風險分析結論的三個具體例子,第7.4.2條提供了大量的臨床收益的概述����。
8.綜合剩余風險
ISO 14971:2019要求根據(jù)醫(yī)療器械預期使用的益處評估總體剩余風險,并且風險管理計劃中應包括總體剩余風險的可接受標準和總體剩余風險的評估方法����。
總體剩余風險的評估是從更廣的角度來看待剩余風險。已評估了所有確定的危險情況,并根據(jù)效益-風險分析將所有風險降低至可接受水平或予以接受?���,F(xiàn)在�,制造商要考慮的是,與醫(yī)療器械整體相關的總體剩余風險是否符合總體剩余風險的可接受標準����。此考慮因素考慮了與醫(yī)療器械預期用途的益處相關的所有剩余風險的貢獻。對于復雜的醫(yī)療器械和具有大量個人風險的醫(yī)療器械��,此步驟尤為重要����。通過評估可以得出醫(yī)療器械安全的結論。
在ISO/TR24971中給出了綜合剩余風險的評估示例����。
9.生產(chǎn)和生產(chǎn)后活動
生產(chǎn)和生產(chǎn)后信息的監(jiān)視是使醫(yī)療器械制造商能夠關閉反饋回路并使風險管理成為連續(xù)生命周期過程的關鍵步驟。在此階段�,從許多不同的來源收集信息,審查其與安全性的相關性����,并在適當?shù)那闆r下反饋到風險管理流程的早期階段,以維持醫(yī)療器械的安全性。
ISO 14971:2019 要求制造商建立一個系統(tǒng)��,以積極收集和審查可能與安全相關的醫(yī)療器械信息����。建立該系統(tǒng)所需的活動記錄在風險管理計劃中。生產(chǎn)和后期生產(chǎn)活動可以是后期市場監(jiān)控系統(tǒng)的一部分��。詳見ISO/TR 20416��,可了解更多有關上市后監(jiān)管的指導�。
在ISO/TR24971中給出了生產(chǎn)和生產(chǎn)后活動的示例。
3.新的ISO/TR 24971:2020包含附錄
附錄A-識別與安全相關的危險和特性
能用作識別影響安全的醫(yī)療器械特性的問題清單已由ISO 14971:2007附錄C移動至ISO/TR 24971 :2020 附錄A��, 并且由34個大問題(C.29包含8個小問題)改為 37個大問題(A.2.31包含9個小問題)�。
附錄B-支持風險分析的技術
本附件提供了可用于支持風險分析的幾種技術的指南。一些技術從可能的傷害開始�,分析可能導致傷害的各種事件。其他技術從引發(fā)事件開始��,分析可能導致傷害的后續(xù)事件序列或組合�。常用的風險分析方法如HAZOP、FMEA����。
附錄C-方針�、風險可接受性標準��、風險控制和風險評價之間的關系
本附件描述了制造商確定最高管理層定義的可接受風險的方針與基于該方針建立的風險可接受性標準之間的關系�。此描述包括可以成為策略一部分的元素。它解釋了如何在風險控制和風險評估中使用風險可接受性標準����。
風險矩陣示例:
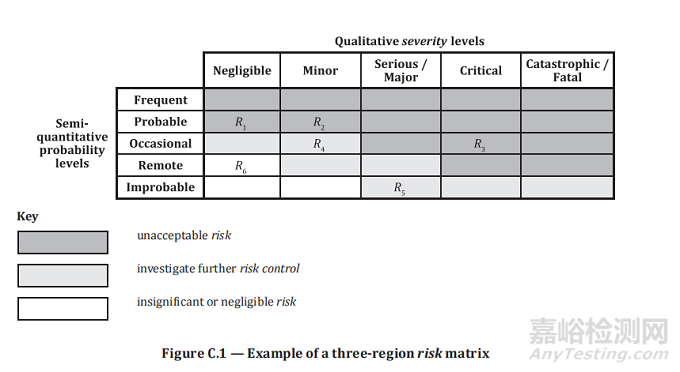
附錄D-安全信息和剩余風險信息
本附錄的目的是闡明“安全信息”和“剩余風險披露”之間的區(qū)別��。它就如何提供安全信息����,以及如何以提高風險意識的方式披露剩余風險提供指南。
附錄E-國際標準在風險管理中的作用
國際標準可以通過對產(chǎn)品和/或過程的安全性提出要求��,在風險管理中發(fā)揮重要作用�。IS0/IEC指南為醫(yī)療器械國際標準的制定和納入安全方面提供指導。國際標準是由該領域的專家制定的����,被認為代表了公認的技術水平。
附錄F-與信息安全相關風險指南
涵蓋了網(wǎng)絡和數(shù)據(jù)安全的風險管理�,以及網(wǎng)絡安全過程與ISO 14971的關系。該專用附錄由ISO和IEC軟件委員會成員共同制定����。
附錄G-設計時未使用ISO 14971的組件和器械
附錄G包含了不按ISO 14971的要求設計的器械和元器件�。附錄G討論了適用于糾正風險管理文件的流程����。當公司修訂其風險管理系統(tǒng)以滿足新版ISO14971的要求時,本節(jié)可能會很有用�。
附錄H-體外診斷(IVD)醫(yī)療器械風險管理指南
附錄H適用于體外診斷器械(IVD),并由ISO 212技術委員會(負責IVD標準的委員會)進行了廣泛的修訂����。這個新的附錄不僅僅對IVD器械有用,而且也包含了對所有醫(yī)療器械有價值的信息�,以獲得一些與您現(xiàn)在所開發(fā)的器械的可能需要的信息,例如如何在風險管理系統(tǒng)中處理假陰性和假陽性����。
4.ISO/TR 24971要點和總結
1.指南總結
在ISO/TR24971描述了制造商能夠用于開發(fā)、實施和保持符合ISO 14971:2019標準的風險管理過程的方法��。替代方法也可以滿足ISO 14971:2019的要求����。
新版風險管理的指南更適用于MDR 法規(guī),它強調(diào)了最新技術state of art和生命周期內(nèi)實施風險分析��、剩余風險及評估受益比的重要性。作為制造商會面臨更加嚴峻的挑戰(zhàn)��,本指南標準為執(zhí)行MDR法規(guī)的符合性奠定了一定的基礎�。
2.指南要點
Ø 制定風險管理計劃,并且按照計劃執(zhí)行風險管理��;
Ø 風險控制措施有效����。
Ø 風險控制措施實施過程中不增加現(xiàn)有風險����。
Ø 每個單獨風險的剩余風險是可以接受的。
Ø 技術水平不落后于行業(yè)水平��。
Ø 符合最新適用標準����。
Ø GSPRs的要求是否滿足?
Ø 剩余風險是否識別�?
Ø 受益風險比


